治疗效果“最大”副作用“最小”!浙江大学研发新型纳米平台,可实现靶向肿瘤药物递送
| 导读 | 多模式治疗需要有效的药物载体,能够以受控方式将多种药物输送到特定位置。 |
8月23日,浙江大学杨明英、毛传斌和杨树旭联合在《Advanced Science》上发表题为“Metal−Organic Frameworks Nucleated by Silk Fibroin and Modified with Tumor-Targeting Peptides for Targeted Multimodal Cancer Therapy”的研究论文,结果表明,AR-ZS/ID-P NPs是一种有前途的多模态治疗诊断纳米平台,具有最大的治疗效果和最小的副作用,用于靶向和可控的药物递送。

https://onlinelibrary.wiley.com/doi/full/10.1002/advs.202302700
研究背景
光疗由光动力疗法(PDT)和光热疗法(PTT)组成,已成为一种有前途的无创和有效的癌症治疗方法。吲哚菁绿(ICG)是PDT/PTT的理想光敏剂,因为它对穿透组织的红外辐射有反应。重要的是,ICG还可用于热成像和近红外荧光成像,以实现图像引导的肿瘤治疗。肿瘤影像学检查为肿瘤的诊断、分期、治疗计划和监测提供了关键信息。然而,游离ICG在体内的亲水性带来了诸如半衰期短和细胞摄取不良等挑战。为了实现PDT/PTT的高时空精度,设计一种能够加载ICG并满足刺激反应释放和肿瘤靶向等要求的智能药物载体至关重要。此外,载体应能够加载和维持化疗药物,以增强化疗和PDT / PTT的协同作用,以改善治疗结果。
沸石咪唑酸盐框架-8(ZIF-8)是金属有机框架(MOF)的一个亚类,为实现可控的药物递送提供了一种可行的解决方案。ZIF-8具有合成可控、化学稳定性好、pH敏感降解等独特特性。此外,ZIF-8的尺寸可以很容易地控制在150nm以下,这有利于“增强的通透性和保留性”(EPR)效应,驱动颗粒靶向肿瘤,并使ZIF-8成为高效,刺激响应药物释放的有希望的候选者。仿生矿化是合成纳米级ZIF-8的简单方法,因为它可以精确控制孔隙形状,化学官能度和大小。因此,确定合适的模板来诱导尺寸小于8 nm的纳米级ZIF-150矿化至关重要。
据报道,生物大分子,如蛋白质、DNA和酶,可用作合成纳米级ZIF-8的生物模板。Bombyx mori (B. mori)丝素蛋白(SF)是一种生物模板,可提供丰富的羧基作为成核位点。我们的团队已成功使用SF作为生物模板来介导磷灰石晶体的成核和沉积和二氧化硅在纳米尺度上。此外,我们确认了ZIF-8在静电纺丝SF纳米纤维上的形成,使得使用SF作为生物模板制备尺寸控制在8 nm的纳米级ZIF-100成为可能。此外,SF本身由于其优异的生物相容性、生物降解性和低免疫原性,可用作药物载体。SF氨基和羧基末端的亲水末端为药物提供了有利的吸附位点,从而提高了载药率。因此,使用SF作为生物模板触发纳米级ZIF-8作为药物载体的成核和沉积是一种合理的方法。
此外,为了提高治疗效率并减少副作用,我们希望将靶药物分子递送到特定的肿瘤部位。肿瘤识别分子,如抗体、叶酸和透明质酸已用于靶向药物递送。然而,这些分子主要与某些类型的蛋白质相互作用,这些蛋白质在肿瘤部位过度表达或明确表达,忽略了相同类型癌症的患者特异性肿瘤差异。为了克服这一挑战,我们利用体内噬菌体展示来鉴定肿瘤靶向肽AREYGTRFSLIGGYR(称为AR),其主动靶向MCF-7肿瘤。我们计划使用AR来引导纳米颗粒(NPs)用于MCF-7乳腺癌治疗中的精准医学。
研究设计
我们设计了一种纳米级ZIF-8,该ZIF-8对pH敏感,并使用化学/ PDT / PTT靶向肿瘤进行协同癌症治疗(方案1)。首先,我们制备SF并将其添加到2-甲基咪唑(2-HmIm)水溶液中以作为生物模板(方案1A)。接下来,我们用混合溶液(方案1B)共培养抗癌药物DOX和光敏剂ICG,然后通过加入Zn2+的一锅工艺快速诱导成核并形成负载DOX / ICG的纳米级ZIF-8(称为ZS / ID NPs)(方案1C)。为了获得MCF-7乳腺肿瘤靶向肽偶联的长期稳定性和丰富的结合位点,我们将聚乙烯亚胺(PEI)涂层引入ZS / ID NP(ZS / ID-P N)(方案1D)。最后,我们将MCF-7乳腺肿瘤靶向肽AR与ZS/ID-P NPs(称为AR-ZS/ID-P NPs)上的PEI联系起来,以选择性抑制乳腺肿瘤(方案1E,F)。通过这种方式,AR-ZS/ID-P NPs由于肿瘤pH响应和肽靶向特性而表现出肿瘤归巢能力,可以实现化疗/PDT/PTT三模式治疗结果。我们发现AR-ZS/ID-P NPs在肿瘤组织中大量积累,实现了超级加性抗肿瘤功效,并减少了光相关副作用。
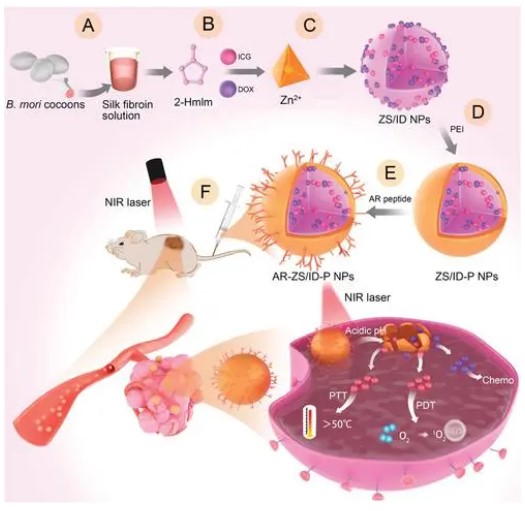
制备AR-ZS/ID-P NPs和靶肽引导乳腺癌治疗的示意图。
研究结论
综上所述,我们开发了一种理想的肿瘤靶向和pH响应纳米平台AR-ZS / ID-P NPs,用于PTT / PDT和化疗的整合,以实现协同癌症治疗。通过调节SF生物模板的浓度,我们获得了尺寸合理、分散性好、ICG和DOX包封效率高的AR-ZS/ID-P NPs。ZIF-8的pH敏感行为在AR-ZS/ID-P NPs中得以维持,允许在酸性肿瘤微环境中触发药物释放,但在中性条件下保持稳定。通过AR肽修饰,AR-ZS/ID-P NPs被选择性归巢并募集到肿瘤细胞中。在激光照射下,ICG产生破坏性热量和ROS以实现PTT和PDT,并启用热成像和荧光成像,可以进一步指导DOX触发的化疗。体内实验证实,AR-ZS/ID-P NPs的肿瘤积累增强,肿瘤生长受到显著抑制。更重要的是,AR-ZS/ID-P NPs具有良好的生物相容性,降低了全身毒性。总的来说,AR-ZS/ID-P NPs代表了一种有前途的多功能载体,用于肿瘤治疗,具有重要的临床应用机会。(转化医学网360zhyx.com)
参考资料:
https://onlinelibrary.wiley.com/doi/full/10.1002/advs.202302700
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录

还没有人评论,赶快抢个沙发