首次!“双向调控”策略——抑制肿瘤免疫逃逸!山大齐鲁联合郑大发文
| 导读 | 低水平的肿瘤免疫原性和免疫检查点依赖性抑制引起的肿瘤免疫逃逸限制了免疫治疗效果。 |
近日,山东大学齐鲁医学院学者联合郑州大学人民医院学者在期刊《Advanced Science》上发表题为“Nano-Regulator Inhibits Tumor Immune Escape via the “Two-Way Regulation” Epigenetic Therapy Strategy”的研究论文,研究结果表明,纳米调节因子CG-J/ZL可以上调TAAs的表达以增强T细胞浸润,下调PD-L1的表达以改善T细胞对肿瘤细胞的识别,代表了一种有前途的改善抗肿瘤免疫应答的策略。

https://onlinelibrary.wiley.com/doi/10.1002/advs.202305275
研究背景
01
免疫疗法是治疗肿瘤最有效的方法之一。然而,大多数患者没有从免疫治疗中获益,免疫治疗的总缓解率仅为10%-35%。免疫编辑理论指出,免疫逃逸是免疫治疗的最大障碍,包括肿瘤免疫原性水平低和免疫检查点依赖性抑制,导致T细胞瘤内浸润不足和T细胞对肿瘤细胞的识别不足。
表观遗传调控是肿瘤免疫逃逸的重要原因。DNA 甲基化是主要的表观遗传调控之一,通过在控制基因表达的 DNA 甲基转移酶 (DNMT) 的催化下向 DNA 中添加甲基(CH3)基团而发生。据报道,肿瘤相关抗原(TAAs)启动子区域存在DNA高甲基化,通过降低TAAs表达导致肿瘤免疫原性水平低,从而降低抗原呈递细胞(APC)向T细胞呈递抗原的能力。因此,抑制肿瘤细胞的DNA高甲基化有望直接上调TAAs的表达,从而增加肿瘤免疫原性并增强T细胞的瘤内浸润。
肿瘤细胞除了通过表观遗传调控DNA高甲基化来抑制肿瘤抗原表达外,还可以调节组蛋白乙酰化机制来控制免疫检查点的表达。程序性死亡-1(PD-1)是一种主要在T细胞上表达的受体,可降低免疫反应。肿瘤细胞表面表达大量程序性细胞死亡1配体1(PD-L1),通过与T细胞上的PD-1受体结合,帮助肿瘤细胞逃避免疫监视。因此,抑制肿瘤细胞中PD-L1的表达是阻断PD-1/PD-L1的有效手段,从而重新激活T细胞以杀死肿瘤。PD-L1由位于9p24.1染色体上的CD274基因编码,9p24.1染色质结构和性质的变化直接影响PD-L1的表达。溴结构域和额外末端结构域(BET)蛋白家族是组蛋白乙酰化的表观遗传读取器,可以调节基因转录。溴结构域蛋白4(BRD4), BET蛋白家族成员,主要参与PD-L1的表达,PD-L1可与CD274启动子和增强子区域的乙酰化组蛋白H3K27Ac结合,促进PD-L1的表达。因此,使用BDD4抑制剂可以有效阻断PD-1/PD-L1免疫检查点,从而重新激活免疫效应细胞对肿瘤细胞的杀伤。
研究设计
02
基于表观遗传调控对肿瘤免疫逃逸的显著影响,首次提出了一种“双向调控”表观遗传治疗策略,通过整合的纳米调节因子抑制肿瘤免疫逃逸,上调TAAs表达以提高免疫原性,下调PD-L1表达阻断PD-1/PD-L1免疫检查点。
为了设计纳米调节剂,将DNMT抑制剂zebularine(Zeb)和BRD4抑制剂JQ1通过静电相互作用与缩合的Toll样受体9(TLR9)激动剂CpG[33-36](G-J/ZL)共同加载到阳离子脂质体中,然后在G-J/ZL表面包覆靶向配体天冬酰胺-甘氨酸-精氨酸(NGR)修饰的电荷逆转材料羧甲基壳聚糖(CMCS),构建核壳结构CG-J/ZL。在NGR的介导下,CG-J/ZL可以靶向肿瘤组织,并在酸性TME下触发拆解。Zeb通过抑制DNA甲基转移酶,有效上调肿瘤表面的TAAs,从而增强肿瘤免疫原性,提高免疫识别能力。JQ1可抑制PD-L1表达,阻断免疫检查点阻断;CpG 作为 TLR9 激动剂,可以促进树突状细胞 (DC) 成熟,从而与 Zeb 合作促进 T 细胞的活化。此外,CpG可以“唤醒”肿瘤相关巨噬细胞(TAM),并重新激活TAM杀死肿瘤细胞的能力。
研究结果
03
本研究成功构建了纳米调节剂CG-J/ZL,表征了CG-J/ZL的理化性质和pH响应性分解,考察了CG-J/ZL的肿瘤蓄积能力和共递送能力,评价了CG-J/ZL的“双向调控”能力,包括TAAs表达上调和PD-L1表达下调。此外,还评估了T细胞、DC、TAM、细胞毒性T淋巴细胞(CTL)和细胞因子分泌的肿瘤内浸润。我们进一步将PD-1单克隆抗体与纳米调节因子CG-J/ZL联合使用,以评估其抗肿瘤作用和抗转移功效。综上所述,CG-J/ZL可以上调TAAs表达以增强T细胞浸润,下调PD-L1表达以改善T细胞对肿瘤细胞的识别,从而抑制肿瘤免疫逃逸,这为改善抗肿瘤免疫应答提供了一种有前途的策略(图1)。(转化医学网360zhyx.com)
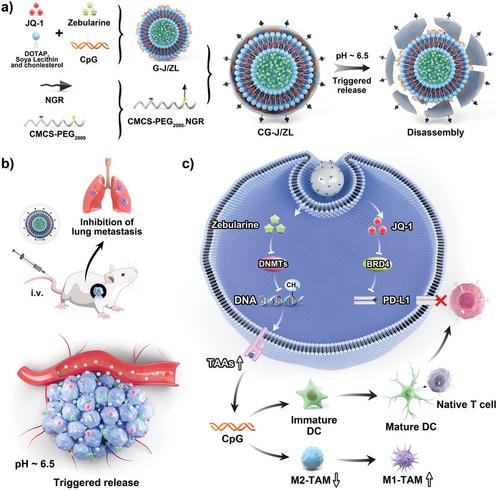
图1:集成纳米调节因子通过“双向调节”表观遗传治疗策略抑制肿瘤免疫逃逸的示意图。
参考资料:
https://onlinelibrary.wiley.com/doi/10.1002/advs.202305275
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录

还没有人评论,赶快抢个沙发