创新视角!上海交通大学李斌等团队:揭示肿瘤免疫治疗新靶点
| 导读 | 靶向肿瘤浸润调节性T细胞(Tregs)是引发抗肿瘤免疫反应的有效途径。然而,Tregs如何保持其脆弱性和稳定性在很大程度上仍然未知。 |
1月2日,上海交通大学李斌教授/李鹤成教授及中国科学院深圳先进技术研究院潘璠教授在期刊《Nature Communications》上发表了研究论文,题为“FOXP3+ regulatory T cell perturbation mediated by the IFNγ-STAT1-IFITM3 feedback loop is essential for anti-tumor immunity”。本研究中,研究人员发现IFITM3-缺陷的Tregs通过增强肿瘤杀伤反应来减弱肿瘤生长,并表现出Th1样Treg表型,IFNγ分泌更高。从机制上讲,IFITM3的敲除增强了STAT1的翻译和磷酸化。相反,在STAT1缺陷的treg中,IFITM3表达减少表明STAT1反过来调控IFITM3的表达,形成一个反馈回路。阻断炎性细胞因子IFNγ或直接敲除STAT1-IFITM3轴,可在肿瘤模型中恢复肿瘤浸润性Tregs的抑制功能。总之,研究表明,通过IFNγ-IFITM3-STAT1反馈回路干扰肿瘤浸润的Treg对抗肿瘤免疫不可或缺,并成为了肿瘤免疫治疗的靶点。

https://www.nature.com/articles/s41467-023-44391-9#Sec12
研究背景
01
FOXP3表达调节性T细胞(Tregs)可以抑制自身免疫反应,但也影响抗肿瘤免疫。Tregs存在于整个肿瘤微环境(TME)中,可以发挥相当大的抑制功能,形成物理、代谢和运输“屏障”,将促炎细胞排除在TME之外。在人类中,消耗Treg细胞实现抗肿瘤免疫正在临床试验中,扩大Treg细胞群体治疗自身免疫性疾病也显示出相当大的疗效。在TME中,通过诱导Treg脆性改变Treg功能,降低FOXP3的表达,增加肿瘤杀伤细胞因子如干扰素γ (IFNγ)的产生,可能有助于抗肿瘤治疗。然而,了解Treg细胞的脆弱性和稳定性在TME中是如何调节的,以及这种调节是否有助于微调免疫反应,仍然具有挑战性。
IFNγ作为ⅱ型干扰素的一员,因其对固有免疫和适应性免疫的调节作用而闻名。IFNγ可通过caspase途径和Fas/ fasl途径诱导肿瘤细胞凋亡。它可以调节抗原的呈递,促进炎症,以及反应性白细胞的激活和极化。此外,它还对T细胞具有直接的抗增殖作用。根据之前的数据,E3去泛素化酶USP21阻止FOXP3的耗竭,并限制th1样Treg细胞的生成。值得注意的是,向Th1样表型分化的Treg细胞有助于癌症的免疫治疗。
研究进展
02
由于IFITM3与肿瘤进展及其缺陷诱导的Treg细胞不稳定性有关,研究人员假设IFITM3参与调节TME中的Treg细胞。为了验证这一假设,我们在WT和cKO小鼠皮下接种MC38小鼠结肠癌细胞,以确定体内Treg细胞的抗肿瘤反应是否需要Ifitm3。总之,结果表明,Treg细胞中IFITM3的缺陷有助于肿瘤杀伤细胞的浸润和TME中效应细胞因子的产生,从而导致更强的抗肿瘤反应。研究结果进一步支持了在IFITM3缺陷的情况下,TI-Tregs的免疫抑制功能受损。然而,在肿瘤模型中,外周Treg细胞没有明显差异,这表明IFITM3在Treg细胞中的作用依赖于肿瘤微环境。
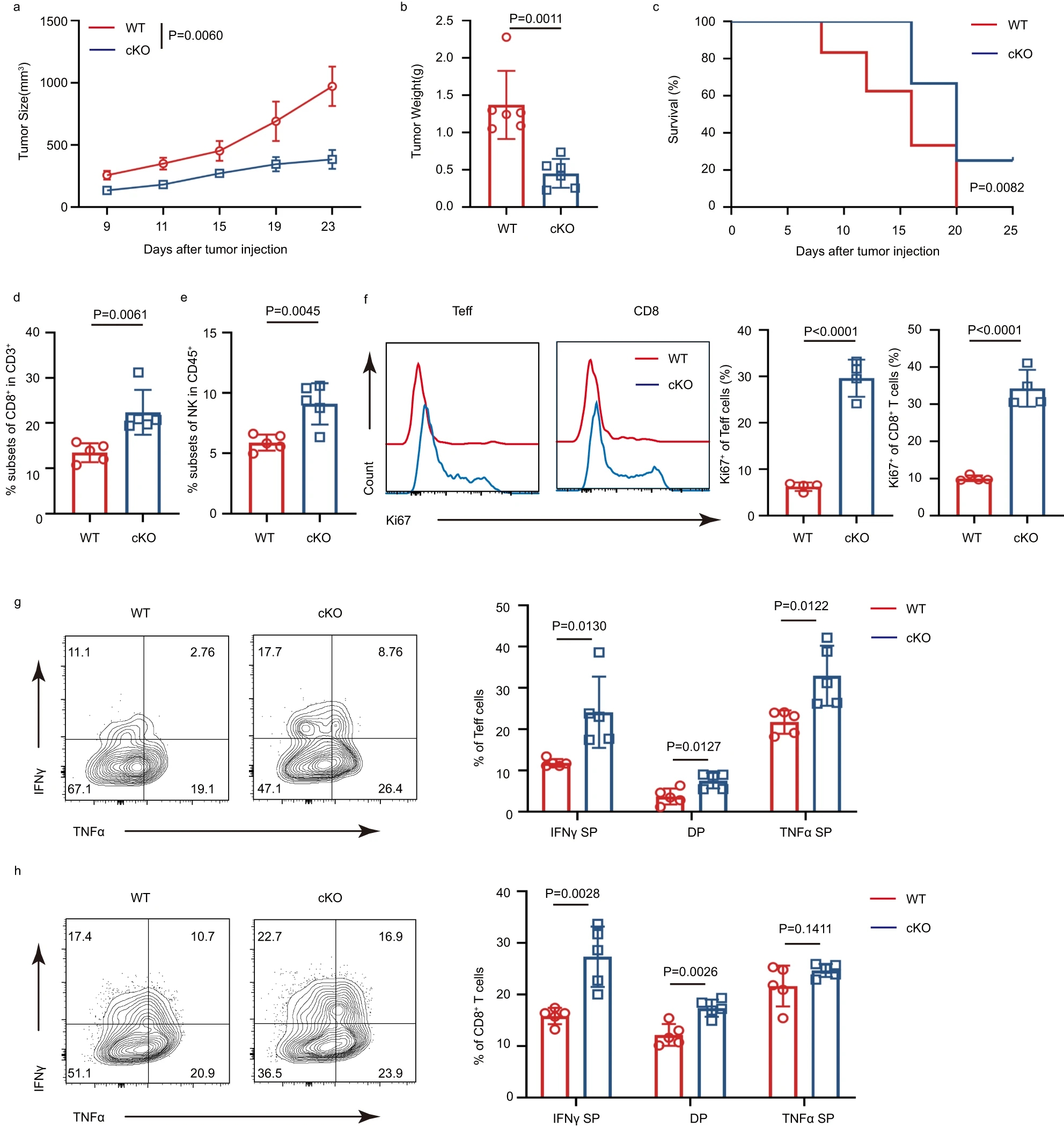
图1:IFITM3缺陷的treg细胞可促进体内抗肿瘤反应
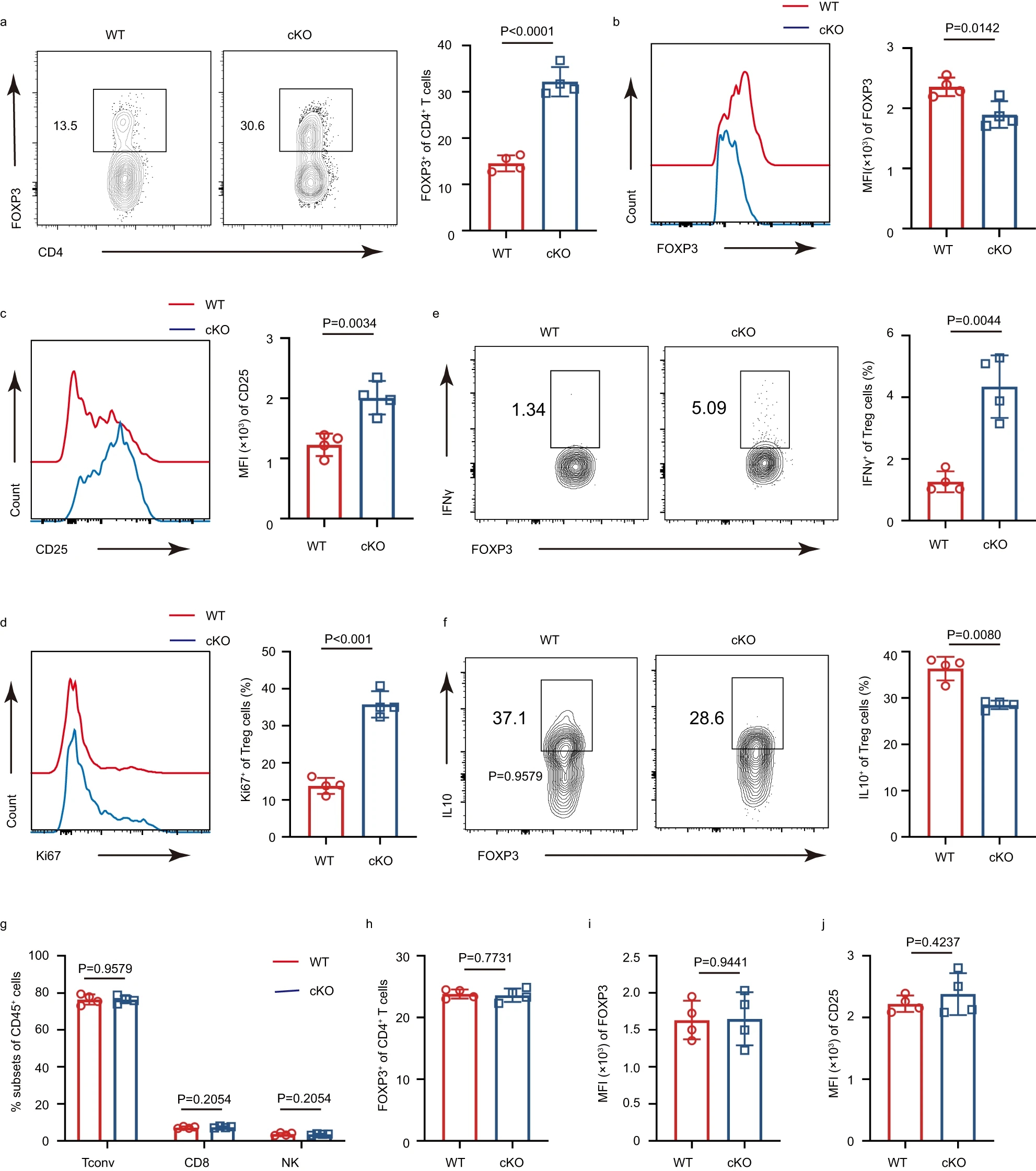
图2:IFITM3 消融可抑制肿瘤中Treg的功能和稳定性
研究结论
03
综上所述,研究人员发现STAT1-IFITM3的反馈回路维持了肿瘤微环境中Treg的功能和稳定性,为临床患者实现抗肿瘤免疫提供了创新的见解和靶点。本研究也为靶向Treg扰动调节IFNγ富集的肿瘤微环境中的抗肿瘤免疫提供了创新的视角。(转化医学网360zhyx.com)
参考资料:
https://www.nature.com/articles/s41467-023-44391-9#Sec12
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录

还没有人评论,赶快抢个沙发