靶向“铁死亡”!复旦大学詹成教授合作发文:癌症治疗迎来新机遇
| 导读 | 铁死亡是一种铁依赖的调节性细胞死亡形式,由致命的脂质过氧化物过载引发。在癌症治疗中,由于对肿瘤代谢特征和铁死亡脆弱性交集的了解有限,因此难以靶向铁死亡。 |
3月19日,复旦大学詹成教授与德克萨斯大学安德森癌症中心甘波谊(Boyi Gan)博士合作在期刊《Nature Communications》上发表了研究论文,题为“Polyamine-mediated ferroptosis amplification acts as a targetable vulnerability in cancer”。本研究中,研究人员注意到铁死亡细胞释放增强的含多胺的胞外囊泡到微环境中,从而进一步使邻近细胞对铁死亡敏感,并加速铁死亡在肿瘤区域的“传播”。此外,多胺补充也通过诱导铁死亡使癌细胞或异种移植肿瘤对放疗或化疗敏感。研究结果表明,多胺代谢暴露了铁死亡的可靶向脆弱性,并为癌症治疗带来了令人兴奋的机会。

https://www.nature.com/articles/s41467-024-46776-w
研究背景
01
铁死亡是指由质膜或膜细胞器中不受限制的脂质过氧化引发的一种铁依赖性细胞死亡形式,由于其独特的机制和形态学特征,它不同于其他形式的调控细胞死亡,如凋亡。简而言之,在一个富铁微环境中,过载的H2O2与铁在芬顿反应中产生高活性的羟基自由基,这些自由基攻击和过氧化位于细胞膜上的含多不饱和脂肪酸(PUFA)的磷脂的双烯丙基部分,从而导致膜破裂和铁死亡细胞死亡。同时,为了抵消这种影响,细胞进化出多种铁死亡防御机制。由于两个过程之间的不平衡,如铁死亡诱导因子(FINs)导致的防御途径失活,导致脂质过氧化物的快速积累,并触发有效的铁死亡细胞死亡。
研究发现
02
本研究结果支持了铁死亡细胞不仅增强细胞内多胺合成,而且以EV依赖的方式向肿瘤微环境释放多胺的观点。这种现象可能被认为是一种自发的自我保护机制,以输出铁死亡过程中产生的过载多胺。然而,释放的多胺进一步使邻近细胞对FINs敏感,从而加速了铁死亡在肿瘤区域的“传播”。
研究人员通过TCGA数据库的基因表达分析,发现ODC1表达水平在多种癌症中比其相应的正常组织显著上调,包括肺腺癌(LUAD)、肺鳞癌(LUSC)、食管癌(ESCA)、胶质母细胞瘤(GBM)、头颈部癌(HNSC)等。同时,研究小组发表的一项单细胞RNA-seq研究,重点关注17个LUAD组织和12个正常肺组织,也表明癌细胞中的ODC1水平比其他细胞类型上调。研究人员通过使用获得的手术切除的LUAD样本进行蛋白印迹验证了这一生物信息学结果,从而暗示了肿瘤区域多胺合成的增强。研究人员对一个LUAD组织切片进行了空间分辨代谢组学,并使用苏木精-伊红(H&E)染色区分肿瘤和正常组织。如图1e所示,研究人员注意到肿瘤区域内腐胺、亚精胺和精胺的显著富集,这与之前的研究结果一致。
一般认为,多胺上调会促进肿瘤转化、增殖和进展。然而,考虑到多胺的强效促铁死亡作用,多胺合成的增加不再是导致肿瘤发展的“坏小子”,而是使癌细胞内在易受铁死亡的影响,从而暴露出在特定情况下可以作为治疗靶点的脆弱性。
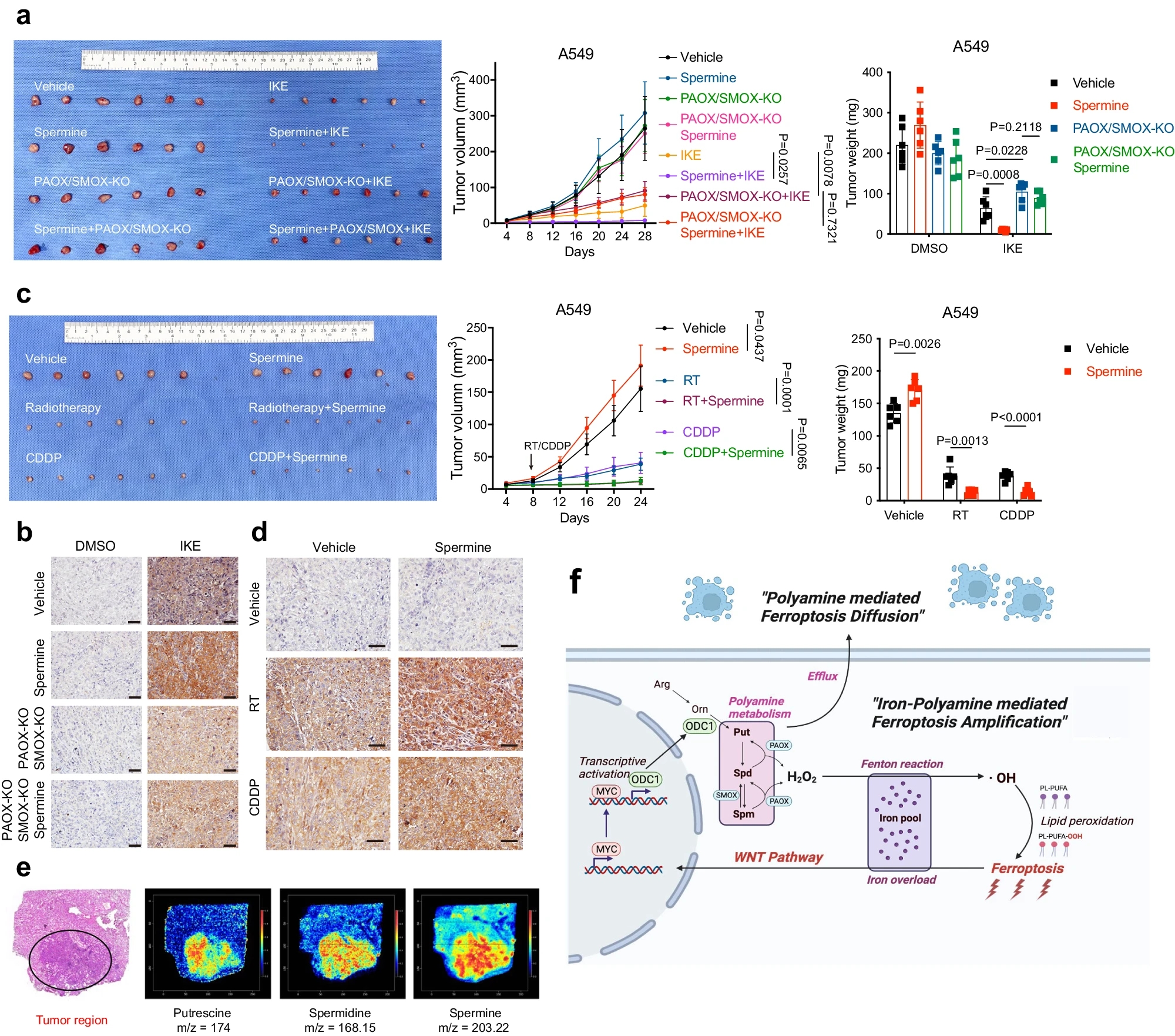
图1:多胺代谢是基于铁死亡的癌症治疗的潜在靶点
研究结论
03
总之,通过鉴定精氨酸作为铁死亡的中介,本研究阐明了多胺的强效促铁死亡特性和相应的机制,以及铁过载-WNT/MYC/ODC1-多胺-H2O2正反馈轴,该轴放大了铁死亡。本研究结果还提出了以前未被重视的多胺过载肿瘤的代谢易感性,这可能为铁死亡相关癌症治疗提供潜在的靶点和策略。(转化医学网360zhyx.com)
参考资料:
https://www.nature.com/articles/s41467-024-46776-w
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录

还没有人评论,赶快抢个沙发