两篇Science聚焦衰老相关蛋白酶
| 导读 |
本期Science杂志发表了两项研究,研究人员分别获得了两种蛋白酶的三维晶体结构,人类ZMPSTE24及其酵母类似物Ste24p。这两项结构研究,将帮助人们更好的理解这类蛋白酶的功能,并由此解析它们与衰老的关系。
若核纤层蛋白lamin A或金属蛋白酶ZMPSTE24的编码基因发生了突变,就会引发严重的早老病HGPS和一些相关疾病,如限制性皮肤... |
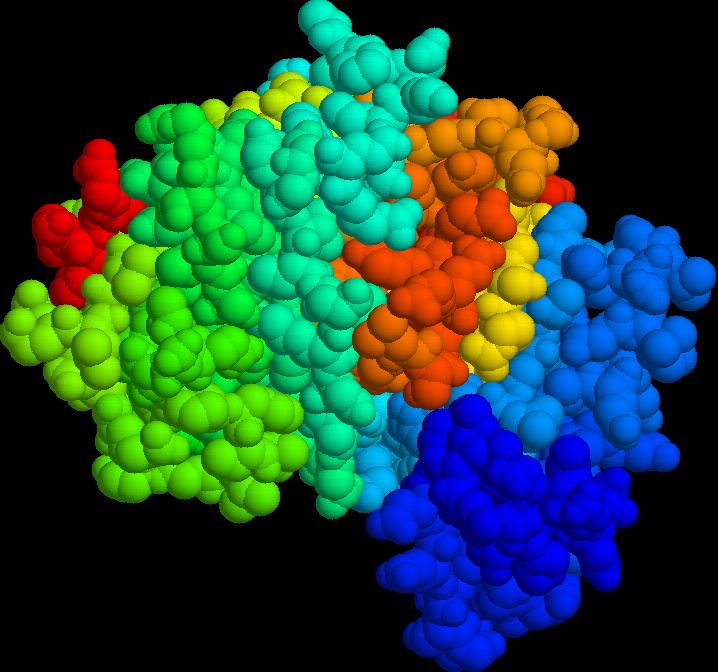
本期Science杂志发表了两项研究,研究人员分别获得了两种蛋白酶的三维晶体结构,人类ZMPSTE24及其酵母类似物Ste24p。这两项结构研究,将帮助人们更好的理解这类蛋白酶的功能,并由此解析它们与衰老的关系。
若核纤层蛋白lamin A或金属蛋白酶ZMPSTE24的编码基因发生了突变,就会引发严重的早老病HGPS和一些相关疾病,如限制性皮肤病RD和MAD-B(mandibuloacral dysplasia)。患有HGPS的儿童会加速衰老,其症状包括生长迟缓、脱发、关节病、脂肪营养不良和心血管疾病等,患儿往往会在青少年时期死亡。这些早衰疾病被认为是由lamin A的持续法尼基化和甲基化引起的。
本期Science杂志发表了两项研究,研究人员分别获得了两种蛋白酶的三维晶体结构,人类ZMPSTE24及其酵母类似物Ste24p。这两种蛋白酶对lamin A和酵母交配信息素a-factor的成熟过程,具有关键作用。这两项结构研究,将帮助人们更好的理解这类蛋白酶的功能,并由此解析它们与衰老的关系。
ZMPSTE24的底物lamin A,负责维持细胞核的结构完整性。prelamin A是lamin A的前体,其C端末尾具有一个CAAX结构。prelamin A与其他CAAX蛋白类似,都会经历三次翻译后修饰。不过除此之外,prelamin A的成熟还要经历二次剪切,而这两次剪切都由ZMPSTE24所介导。Quigley等人揭示了ZMPSTE24的晶体结构,人们可以在此基础上了解该蛋白酶识别剪切位点的机制,以及 lamin A的二次剪切过程。
研究人员指出,在衰老相关疾病中,lamin A的C端修饰和剪切很重要,说明金属蛋白酶在人类的正常衰老过程中具有关键作用。因此,有必要确保新蛋白酶抑制剂及其他药物,不会经脱靶效应影响了ZMPSTE24的功能。目前已经有体外研究显示,一些HIV蛋白酶抑制剂干扰了ZMPSTE24,由此导致了HIV治疗中的副作用。
此外,研究人员还发现,人类ZMPSTE24和酵母Ste24p的结构中,存在大量膜包围的空腔,可以作为酶促反应的场所。据Pryor等人估计,这种空腔足以容纳约450个水分子或者一个约10 kD的蛋白。研究人员还在结构研究的基础上,阐明了MAD-B和RD致病突变阻断蛋白酶活性的机制。
ZMPSTE24/Ste24p的晶体结构,为其底物的二次剪切机制提供了线索。人们曾经认为,ZMPSTE24/Ste24p在一次剪切后,可能先释放底物,等甲基化之后再与底物结合。但研究显示,这是一个持续的过程,底物从未完全离开。第一次剪切后,底物在酶中移动,伸出一部分进行甲基化,然后再缩回来进行最后的剪切。
研究人员指出,确定ZMPSTE24的作用机制,将为相关治疗药物的开发带来重要启示,帮助人们避免阻断关键蛋白酶的功能。此外,这些知识将会扩展我们对早老病以及正常生理性衰老的理解。
原文链接:
The Structural Basis of ZMPSTE24-Dependent LaminopathiesStructure of the Integral Membrane Protein CAAX Protease Ste24p
来源:生物通
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发