检测方法新突破:分子诊断应用于肿瘤研究
| 导读 | 临床医生越来越重视的诊断工具是可检测基因变化和蛋白表达等分子方法,这些改变的基因和蛋白表达促进了肿瘤的发生、发展、预后和异质性,并成为治疗方案选取的依据以及解释肿瘤药物抗性。
研究人员和临床医生利用测序技术,以及基因组学、蛋白质组学和代谢组学方法去识别生物标记分子,后者有望用在遗传诊断、药物研发和临床药物测试的患者分类。
在最近召开的美国癌症研究学会(AACR)上,Mizuho Secur... |
临床医生越来越重视的诊断工具是可检测基因变化和蛋白表达等分子方法,这些改变的基因和蛋白表达促进了肿瘤的发生、发展、预后和异质性,并成为治疗方案选取的依据以及解释肿瘤药物抗性。
研究人员和临床医生利用测序技术,以及基因组学、蛋白质组学和代谢组学方法去识别生物标记分子,后者有望用在遗传诊断、药物研发和临床药物测试的患者分类。
在最近召开的美国癌症研究学会(AACR)上,Mizuho Securities机构的分析师指出,分子诊断明显是肿瘤学的重要组成部分,即便大多数与会人士认为短期内分子诊断不能取代现存的诊断法,但是肿瘤基因组测序这一领域仍让多数人持乐观态度。报告提到了,更好的生物标记分子和诊断法被迫切需要,而那些处于研发阶段、较早使用的生物标记分子和诊断法仍是被低水平利用,此外,基因组学明显地驱动肿瘤学研发的许多方面。
在AACR会议上几位演讲嘉宾强调了,分子诊断法应用于肿瘤学和肿瘤诊断产品的研发。来自Flagship Biosciences和 Affymetrix/Panomics公司的Mirza Peljto等人员,研发了一种定量方法可原位检测人体肿瘤样本中肿瘤RNA和蛋白的表达量,以供生物标记分子的识别和新诊断方法的研发。在乳腺癌中,Her癌基因的表达提高了约30%,但是研究人员还不清楚乳腺癌中Her2基因表达和蛋白表达之间的关联。
研究人员利用发光RNA(在原位杂交法和免疫组化中使用的)研发出基于定量分析的成像检测法,其中Her2蛋白和RNA水平在不同组织之间进行原位比较。这一方法支持了在整个组织切片中检测Her2 RNA,并将其与膜蛋白表达进行关联。据Peljto称:“该方法以自动方式提高了诊断一致性,也提高了对整个切片上所用肿瘤细胞的评估可信度”。
研究者利用CellMap™算法能区分处于高水平或低水平表达的活检样本,以分析生成的数字图像,识别肿瘤细胞(从周围正常细胞中),以及将图像转换成细胞中的标记分子图谱并定量标记分子(RNA和蛋白质)的水平。
作者报道了HER2在RNA和蛋白表达水平上蛋白表达之间的79%的一致性,并得出了以下结论:结合分子和成像在分析临床肿瘤样本中具有实际可行性;将完整切片的IHC和CISH自动注解整合后用在分子评测中,可有助于解决长期以来病理学家在人工评测中所存在的问题,并提高了基于RNA的读出数据(同时转换成基于CISH的读出数据)的一致性。
DNA和蛋白质标记分子分析
Predictive Biosciences公司利用临床干预决定诊断方法(Clinical Intervention Determining Diagnostic,CIDD),开发出商业用途的肿瘤诊断测试。上述方法在测试DNA和蛋白质标记分子的基础上利用了多分析物的诊断读出数据,从而确保了90%的检测灵敏度和特异性。在AACR会议上,公司代表还谈到关于膀胱癌相关的突变基因和表观遗传变化的检测。
取代之前定义的阳性/阴性结果,此方法基于患癌风险系数将人群分为三类:高风险患癌群体(识别致癌基因以最快的、最大程度地进行医治)、可能患癌群体(接受适当的治疗)和无患癌风险群体(不需要接受安全评估和治疗)。
应用科学主任Cecilia Fernandez 称:“将高特异性的DNA标记分子和蛋白质标记分子(基于诊断测试发现的)结合后,基本上能把DNA标记分子呈阳性的样本对应为高风险群体以备医学治疗。此外,灵敏度提高的多分析物测试支持了较高水平的蛋白标记分子设置标准,从而让更高比例的群体被定义为无患癌风险群体(基于尿液检测),以避免进一步的检测和创伤性组织取样。”
Predictive Biosciences公司的John Millholland在演讲中侧重于那些应用下一代测序技术对扩增子深度测序的研究,通常这一测序技术能够在突变DNA仅为正常DNA 0.02%这一很小比例时定量地检测突变基因,这就支持了尿液样本取代膀胱组织样本。
作者提到,相比于定量PCR,FGFR3扩增子的深度测序法在组织和尿液中产生高度一致性的基因突变——在一致性上测序法为90%而定量PCR约为50%。Millholland报告称,利用深度测序法分别在尿液和组织样本中检测其它突变位点,发现尿液更具代表整体器官(而非组织切片),有望成为肿瘤取样的随机样本。
当研究者添加膀胱癌相关的另一个突变基因TP53时,测试结果在准确性提高了。研究发现,没有重叠样本出现GFR3 和TP53突变基因的阳性结果,而在测试中这两个突变基因相互补充,它们之间的相互作用提高了测试的灵敏度。首席技术官Anthony P. Shuber称:“将TP53 整合到目前的FGFR3测试中,我们能提供针对所有阶段、不同程度膀胱癌的最佳检测法。”
Predictive Biosciences公司的另一研究者介绍了可在尿液等体液中检测甲基化基因的技术,将其整合到多分析物诊断测试(上面提到的硫酸氢盐下一代测序方法)中,以识别在单碱基水平上的CpG位点甲基化。
识别甲基化变化模式是日益重要的肿瘤诊断方法,作者提到:“该方法可用于检测体液中的其它高度甲基化的基因,这些体液中的甲基化比例仍低于肿瘤组织样本中的”。 Shuber解释道,通过研发出将所有标记分子(能够在下一代测序系统NGS运行)进行整合的新测试, 我们提高了高通量,降低了成本,从而让该测试可应用于开发体外诊断试剂盒。

来源:生物探索
研究人员和临床医生利用测序技术,以及基因组学、蛋白质组学和代谢组学方法去识别生物标记分子,后者有望用在遗传诊断、药物研发和临床药物测试的患者分类。
在最近召开的美国癌症研究学会(AACR)上,Mizuho Securities机构的分析师指出,分子诊断明显是肿瘤学的重要组成部分,即便大多数与会人士认为短期内分子诊断不能取代现存的诊断法,但是肿瘤基因组测序这一领域仍让多数人持乐观态度。报告提到了,更好的生物标记分子和诊断法被迫切需要,而那些处于研发阶段、较早使用的生物标记分子和诊断法仍是被低水平利用,此外,基因组学明显地驱动肿瘤学研发的许多方面。
成像检测法在肿瘤研究中应用
在AACR会议上几位演讲嘉宾强调了,分子诊断法应用于肿瘤学和肿瘤诊断产品的研发。来自Flagship Biosciences和 Affymetrix/Panomics公司的Mirza Peljto等人员,研发了一种定量方法可原位检测人体肿瘤样本中肿瘤RNA和蛋白的表达量,以供生物标记分子的识别和新诊断方法的研发。在乳腺癌中,Her癌基因的表达提高了约30%,但是研究人员还不清楚乳腺癌中Her2基因表达和蛋白表达之间的关联。
研究人员利用发光RNA(在原位杂交法和免疫组化中使用的)研发出基于定量分析的成像检测法,其中Her2蛋白和RNA水平在不同组织之间进行原位比较。这一方法支持了在整个组织切片中检测Her2 RNA,并将其与膜蛋白表达进行关联。据Peljto称:“该方法以自动方式提高了诊断一致性,也提高了对整个切片上所用肿瘤细胞的评估可信度”。
研究者利用CellMap™算法能区分处于高水平或低水平表达的活检样本,以分析生成的数字图像,识别肿瘤细胞(从周围正常细胞中),以及将图像转换成细胞中的标记分子图谱并定量标记分子(RNA和蛋白质)的水平。

CellMap™算法识别和定量Her2基因
作者报道了HER2在RNA和蛋白表达水平上蛋白表达之间的79%的一致性,并得出了以下结论:结合分子和成像在分析临床肿瘤样本中具有实际可行性;将完整切片的IHC和CISH自动注解整合后用在分子评测中,可有助于解决长期以来病理学家在人工评测中所存在的问题,并提高了基于RNA的读出数据(同时转换成基于CISH的读出数据)的一致性。
DNA和蛋白质标记分子分析
Predictive Biosciences公司利用临床干预决定诊断方法(Clinical Intervention Determining Diagnostic,CIDD),开发出商业用途的肿瘤诊断测试。上述方法在测试DNA和蛋白质标记分子的基础上利用了多分析物的诊断读出数据,从而确保了90%的检测灵敏度和特异性。在AACR会议上,公司代表还谈到关于膀胱癌相关的突变基因和表观遗传变化的检测。
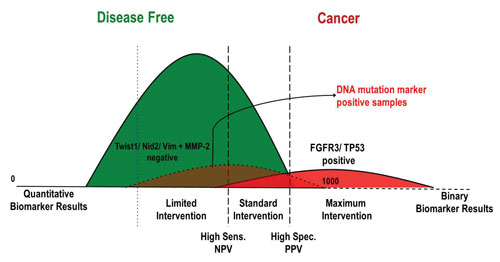
取代之前定义的阳性/阴性结果,此方法基于患癌风险系数将人群分为三类:高风险患癌群体(识别致癌基因以最快的、最大程度地进行医治)、可能患癌群体(接受适当的治疗)和无患癌风险群体(不需要接受安全评估和治疗)。

应用科学主任Cecilia Fernandez 称:“将高特异性的DNA标记分子和蛋白质标记分子(基于诊断测试发现的)结合后,基本上能把DNA标记分子呈阳性的样本对应为高风险群体以备医学治疗。此外,灵敏度提高的多分析物测试支持了较高水平的蛋白标记分子设置标准,从而让更高比例的群体被定义为无患癌风险群体(基于尿液检测),以避免进一步的检测和创伤性组织取样。”
Predictive Biosciences公司的John Millholland在演讲中侧重于那些应用下一代测序技术对扩增子深度测序的研究,通常这一测序技术能够在突变DNA仅为正常DNA 0.02%这一很小比例时定量地检测突变基因,这就支持了尿液样本取代膀胱组织样本。
作者提到,相比于定量PCR,FGFR3扩增子的深度测序法在组织和尿液中产生高度一致性的基因突变——在一致性上测序法为90%而定量PCR约为50%。Millholland报告称,利用深度测序法分别在尿液和组织样本中检测其它突变位点,发现尿液更具代表整体器官(而非组织切片),有望成为肿瘤取样的随机样本。
当研究者添加膀胱癌相关的另一个突变基因TP53时,测试结果在准确性提高了。研究发现,没有重叠样本出现GFR3 和TP53突变基因的阳性结果,而在测试中这两个突变基因相互补充,它们之间的相互作用提高了测试的灵敏度。首席技术官Anthony P. Shuber称:“将TP53 整合到目前的FGFR3测试中,我们能提供针对所有阶段、不同程度膀胱癌的最佳检测法。”
Predictive Biosciences公司的另一研究者介绍了可在尿液等体液中检测甲基化基因的技术,将其整合到多分析物诊断测试(上面提到的硫酸氢盐下一代测序方法)中,以识别在单碱基水平上的CpG位点甲基化。
识别甲基化变化模式是日益重要的肿瘤诊断方法,作者提到:“该方法可用于检测体液中的其它高度甲基化的基因,这些体液中的甲基化比例仍低于肿瘤组织样本中的”。 Shuber解释道,通过研发出将所有标记分子(能够在下一代测序系统NGS运行)进行整合的新测试, 我们提高了高通量,降低了成本,从而让该测试可应用于开发体外诊断试剂盒。

来源:生物探索
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发