FDA批准RAM联合紫杉醇用于晚期胃癌
| 导读 | FDA于2014年11月5日批准了ramucirumab联合紫杉醇用于治疗晚期胃癌及胃食管连接部腺癌。 |
FDA于2014年11月5日批准了ramucirumab联合紫杉醇用于治疗晚期胃癌及胃食管连接部腺癌。
Ramucirumab (Cyramza, Lilly)曾在2014年4月获准用于单药治疗经氟尿嘧啶或含铂化疗或治疗后出现疾病进展的晚期胃癌及胃食管连接部腺癌。
礼来肿瘤产品开发和医学事务部的高级副总裁Richard Gaynor博士对媒体表示;“这次FDA对Cyramza的批准,代表了人们与毁灭性难治性疾病斗争的又一个里程碑。”
RAINBOW研究
FDA此次的批准是基于一项3期临床试验RAINBOW的结果。在这项多中心、双盲、以安慰剂为对照的研究中,共纳入了665位经治的晚期或转移性胃癌或胃食管连接部腺癌患者。
研究详情:【ASCO2014】RAINBOW:RAM+紫杉醇方案使mGC患者预后获益
这项研究的有效终点包括,首要终点OS,次要终点PFS和客观缓解率。
患者被随机分配入组,其中330位患者接受ramucirumab (8 mg/kg 每两周)联用紫杉醇(80 mg/m2 每周一次,在每28天的一个周期中使用3周);另外的患者接受安慰剂加紫杉醇治疗(n=335)。
据研究结果显示,ramucirumab联用紫杉醇组患者的中位OS为9.6个月,安慰剂加紫杉醇组患者的中位OS为7.4个月(HR=0.81; 95% CI, 0.68-0.96)。
研究者们还发现ramucirumab联用紫杉醇组患者的PFS也明显延长(HR=0.64; 95% CI, 0.54-0.75)。
研究纳入的665例患者中,140例是日本患者,398例是西方患者。日本和西方患者的效能结果对比如下表。
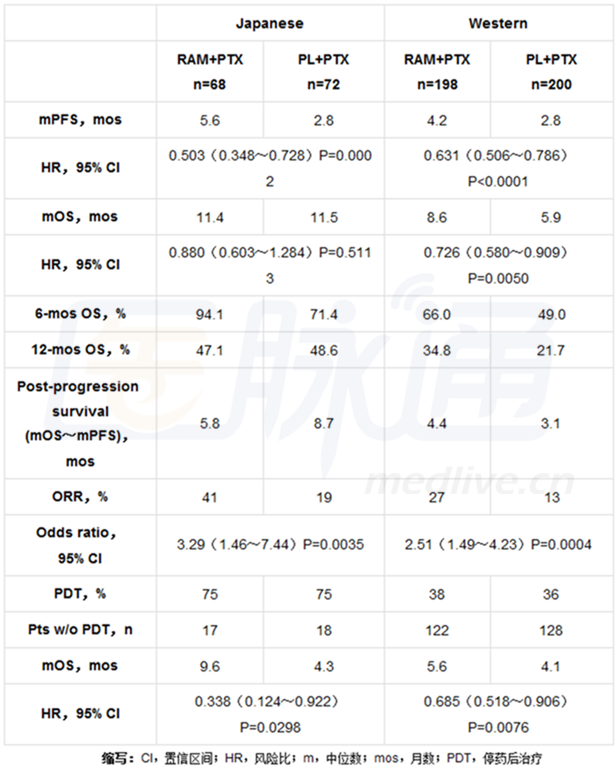
研究人员发现,在日本人群中,可以观察到无进展生存期,客观缓解率,以及6个月总存活率均获益,这与西方人群是一致的。日本患者进展后生存期延长可能是由于停药后处理(PDT)的较高使用,或许掩盖了潜在的总生存期获益。
Ramucirumab联用紫杉醇组的常见不良反应包括疲劳/无力,中性粒细胞减少,腹泻及鼻衄,该组患者出现的严重不良反应包括中性粒细胞减少,发热性中性粒细胞减少。(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发