解读《CVD合并糖尿病口服降糖药物应用专家共识》
| 导读 | 我国是糖尿病和心血管疾病(CVD)的高发国家。2型糖尿病(T2DM)和冠心病(CHD)、高血压可互为因果,共同导致心血管事件,加重肾功能不全。由此,《CVD合并糖尿病口服降糖药物(OAD)应用专家共识》(以下简称“共识”)应运而生。 |
我国是糖尿病和心血管疾病(CVD)的高发国家。2型糖尿病(T2DM)和冠心病(CHD)、高血压可互为因果,共同导致心血管事件,加重肾功能不全。由此,《CVD合并糖尿病口服降糖药物(OAD)应用专家共识》(以下简称“共识”)应运而生,共识深入浅出、简明扼要、实用性强,不仅推荐了CVD合并糖尿病患者的筛查流程、诊断标准、用药原则和治疗目标,还对糖尿病合并CHD、糖尿病合并高血压伴肾功能不全的患者提出了具体的治疗建议。
识别CVD患者中的糖尿病高危人群
2013年国际糖尿病联盟发布的第6版“糖尿病地图”显示,我国糖尿病患病人数为9840万,居全球首位。同年《美国医学会杂志》(JAMA)发表的中国成年人糖尿病患病率调查表明,我国成年人糖尿病患病率为11.6%,高于全球水平(8.3%),而糖尿病前期的患病率已高达50.1%。CVD与糖尿病关系密切,2006年的中国心脏调查发现,CVD住院患者中,约80%存在不同程度的糖代谢异常,其中糖尿病占52.9%,糖尿病前期占26.4%。
糖尿病可显著增加CVD风险,荟萃分析表明,糖化血红蛋白(HbA1c)>5%的患者,HbA1c每增加1%,心血管事件风险增加21%。英国前瞻性糖尿病研究(UKPDS)提示,早期严格血糖控制对降低大血管并发症非常重要。因此,应当有针对性地筛查CVD患者中的糖尿病高危人群,尽早实现其血糖达标。
共识建议,成人具有下列任何一个及以上危险因素,可被定义为糖尿病高危人群,应进行糖尿病筛查:有糖调节受损史,年龄≥40岁,超重(BMI≥24kg/m2)或肥胖(BMI≥28kg/m2)和(或)向心性肥胖(男性腰围≥90cm,女性腰围≥85cm),T2DM患者的一级亲属,高血压(血压≥140/90mmHg)或正在接受降压治疗,血脂异常或正接受调脂治疗,动脉粥样硬化性心脑血管疾病患者及其他因素等。筛查措施包括空腹静脉血浆血糖(FPG)、口服葡萄糖耐量试验(OGTT)和HbA1c检测等。
个体化用药实现CVD合并糖尿病患者血糖达标
对于CVD合并糖尿病患者,共识指出,应当综合循证医学证据,充分平衡风险和血管获益,结合患者的年龄、糖尿病病程以及CVD病史等,将血糖控制目标个体化。
共识建议,糖尿病血糖控制可根据自我血糖监测(SMBG)的结果和HbA1c综合判断。血糖控制目标为:HbA1c<7.0%,FPG<7.0mmol/L,餐后2小时血糖(2hPG)<10mmol/L;糖尿病病史较短、预期寿命较长、无并发症的患者,在不发生低血糖的情况下可考虑将HbA1c控制至<6.5%,否则可放宽血糖目标值至HbA1c<7.5%~8.0%;慢性疾病终末期患者的HbA1c可放宽至<8.5%。
共识列出了目前常见的心内科临床应用的各种OAD:包括双胍类、磺脲类胰岛素促泌剂、格列奈类胰岛素促泌剂、α-糖苷酶抑制剂、二肽基肽酶-4(DPP-4)抑制剂和噻唑烷二酮类等。UKPDS显示,二甲双胍可减少超重或肥胖T2DM患者的心血管事件和死亡。共识建议,若无禁忌且能耐受,二甲双胍是T2DM患者的基础用药。但二甲双胍禁用于肾功能不全[血肌酐水平男性>1.5mg/dl(132.6μmol/L),女性>1.4mg/dl(123.8μmol/L);或肾小球滤过率<45ml/(min?1.73m2)]、肝功能不全、严重感染、缺氧或接受大手术的患者。若存在二甲双胍禁忌或不能耐受,可考虑应用胰岛素促泌剂或α-糖苷酶抑制剂。
除一线用药外,共识还推荐了联合用药方案。指出如果起始HbA1c≥9%或生活方式干预联合一线OAD单药治疗3个月不能使血糖达标,需联合OAD治疗;若两种OAD联合治疗3个月不能使患者血糖达标,可考虑联合第3种OAD,或者联合胰岛素或胰高糖素样肽-1(GLP-1)受体激动剂治疗。共识强调,选择联合用药方案应根据患者的情况。欧洲心脏病学会(ESC)/欧洲糖尿病研究学会(EASD)糖尿病、糖尿病前期和心血管疾病指南也指出,应根据糖代谢异常的特点选择降糖药物。
我国新诊断CHD合并糖尿病患者约97%存在餐后高血糖。与空腹血糖相比,餐后高血糖与心血管死亡的关系更加密切。共识建议,以餐后血糖升高为主者,可优先选用格列奈类降糖药、α-糖苷酶抑制剂或DPP-4抑制剂。因此,应用二甲双胍联合格列奈类以干预空腹+餐后血糖,能获得更佳的HbA1c降低,进而获得降低大/微血管病变等临床获益。
高血压合并糖尿病的降糖药物选择
我国医院门诊高血压患者中糖尿病患病率为24.3%。中华医学会糖尿病学分会慢性并发症调查组报告,1991-2000年部分三甲医院的住院T2DM患者中合并高血压者占34.2%,合并其他CVD者占17.1%。高血压和糖尿病患者均是慢性肾脏疾病(CKD)的高发人群,高血压和糖尿病也是终末期肾病(ESRD)最常见的两大病因。一方面,由于糖尿病患者的代谢紊乱、血流动力学改变等多种因素可导致糖尿病肾病(DN)发生;另一方面,由于糖尿病患者存在胰岛素抵抗和糖脂代谢紊乱,导致内皮功能受损,进一步造成小动脉硬化,最终可导致高血压。由此可见,糖尿病、高血压和CKD三者在病理生理机制上是密切相关的,应对高血压合并糖尿病患者实施早期监测和干预,尽早避免三者之间的恶性循环。
在糖尿病监测方面,2013年欧洲高血压学会(ESH)/ESC动脉高血压管理指南、2014年美国糖尿病学会(ADA)指南、中国2型糖尿病防治指南(2013年版)和中国高血压防治指南(2010年版)均建议动态监测高血压和糖尿病患者的肾功能,包括血清肌酐浓度、尿蛋白排泄率和估计肾小球滤过率(eGFR)。
有效控制血糖,兼顾肾脏安全性是高血压合并糖尿病患者的治疗需求。日本一项研究表明,严格血糖控制使T2DM患者的CKD风险降低70%;UKPDS显示,严格血糖控制使T2DM患者蛋白尿降低34%;君(Jun M)等的研究表明,糖尿病患者血糖控制不佳会导致微血管及大血管病变及不良预后,无论对于1型糖尿病(T1DM)还是T2DM,严格控制血糖,均可推迟或减缓DN的发展。另一方面,血糖控制必须兼顾有效性和安全性。首先,肾功能不全患者因存在肾糖异生作用减弱、药物清除率降低和胰岛素半衰期延长等情况,导致其低血糖的发生风险增加,急性低血糖可减少约22%的肾血流,进一步加重肾功能不全;其次,高血压合并糖尿病患者宜优先选择从肾排泄较少的降糖药,以减小对肾功能的影响。
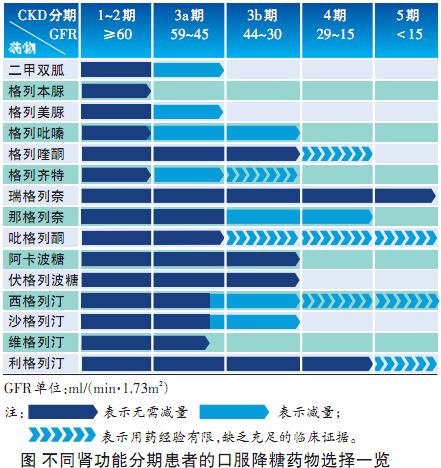
因此,共识指出,CKD患者应基于药物的药代动力学特征及患者肾功能水平综合判断,选择合适的降糖药物并调整剂量,确保在有效降糖的同时不增加低血糖风险。与磺脲类和双胍类等药物相比,瑞格列奈在体内快速起效和代谢,半衰期不受肾功能影响,可发挥血糖依赖性降糖作用模拟生理胰岛素分泌,在避免低血糖方面具有优势;瑞格列奈较少经肾脏途径排泄(<8%),体内代谢在正常人群和CKD患者间无明显差异;瑞格列奈可恢复早相胰岛素分泌,共识推荐优先用于餐后血糖升高患者。因此,共识指出瑞格列奈在肾功能不全时无需调整剂量,可用于GFR低于60ml/(min?1.73m2)(CKD1~5期)的高血压合并糖尿病患者(图)。
小 结
纵览共识,CVD合并糖尿病的规范、安全和个体化治疗跃然纸上。共识不仅为临床医师提供了处置CVD合并糖尿病的基本原则,还始终强调了糖尿病治疗的目的要兼顾心血管获益和用药安全。CVD合并糖尿病治疗应以二甲双胍为基础,必要时联合用药。高血压合并糖尿病患者可应用瑞格列奈等药物以有效控制血糖,最大程度减少低血糖事件和对肾功能的影响。(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发