基因技术阻断遗传性乳腺癌发病
| 导读 | 现代医学研究表明,乳腺癌家族史是乳腺癌发病风险因素的重要预测因子,危险度与血缘关系的亲密程度、家系中患病人数等有关。对于家族遗传性乳腺癌病人,若能尽早预防其后代发病,则可以大大降低家族遗传性乳腺癌的发病。 |

现代医学研究表明,乳腺癌家族史是乳腺癌发病风险因素的重要预测因子,危险度与血缘关系的亲密程度、家系中患病人数等有关。对于家族遗传性乳腺癌病人,若能尽早预防其后代发病,则可以大大降低家族遗传性乳腺癌的发病。
2015年起,国妇婴掌上医院开始对乳腺癌致病相关基因序列进行检测,通过高通量测序平台分析确定病因,并利用植入前胚胎遗传学诊断(PGD技术)帮助乳腺癌家族从胚胎源头开始阻断发病。
1、遗传性乳腺癌大约占所有乳腺癌的5%~10%。
乳腺癌是女性最常见的恶性肿瘤之一,在中国,每年超过160万人诊断为癌症,120万人因癌症而死亡。近年来,乳腺癌在我国的发病率逐年上升,发病年龄亦趋于年轻化。在乳腺癌人群中,遗传性乳腺癌占5%~10%。
影响乳腺癌发病的因素很多,其中家族遗传因素占有重要的地位。1866年第一次报道了乳腺癌家族,此后很多具有明显的乳腺癌易感遗传倾向的家族谱系得到报道。家系中有三个或三个以上个体患乳腺癌则被称为“乳腺癌家族”。
家族性乳腺癌在临床表现上具有发病早、双侧乳腺癌、多中心病灶等特点,同时具有家族聚集性,常染色体显性遗传。如果一直系亲属患病,那么发病风险比正常女性增加2倍。
2、遗传性乳腺癌相关基因。
与遗传性乳腺癌相关的基因包括:BRCA1、BRCA2、P53、PTEN、CHEK2、ATM、NBS1、RAD50、BRIP1和PALB2等。BRCA1、BRCA2基因突变在家族遗传性乳腺癌患者中占有很大的比例。
在遗传性乳腺癌患者中40%~45%存在BRCA1/2突变,而在乳腺癌和卵巢癌高发家族中80%的患者存在BRCA 1/2基因突变。BRCA1突变携带者一生患乳腺癌的几率大于80%,患卵巢癌的几率也达54%;BRCA2突变携带者一生发生乳腺癌的和卵巢癌的机率分别为45%和11%。
3、遗传性乳腺癌可通过基因检测明确携带的致病基因。
有家族遗传背景的患者,只需抽取10ml血液标本,采用高通量测序平台,即可对乳腺癌致病相关基因序列进行全面检测。自去年开始,我院乳腺科对近30例家族遗传倾向乳腺癌患者进行了乳腺癌相关致病基因检测,突变率为50%,其中已知致病突变为16.67%,疑似致病突变为5.56%,意义未明突变为27.78%。
采用这种高通量测序平台基因检测方法,DNA片段的每个核苷酸位置都将被多次读取,能够准确鉴定出任何核苷酸位置的序列信息差异(甚至是极低频率的变异)。因此,灵敏度极高,是遗传性乳腺癌患者明确携带致病基因的灵敏、高效、且准确的检测方法。该基因检测技术具体流程见图1。
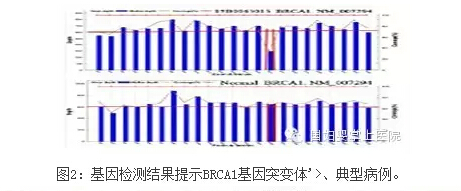
患者,女,27岁,发现左乳肿块2个月,入院手术病理诊断为乳腺癌。患者有家族史:姨妈患乳腺癌,爷爷患肺癌。对该患者血液进行乳腺癌相关致病基因检测结果如图2、3。结果表明:患者存在BRCA1和BRIP1基因突变,BRCA1是已经被证实了的致病性突变。此次检测对阻断该家族乳腺癌下行传播后代具有重要的意义。

胚胎植入前遗传学诊断(PGD)是从胚胎源头上阻断遗传缺陷下传的一种治疗手段,始于上世纪90年代,首先应用在性染色体连锁单基因遗传病的治疗。现在,更多新技术已在临床上推广应用,PGD技术除了应用于50余种单基因遗传病的遗传阻断外,也进一步应用于肿瘤易感性的检测、HLA配对等,染色体疾病的PGD诊断也已经从少数几条染色体的诊断扩大到利用基因芯片的方法对全部23对条染色体或全基因组筛查,并扩展到用于不孕不育反复治疗失败或反复流产的治疗。
最近,我院在此前成功通过全部染色体异常筛查产下健康宝宝的基础上,成功通过PGD完成了10余例基因遗传病的诊断,包括成人型多囊肾病、成骨不全、多发性内分泌肿瘤综合征、粘多糖贮积症、嗜血细胞综合征、脊髓性肌萎缩、进行性肌营养不良、ADA缺陷性重症联合免疫缺陷症、WAS综合征(中性粒细胞减少症)、肝豆状核变性等单基因遗传病的诊断。
针对遗传性乳腺癌的发病,可以通过PGD技术选取未携带乳腺癌致病基因的健康胚胎移植入子宫,以此来减少因携带遗传性乳腺癌致病基因所致的家族遗传性乳腺癌的下行传播。此外,植入前遗传学诊断由于完成于胚胎形成前,因此亦不涉及相应伦理问题。
我院目前已建立出生缺陷防控体系,全面解答病人疑问并给出治疗方案。如果有家族遗传病背景,可在生殖遗传门诊咨询,即使本人没有表征,也需要确认遗传信息,对家族进行基因筛查,这样可以从根本上阻断遗传病下行传播。
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发