肺癌手术前进行免疫治疗,或可形成终生肿瘤免疫记忆!
| 导读 | 可是术前以铂类为基础的化疗仅仅将生存率提高了5.4个百分点,然而多于60%的患者会出现3级以上严重副作用.术前的免疫治疗是一... |
晚期肺癌难以治愈,而那些I期到IIIA期的早期肺癌同样缺乏有效治疗手段。而手术是治疗这些早期肺癌患者的标准治疗方案。
据统计,手术以后大部分患者的肿瘤还是会复发,5年生存率IIIA期只有20%,而被认为非常早期的I A期肺癌也只有50%的术后5年生存率。针对这一困境,医学科学家们引入术前化疗来配合手术,用以降低术后的复发。
可是术前以铂类为基础的化疗仅仅将生存率提高了5.4个百分点,然而多于60%的患者会出现3级以上严重副作用。
术前的免疫治疗是一个非常吸引医生和学者的话题,因为我们认为肿瘤本身作为一个肿瘤抗原库,如果可以通过免疫治疗去激活患者身体里的免疫系统去识别这些肿瘤抗原并形成免疫记忆,才真正能够使免疫系统在手术切除肿瘤以后依然发挥监视新的肿瘤细胞的出现并将其消灭的作用。
反过来,如果将肿瘤直接切除而不做术前免疫激活,则将会失去这个将肿瘤本身“变害为利”形成终身肿瘤抗原免疫记忆的机会。
此前这种效应已经在小鼠身上观察到,而这次,美国的医学科学家们将这个结论在人体上印证了,并且将试验的结果发表在了4月16号最新刊出的《新英格兰医学》上。
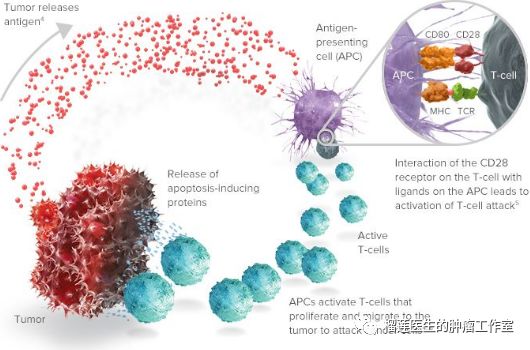
(图示为红色的肿瘤细胞在被PD-1抗体激活的T细胞[蓝色]攻击后释放出肿瘤抗原[红色的小颗粒],这些肿瘤抗原被抗原提呈细胞[紫色]捕获以后用来教育其他的T细胞去识别这些肿瘤抗原并去捕杀带有这些肿瘤抗原的癌细胞)
具体的做法是:21名早期(I,II或IIIA期)非小细胞肺癌患者,术前使用3mg/kg的Nivolumab(即我们平时说的PD-1 抗体O药)每2周一次,共使用2次。手术安排在第一次O药注射的4周后(其中有1名患者因为O药使用后发生了严重的肺炎而只用了1次O药)。最后患者均在O药结束后的18天左右(11天到29天)进行了手术,可见O药的使用并没有对手术的计划造成延迟。
21名患者中,有20人手术完全切除了肿瘤,1名IIIA期患者术中发现肿瘤侵犯气管而无法完整切除肿瘤。
-
2次O药之后的术前影像学检查发现,2名患者出现了部分缓解/肿瘤缩小,18名患者疾病稳定不进展,1名患者出现了疾病进展。
-
而术后的病理检查发现,这20个完全切除的肿瘤有9个达到了病理学上的治疗有效。其中3名患者达到了病理完全缓解,在显微镜下找不到肿瘤细胞了!
而且这些治疗有效的患者既有PD-L1阳性表达的,也有PD-L1阴性表达的。病理有效与术前肿瘤突变负荷TMB具有极大的相关性。在接下来长达约1年的随访中发现,16人(80%)依然无瘤生存,没有肿瘤复发;18个月疾病无复发率为75%。
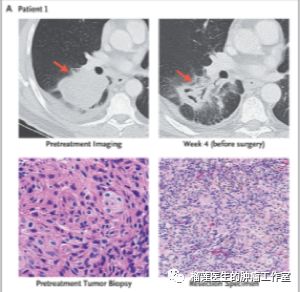
图为一位62岁男性吸烟者,治疗前(左)诊断为IIB期肺鳞癌,肿瘤直径8厘米。术后病理(右下)显示肿瘤完全缓解。
3人出现了疾病进展。这3名患者都各自是什么情况呢?
-
第一位患者术后病理显示依然有75%的肿瘤残余,在术后2个月发生了脑转移。之后医生予以立体定向放疗,这名患者在16个月后依然没有复发。
-
第二名患者是术后病理显示有5%的肿瘤残余,术后出现了纵隔淋巴结的复发,在给予化疗和放疗以后,这名患者在12个月后依然没有疾病再进展。
-
第三名患者术后病理发现有80%的肿瘤残余,在手术一年以后发生了远端器官转移,并在肺部肿瘤复发后的4个月去世。
在9名治疗前后提供血液标本的患者中,发现有8人的外周血中和肿瘤中均出现了抗肿瘤的特异性杀伤T细胞。研究者还发现一些与肿瘤突变相关的专门针对肿瘤新生抗原的T细胞在外周血中大量扩增。而这些T细胞中,有一些是在抗PD-1治疗前没有出现的。
我们认为这些T细胞将成为具有记忆性的专门攻击肿瘤突变和新生抗原的免疫卫士,就如我们儿时接种疫苗一样,这些T细胞将使这些患者今后在相当长的一段时间内再不会有肿瘤发生。
在其他癌种如三阴性乳腺癌,头颈鳞癌,膀胱癌,黑色素瘤和肾癌中也在开展同样的III期临床试验。在不久后会有更多证据更足的数据为我们展示出来。

References:
Ford P, Chaft J, Smith K, et al. Neoadjuvant PD-1 Blockade in Resectable Lung Cancer. N Engl J Med 2018;DOI: 10.1056/NEJMoa1716078
Goldstraw P, Crowley J, Chansky K, et al. The IASLC Lung Cancer Staging Project: proposals for the revision of the TNM stage groupings in the forthcoming (seventh) edition of the TNM Classification of malignant tumours. J Thorac Oncol 2007;2:706-714.
Pignon JP, Tribodet H, Scagliotti GV, et al. Lung adjuvant cisplatin evaluation: a pooled analysis by the LACE Collaborative Group. J Clin Oncol 2008;26:3552-3559.
Wakelee HA, Dahlberg SE, Keller SM, et al. Adjuvant chemotherapy with or without bevacizumab in patients with resected non-small-cell lung cancer (E1505): an open-label, multicentre, randomized, phase 3 trial.Lancet Oncol 2017;18:1610-1623.
Liu J, Blake SJ, Yong MC, et al. Improved efficacy of neoadjuvant compared to adjuvant immunotherapy to eradicate metastatic disease.Cancer Discov 2016;6:1382-1399.
www.clinicaltrials.gov/NCT03036488, NCT02998528, NCT02519322, NCT02296684, NCT02845323, and NCT02575222
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发