JCI重磅!溶瘤病毒治疗肿瘤的耐药机制被发现!居然是PD-L1!成也它败也它~
| 导读 | 近日,J Clin Invest杂志在线发表的一篇名为“PD-L1 in tumor microenvironment mediates resistance to oncolytic immunotherapy”的文章,该文章指出,肿瘤微环境中的PD-L1介导了对溶瘤性免疫疗法的抗性,诠释了溶瘤病毒疗法的耐药性产生的机制,为进一步优化溶瘤病毒疗法提供了方向。同期,J Clin Invest杂志刊出了一篇名为“Unleashing the therapeutic potentialof oncolytic viruses”的特约评论,对该研究做出了高度的评价!
|

近日,J Clin Invest杂志在线发表的一篇名为“PD-L1 in tumor microenvironment mediates resistance to oncolytic immunotherapy”的文章,该文章指出,肿瘤微环境中的PD-L1介导了对溶瘤性免疫疗法的抗性,诠释了溶瘤病毒疗法的耐药性产生的机制,为进一步优化溶瘤病毒疗法提供了方向。同期,J Clin Invest杂志刊出了一篇名为“Unleashing the therapeutic potentialof oncolytic viruses”的特约评论,对该研究做出了高度的评价!
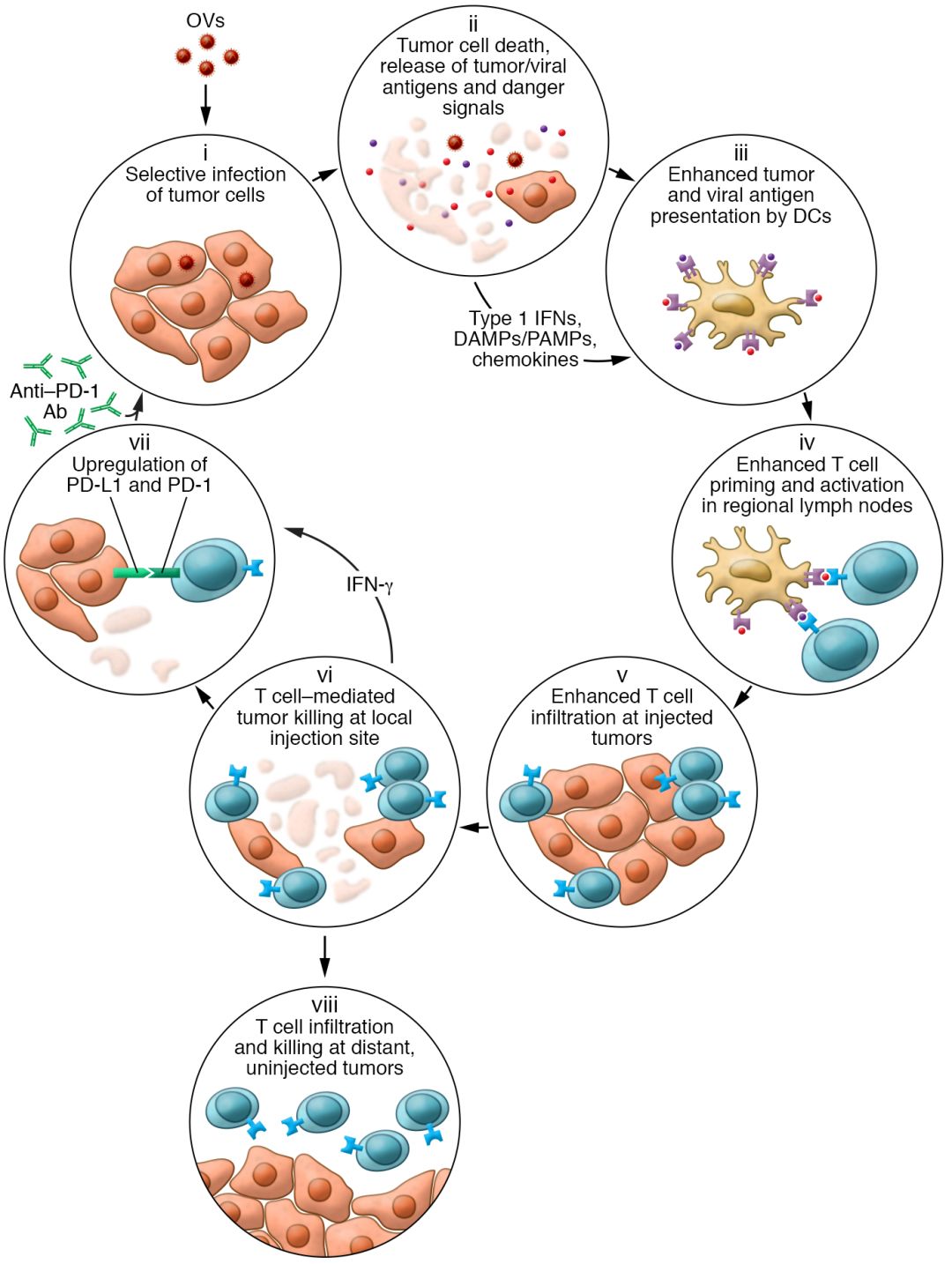
溶瘤病毒(Oncolytic virus)源于天然或基因修饰或改造的一类病毒,是一种多功能的新型治疗药物。溶瘤病毒在肿瘤细胞进行复制和增殖,释放出新的感染性病毒颗粒感染和破坏其他肿瘤细胞,或者表达对肿瘤细胞具有效应作用的蛋白影响肿瘤微环境、刺激宿主产生抗肿瘤免疫反应或者直接溶解肿瘤。但是,迄今为止,对大多数溶瘤病毒(Oncolytic virus)的潜在作用机制以及产生耐药性机制(先天性或者活动性耐药机制)的了解很是有限。

Zamarin等人从病人体内获得肿瘤组织(RCC, CRC, breast cancer, and HNSCC tumor specimens)并进行肿瘤外植体实验,并用新城疫溶瘤病毒(NDV)对其进行治疗,病毒注射24H后,收取组织样本进行RT-PCR检测分析。结果显示,感染NDV后许多免疫相关基因表达量被上调,包括I型IFN相关转录物和编码范围的转录物趋化因子等。
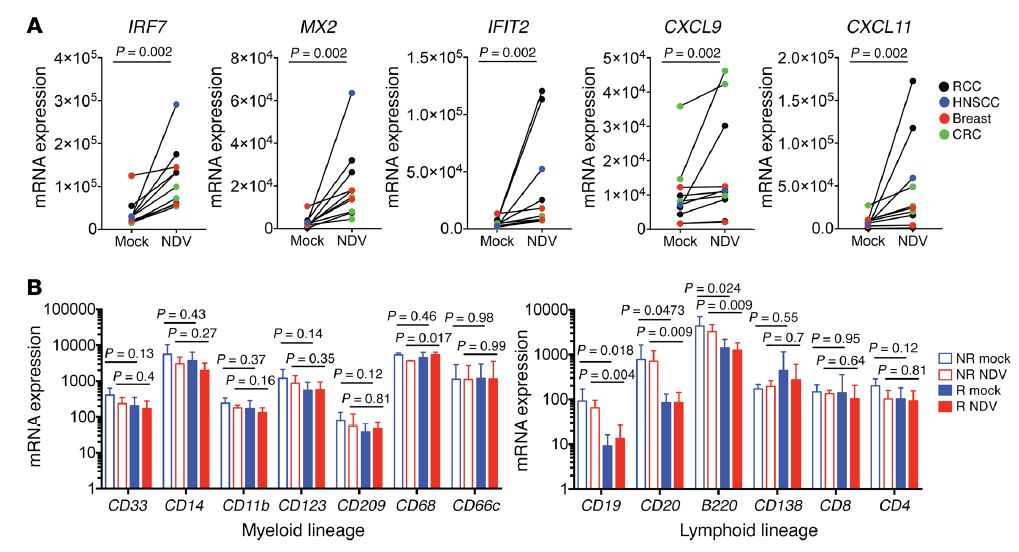
除此以外,研究者还对远端的非注射位的肿瘤进行分析,结果发现,远端的未注射新城疫溶瘤病毒(NDV)的肿瘤也有淋巴细胞的浸润,但NDV对远端肿瘤的抑制效率,不如原位注射的肿瘤。也即,在对肿瘤内注射NDV后,引起了全身性的免疫应答,激活了机体的抗肿瘤免疫,引起了肿瘤组织内的免疫淋巴细胞的浸润。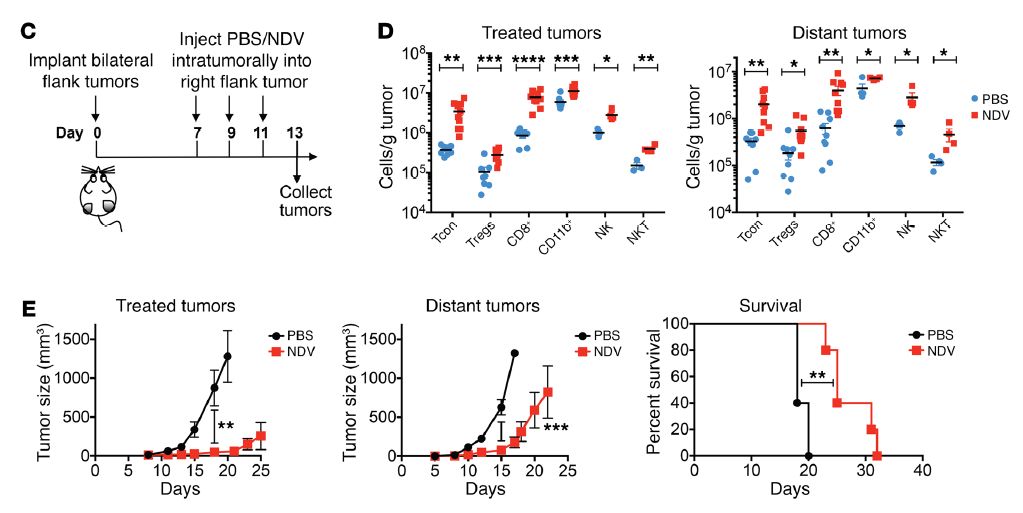
那么,这种免疫应答反应的产生机制是什么?是什么抑制了远端肿瘤组织内的免疫淋巴细胞发挥其杀伤性作用呢?研究者继续对两组的样本进行比较分析,并将研究重点放在了PD-1/PD-L1信号通路上,研究分析认为,NDV接种肿瘤细胞后,引起IFN的释放并促进了远端肿瘤的内PD-L1的表达,抑制了浸润的淋巴细胞发挥其杀伤作用。
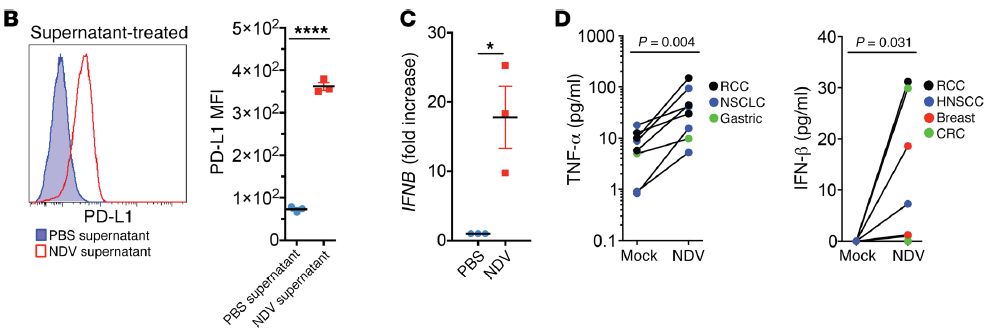
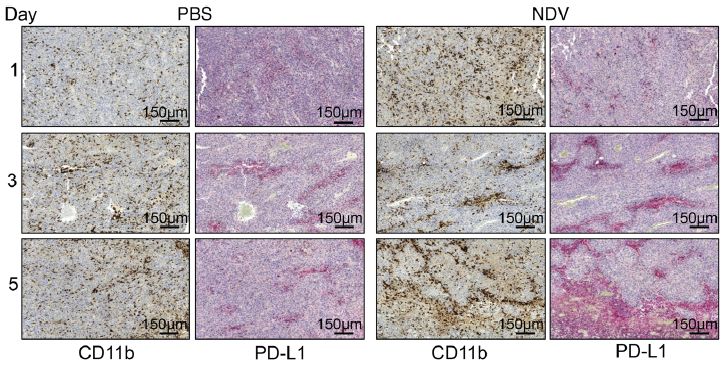
研究者分析认为,PD-L1可能是引起肿瘤对溶瘤病毒治疗(NDV)产生耐药性的一个重要因素。因此,设计实验,通过联合使用PD-1/PD-L1抑制剂和溶瘤新城疫病毒(NDV)对肿瘤进行治疗,结果显示,联合用药可以实现对肿瘤的高效杀伤。
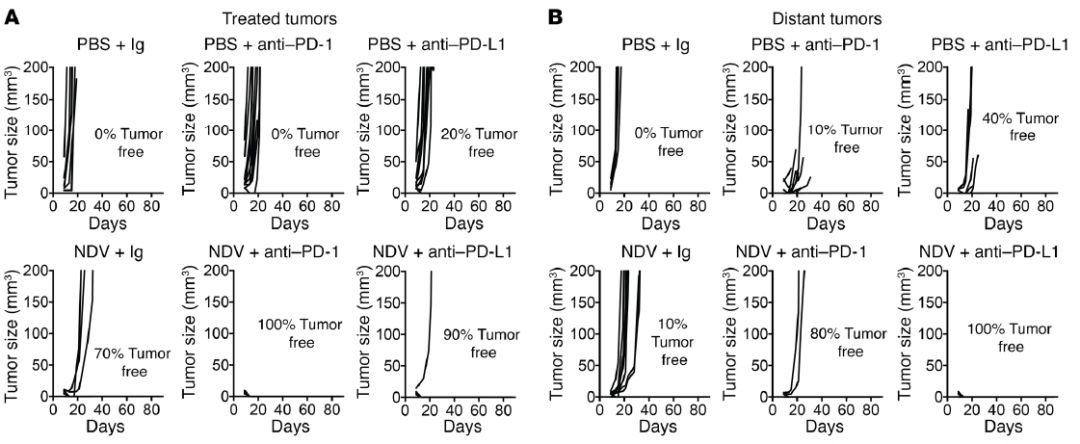

综上,溶瘤病毒(NDV)可以引起全身性的免疫应答,激活机体的抗肿瘤免疫。肿瘤微环境中的PD-L1介导了对溶瘤病毒免疫疗法的抗性,诠释了溶瘤病毒疗法的耐药性产生的机制,这也为近来的免疫抑制剂和溶瘤病毒的联合用药能显著提高治疗效果提供了理论依据,为进一步完善溶瘤病毒的设计及治疗,以及临床联合用药提供了方向。
溶瘤病毒
是一类具有复制能力的肿瘤杀伤型病毒,世界上最早出现溶瘤病毒的报道,是由于当时发现一名子宫颈癌患者在感染狂犬病病毒后,肿瘤随之消退。
1991年,Martuza等人在《Science》杂志发表文章,称转基因HSV在恶性胶质瘤治疗中有一定的效果以后,采用HSV进行的溶瘤病毒治疗就日益受到关注。其原理是通过对自然界存在的一些致病力较弱的病毒进行基因改造制成特殊的溶瘤病毒,利用靶细胞中抑癌基因的失活或缺陷从而选择性地感染肿瘤细胞,在其内大量复制并最终摧毁肿瘤细胞。同时它还能激发免疫反应,吸引更多免疫细胞来继续杀死残余癌细胞。近几十年来,溶瘤病毒治疗引起了广泛关注,相关研究取得了巨大进展。
新城疫病毒(newcastle disease virus,NDV)、单纯疱疹病毒-1(herpes simplex virus-1,HSV-1)、呼肠孤病毒(reovirus)、溶瘤腺病毒(oncolytic adenovirus)等是由嗜肿瘤特性而被用来改造成溶瘤病毒,它特异性识别并感染肿瘤细胞,最终导致细胞溶胀而摧毁肿瘤细胞,但无法在正常机体细胞内复制而不具有杀伤作用,理论上具有更高的抗肿瘤效应和更低的副作用。
目前研究最深入的溶瘤病毒包括腺病毒和I型单纯疱疹病毒(herpes simplex virus, HSV)等,自从Martuza等1991年在《Science》杂志称转基因HSV在恶性胶质瘤治疗中有一定的效果以后,采用HSV进行的溶瘤病毒治疗就日益受到关注,目前这种治疗已经进入临床试验阶段。
溶瘤病毒通过细胞表面分子入侵到肿瘤细胞中,因而溶瘤病毒治疗的有效策略之一就是要改造出具有特异性的溶瘤病毒,再以那些在肿瘤细胞中过度表达的特异性受体为靶向,将病毒入侵到肿瘤细胞中并行使后续的各项功能。人表皮生长因子受体-2(human epidermal growth factor receptor -2,HER-2)就是这样一个特异性的受体,它在1/4的乳腺癌和卵巢癌患者中过度表达。美国每年新增20万例乳腺癌及卵巢癌患者,因此如果能够成功进行溶瘤病毒治疗,将造福于这些患者和他们的家庭。
美国俄亥俄州立大学的研究人员开发出一种全新的肿瘤攻击病毒(tumor-attacking virus),不但能够杀死大脑内的肿瘤细胞,还能够阻断肿瘤内血管的生长。该研究表明,这种能够杀死肿瘤的溶瘤病毒(oncolytic viruses)如果携带能够抑制血管生长的蛋白vasculostatin,那么或许能够更有效的治疗侵润性脑部肿瘤。这项研究发表在Molecular Therapy杂志网络版上。
意大利博洛尼亚大学的Laura Menottia等研究者开展了一项研究,尝试将改造后的HSV用于HER-2阳性肿瘤的溶瘤病毒治疗。研究者通过生物医学工程的方法,采用抗HER-2单链抗体替代了HSV受体结合糖化蛋白中的免疫球蛋白折叠核心,如此将HSV进行改造后,这种重组体就可以特异性地进入HER-2阳性癌症细胞,起到溶瘤治疗的效果。由于特异性非常强,这种重组体在采用腹腔注射治疗的小鼠试验中,安全性数据非常好,半数致死量(LD50 )大于5 ×108 pfu。将这种重组体对负荷人类HER-2阳性癌症的裸鼠进行瘤内注射后,癌症细胞的生长受到了强烈的抑制。
该研究提示,经过改造的HSV重组体可以对HER-2阳性的肿瘤进行溶瘤病毒治疗,特异性强且安全性好.。
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发