爱眼日 | 基因治疗能够让失明患者重见光明
| 导读 | 当一个又一个不治之症在基因治疗领域得到诊断和治疗,我们有理由相信基因治疗的明天值得期待。 |
Luxturna--首款矫正基因缺陷的药物,针对由RPE65基因突变导致的雷柏氏先天性黑朦2型RPE65基因突变引起的失明患者治疗,于去年12月获FDA批准上市。
它的出现点燃了基因治疗热火,对于在基因科研领域钻研的科学家更是一剂强心针。Luxturna在临床上的成功应用,令基因疗法将逐步成为治疗常见遗传性疾病的主流手段。
一份光明大礼
雷柏氏先天性黑朦(LCA),这是一种导致婴幼儿先天性盲的严重遗传性视网膜疾病。患者的视功能损伤往往在出生后前几个月就开始出现,表现为患儿双眼不追物,还可以出现特征性的压眼现象,如戳眼、揉眼、按压眼球等。稍大可见严重视觉障碍引起的眼球异常转动(眼球震颤),传统的方法难以治愈雷柏氏先天性黑朦(LCA),使得患者终身生活在漆黑里。
目前超70%的LCA临床诊断患者可通过基因检测明确致病基因。基因检测已经鉴定出25种LCA相关致病基因,RPE65就是常见的致病基因之一,临床上定为亚型2(LCA2)。
在人体内,RPE65基因编码了对正常视力起重要作用的一种酶。因为基因突变引起的RPE65酶水平下降或缺失会导致患者视网膜不能合成感光物质,进而导致严重的夜盲和视力障碍。
Luxturna是利用腺相关病毒技术,将健康的RPE65基因直接引入到视网膜相关细胞中,让它们产生正常的RPE65酶,恢复患者的感光物质和视力。对于由RPE65基因突变导致的雷柏氏先天性黑朦2型(LCA2)导致的严重视力障碍有着“治本”的疗效。
FDA批准的首次治疗案例
美国马萨诸塞州的遗传性视网膜疾病服务的副主任杰森·康芒德博士于3月完成了首次治疗案例,患者是一位来自新泽西州的13岁男孩。这是FAD批准的基因疗法第一次用于遗传性疾病,标志着医学新时代里程碑式的开始。
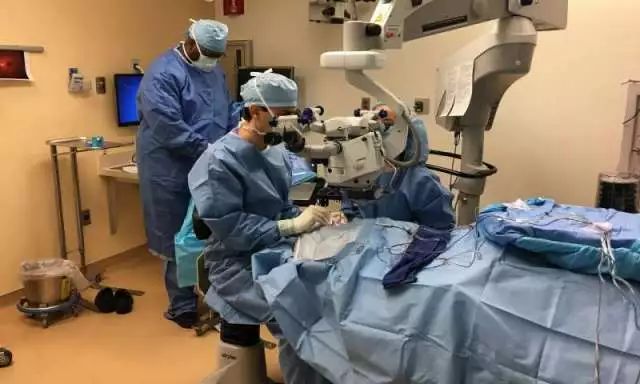
Jason Comander, M.D
Luxturna,由Spark Therapeutics公司研发,12月获得美国食品和药物管理局(FDA)的批准,治疗年龄在12个月以上的患者。
新批准的治疗方法是将一种经过改良的病毒注入患者的眼睛,以纠正RPE65基因突变导致的缺陷。医生们用一种无害的病毒来携带一种新的RPE65基因,然后进行显微手术,用一根和人类眼睫毛差不多宽的管子,将新基因植入视网膜细胞中。这些突变阻止了视网膜正常运作所需的蛋白质的产生或功能,视网膜是眼球后部的感光组织,能启动视觉。
这种基因治疗方法已经通过不少的案例证明了,替换眼睛中的一种基因可以为以前无法治愈的遗传性失明患者带来希望。并且,在10多年前的早期试验中接受治疗的患者目前仍保持视力。
科学家通过了几十年的努力,将设想的基因疗法运用到了实际的临床中,让患者重见光明。当一个又一个不治之症在基因治疗领域得到诊断和治疗,我们有理由相信基因治疗的明天值得期待。
参考文献:
1.Massachusetts Eye and Ear performs first FDA-approved gene therapy procedure for inherited disease
2.FDA panel mulls gene therapy for kids with rare eye disease (Update)
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发