期待!罕见遗传疾病或将成为基因疗法下一攻破领域!
| 导读 | 全世界估计有超过3.5亿人患有罕见病,目前确定的有约7,000种罕见疾病,其中80%是由遗传变异引起的,约有50%的罕见病在出生时或者儿童期即可发病,30%的罕见病患者会在5岁之前去世,病情常进展迅速,死亡率高。另一方面,除了通过孕前筛查、产前筛查、产前诊断排除的一部分疾病之外,其余罕见病的诊断过程很漫长,平均需 |
全世界估计有超过3.5亿人患有罕见病,目前确定的有约7,000种罕见疾病,其中80%是由遗传变异引起的,约有50%的罕见病在出生时或者儿童期即可发病,30%的罕见病患者会在5岁之前去世,病情常进展迅速,死亡率高。另一方面,除了通过孕前筛查、产前筛查、产前诊断排除的一部分疾病之外,其余罕见病的诊断过程很漫长,平均需要5~8年时间才能确诊,而且目前具有有效治疗方法或药物的罕见病种类不足5%。这无疑给患者及其家庭造成了极大的痛苦。
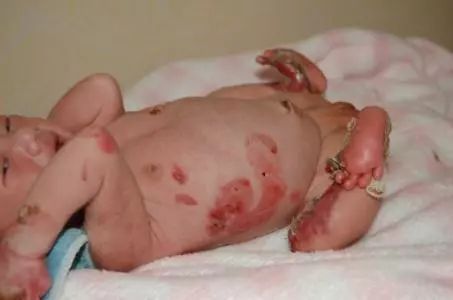
大疱性表皮松解(EB)*图片来源于网络
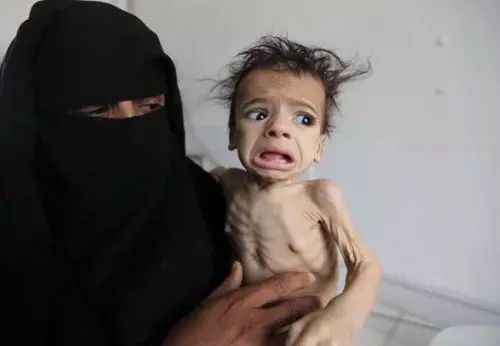
杜氏肌营养不良症(DMD)*图片来源于网络

脊髓性肌萎缩症(SMA)*图片来源于网络
基因疗法概念已经提出30年,即将外源基因通过基因转移技术将其插入病人的适当的受体细胞中,使外源基因制造的产物治疗某种疾病。从广义说,基因治疗还可包括从DNA水平采取的治疗某些疾病的措施和新技术。流程大致为:生产带有目的基因的病毒—从病人体内分离靶细胞—体外转染—把病毒转染的靶细胞回输病人体内四步。

2017年被称为抗癌治疗新纪元,FDA批准了两款癌症基因疗法,一是诺华开发的癌症疗法CAR-T疗法Kymriah,是美国市场上“首款基因疗法”,主要用来治疗儿童和青年所患的白血病和骨癌;二是美国风筝制药公司(Kite Pharma)的Yescarta 基因疗法,首款获批用于治疗特定类型非霍奇金淋巴瘤(non-Hodgkin lymphoma,NHL)的基因疗法。
由于大部分的罕见遗传疾病是有基因突变造成的,那么自然而然的,基因疗法的使用范围除了癌症治疗之外,完全可用于各种罕见遗传疾病的治疗上!近两年,NEJM、Nature上多篇文章揭示基因疗法打破疑难杂症治疗难题,包括血友病、遗传性视网膜病变、脊髓性肌萎缩症等。
2017年3月《新英格兰医学杂志》上一篇论文称,利用基因疗法成功治愈了身患镰状细胞贫血的15岁男孩,而且该疗法在其他7位患者身上也显示出惊人疗效。这是基因疗法首次用于治愈遗传性疾病。同年11月,《Nature》上重磅研究表明,科学家借助于转基因干细胞,成功挽救一名患有罕见皮肤病——大疱性表皮松解(EB)的男孩,使其拥有全新的皮肤。同期,《NEJM》发表头条文章又揭示一项里程碑式的临床结果:AVXS-101基因疗法成功延长了15名身患严重遗传性疾病——1型脊髓性肌萎缩症(SMA1)患儿的生命。(脊髓性肌萎缩症是一类会导致肌肉无力、萎缩的罕见运动神经元性疾病,由运动神经元存活1号基因(SMN1)突变引发)。紧接着,另一项发表在国际杂志Acta Neuropathologica上的研究报告中,称一项新型基因疗法成功治疗名为卡纳万病(海绵状脑白质营养不良症)的罕见致死性的遗传性障碍疾病。
这预示着基因疗法领域的一个里程碑,基因疗法使用范围完全可扩展至癌症治疗之外!FDA对于罕见疾病与基因疗法也极其关注,截至目前,已陆续批准了几款罕见遗传疾病的基因疗法。
2017年11月,FDA提前批准了罗氏药物Hemlibra,用于防止或减少成人和儿童A型血友病患者出血的频率。(A型血友病又名抗血友病球蛋白缺乏症或第Ⅷ因子缺乏症,在遗传性凝血病中占首位,是由于X染色体上的抗血友病球蛋白基因(FⅧ基因)突变引起)。
2017年12月,FDA批准美国火花基因疗法公司的Luxturna基因疗法,用于治疗双等位基因RPE65突变导致的遗传性视网膜病变(IRD)的儿童和成人患者,是首款在美国获批、靶向特定基因突变的“直接给药型”基因疗法。
2018年全球首个RNAi药物获得批准———由生物技术公司Alnylam开发的patisiran,通过干扰细胞内信息的传递以治疗罕见的家族性淀粉样多发性神经病变,该疾病是由TTR基因突变导致的一种可遗传的退行性致命疾病,发病率和死亡率很高,全球约有5万名患者,这些患者的平均寿命为2.5-15年。
6月份,FDA通过了Bioverativ公司的治疗镰状细胞贫血(sickle cell disease)的候选基因编辑细胞疗法(gene-edited cell therapy)BIVV003的新药临床研究(IND)申请。距离最终战胜镰状细胞贫血症仅一步之遥。
近日,美国FDA也已允许Solid Biosciences继续IGNITE DMD临床试验,评估基因疗法SGT-001在杜氏肌营养不良症(DMD)中的治疗效果。SGT-001是Solid Biosciences的领先在研新药,能通过创新AAV9载体,将合成的抗肌萎缩蛋白基因递送至患者体内,治疗杜氏肌营养不良症的遗传根源。它曾获得美国FDA颁发的罕见儿童疾病认定(RPDD)、以及孤儿药资格。
除此之外也还包括上文所说的SMA,作为导致婴儿死亡的头号遗传病因,90%的病儿寿命不足2岁,即便能够存活,也需要终身依赖呼吸机才能生存。而AVXS-101基因疗法的突破无疑为这些患者带来了福音,而且美国FDA已经授予AVXS-101孤儿药资格和突破性疗法认定,相信这款创新基因疗法也有望在今年递交上市申请。
刚刚过去的美国生物技术大会暨展览会(BIO International Convention),美国FDA局长Scott Gottlieb博士也说道,对于罕见遗传疾病,期望到2022年,FDA有望批准达40款基因疗法。对于镰状红细胞病这样的遗传疾病,10年内能看到治愈的希望。除此之外,还指出FDA计划出台一系列指导性文件,指明基因疗法的监管方向与细则。另外,今年3月,我国国内首个全基因组测序临床研究在沪启动,将通过全基因组测序和数据解读明确遗传性疾病的发病机制,筛选鉴定疾病诊断的生物标记物和药物靶点,为更精准的个性化治疗方案提供理论基础和研究数据,从而逐步构建中国儿童遗传疾病检测基因组数据库。
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发