又一次突破 | 张令强、贺福初院士再次出手,提供肿瘤治疗新靶标
| 导读 | 2018年6月25号,军事医学科学院张令强课题组与贺福初课题组合作在Nature Communications上在线发表了题为“Mutually exclusive acetylation and ubiquitylation of the splicing factor SRSF5 control tumor growth”的研究论文。 |
背景介绍
2018年6月25号,军事医学科学院张令强课题组与贺福初课题组合作在Nature Communications上在线发表了题为“Mutually exclusive acetylation and ubiquitylation of the splicing factor SRSF5 control tumor growth”的研究论文。研究人员发现,在葡萄糖摄入时,剪接因子SRSF 5是通过Tip 60介导的K 125乙酰化特异性诱导的,拮抗Smurf 1介导的泛素化。SRSF 5促进CCAR 1的选择性剪接,产生CCAR1S蛋白,通过增加葡萄糖消耗和乙酰辅酶A的产生促进肿瘤的生长。相反,在葡萄糖饥饿时,SRSF 5被HDAC 1去乙酰化,Smurf 1在同一赖氨酸上泛素化,导致SRSF 5的蛋白酶体降解。CCAR1L蛋白积累促进细胞凋亡。重要的是,SRSF 5在人肺癌中是高乙酰化和上调的,这与CCAR1S的表达增加和肿瘤的进展有关。因此,SRSF 5对高糖有促进肿瘤发展的作用,SRSF5-CCAR 1轴可能是肿瘤治疗的重要靶点。

作为基因调控最普遍的机制之一,替代剪接在蛋白质功能的复杂调控中起着至关重要的作用,剪接失调与人的癌变密切相关。AS主要由多个CIS元件来调节,这些CIS元件通过不同的机构将各种拼接因子招募到相邻的拼接位置。值得注意的是,剪接因子可分为两类,丝氨酸/精氨酸(SR)蛋白能以与环境相关的方式促进剪接,而非均质核核糖核蛋白(HnRNPs)可以正向和负调节分裂。SR蛋白由经典的SR-剪接因子(SRSF)和RNA结合的SR-样剪接因子S4组成。迄今为止,所有报道的经典SRSF敲除小鼠显示了早期胚胎致死表型,因此支持SR蛋白在体内的基本作用,并进一步表明,在不同细胞和组织条件下,SRSF的丰度和活性的微调确定剪接结果。
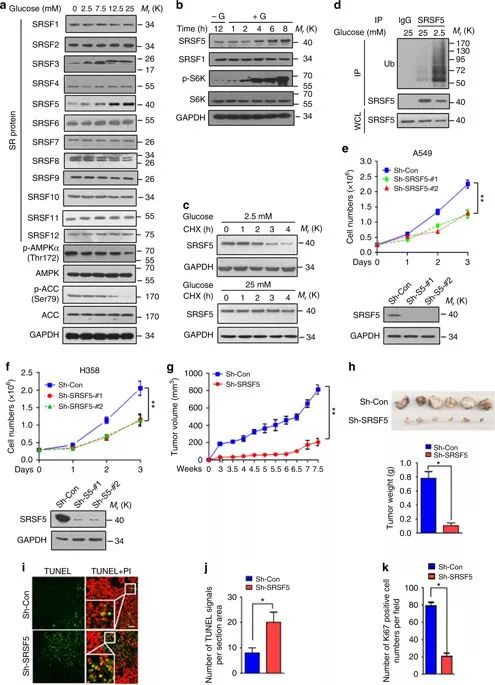
SRSF 5在高糖条件下稳定,促进肿瘤发生
最近的发现表明,SRSFs的失调导致多种类型的人类肿瘤的进展。例如,原癌基因SRSF 1在癌症信号通路的关键枢纽中控制着无数的基因,SRSF 2的功能增益突变有助于骨髓增殖性肿瘤的发展。此外,SRSF 9通过促进β-catenin 的积累被确认为大肠癌的致癌变压器,SRSF 10通过增强抗凋亡异构体BCLAF 1的剪接来促进大肠癌的进展。由于改变剪接可能会带来潜在的癌症风险,特别是针对SRSF的研究将为癌症治疗提供新的见解。
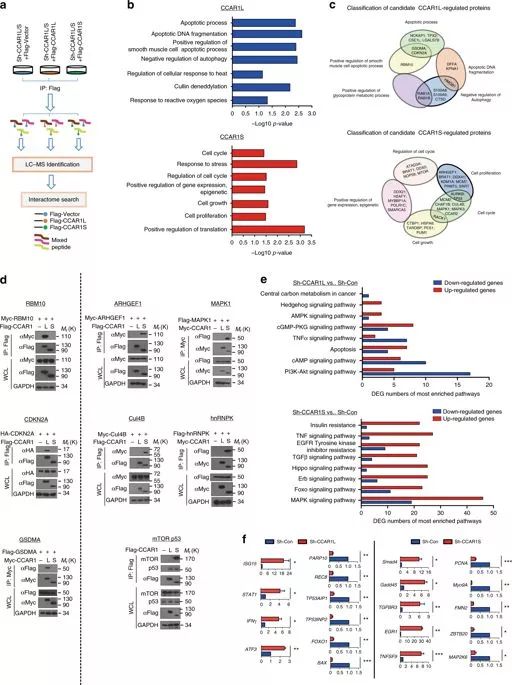
CCAR1L/S相关蛋白的网络分析
细胞代谢失调是肿瘤的标志之一,其中糖酵解途径的升高在促进肿瘤生长中起着引导作用。由于葡萄糖是最重要的营养合成来源,可以作为细胞生长的基石,因此大多数肿瘤细胞比正常细胞摄取更多的葡萄糖,细胞对高糖的反应可能是肿瘤发生的原因之一。经典的SR蛋白目前已被报道调节代谢稳态和能量依赖的发展。然而,剪接因子在糖代谢和肿瘤发展中的作用仍未明确。
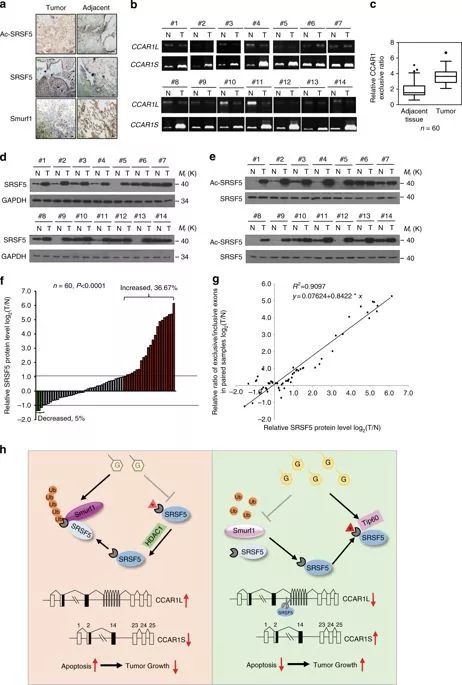
SRSF 5状态与CCAR 1剪接及肿瘤发生相关
在此,研究人员发现,在葡萄糖摄入时,剪接因子SRSF 5是通过Tip 60介导的K 125乙酰化特异性诱导的,拮抗Smurf 1介导的泛素化。SRSF 5促进CCAR 1的选择性剪接,产生CCAR1S蛋白,通过增加葡萄糖消耗和乙酰辅酶A的产生促进肿瘤的生长。相反,在葡萄糖饥饿时,SRSF 5被HDAC 1去乙酰化,Smurf 1在同一赖氨酸上泛素化,导致SRSF 5的蛋白酶体降解。CCAR1L蛋白积累促进细胞凋亡。重要的是,SRSF 5在人肺癌中是高乙酰化和上调的,这与CCAR1S的表达增加和肿瘤的进展有关。因此,SRSF 5对高糖有促进肿瘤发展的作用,SRSF5-CCAR 1轴可能是肿瘤治疗的重要靶点。
原文链接:
https://www.nature.com/articles/s41467-018-04815-3
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发