一文读懂丨肿瘤免疫治疗原则
| 导读 | 肿瘤免疫治疗历史悠久,但是2010年以来才发展迅速。肿瘤免疫治疗旨在通过激活或重新激活免疫系统,杀死或控制癌细胞。 |
机体免疫系统已经发展为包含固有免疫系统和适应性免疫系统的复杂系统。固有免疫始于物理屏障(皮肤,黏膜),涉及免疫细胞(嗜中性粒细胞和NK细胞)的非特异性防御。适应性免疫系统由固有免疫细胞演变而来,固有免疫细胞包含B细胞,受淋巴细胞“管制”。适应性免疫系统与免疫系统管理,病毒感染处理最相关,是控制和消除肿瘤最重要的部分。适应性免疫细胞通过抗原呈递识别其他细胞。
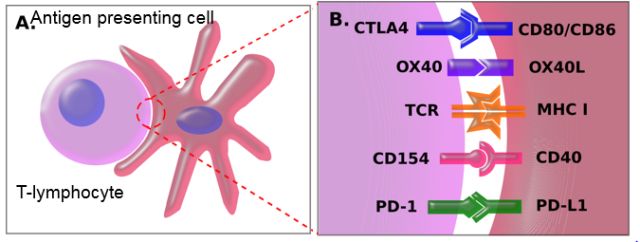
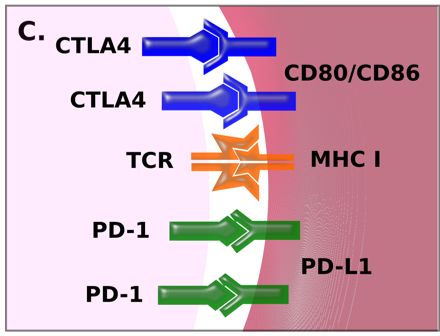
免疫激活失控会引发自身免疫性疾病,如溃疡性结肠炎,皮炎和间质性肺炎。免疫系统的活性受共刺激分子,即免疫检查点调控。当发生抗原识别时,其他分子与免疫细胞和靶细胞表面分子相互作用以确定相互作用的平衡。如果很大程度上信号是正性的,免疫细胞会激活并攻击靶细胞呈递的抗原。反之,如果信号是负性的,免疫细胞会失活,这种失活有时是永久性的,并且抗原被识别为正常/自身抗原。癌症相关免疫检查点包括CTLA-4,PD-1和PD-L1。
肿瘤免疫监视和免疫逃逸
每一种临床上可检测到及临床相关肿瘤均可通过免疫系统消除。微小癌症一旦形成,其表达的异常蛋白将产生所谓的“新抗原”,该新抗原可以被免疫系统识别。肿瘤通过该过程被编辑,可能在此时被消除,即所谓的免疫监视。有些肿瘤可以进入免疫系统的平衡状态。如果这种平衡受到年龄,疾病或医源性病因干扰,肿瘤可以逃脱并逃避免疫控制。肿瘤免疫治疗尝试在许多方面纠正免疫逃逸机制,但是肿瘤细胞逃避免疫系统的关键机制可能是负性免疫检查点信号传导。
肿瘤免疫治疗范围
肿瘤免疫治疗可以按照以下方式分类:a)主动刺激免疫系统,或被动改变免疫系统信号或细胞群,以及b) 治疗靶向特异性,已知抗原靶标,或非特异性刺激免疫系统。
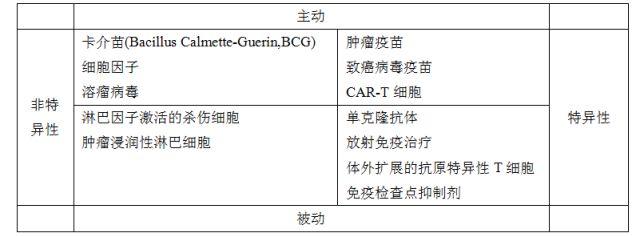
主动非特异性肿瘤免疫治疗
➤卡介苗(Bacillus Calmette-Guerin, BCG)是一种最常用和最早被发现的肿瘤免疫治疗之一。该结核分枝杆菌活减毒株经膀胱内灌注可减少切除的非肌层浸润性膀胱癌复发。作用机制为非特异性炎性反应;副作用可能包括排尿困难和其它下尿路症状。
➤免疫刺激性细胞因子,如干扰素-α和细胞介素-2曾是转移性肾癌和黑色素瘤的主要治疗方案。干扰素-α用于切除的高危黑色素瘤的辅助治疗,但生存优势值得商榷。
➤溶瘤病毒,如T-VEC(talimogene laherparepvec)和CAVATAK®(Coxsackievirus A21)是减毒或修饰的病毒,可直接注入肿瘤块或静脉注射。肿瘤细胞感染与免疫反应激活有关,某些患者甚至可以扩散到其他未注射的肿瘤部位(“远隔”效应)。
主动特异性肿瘤免疫治疗
➤肿瘤疫苗可以靶向单个肽,蛋白质或同种异体癌细胞,但大多数疫苗未能改善患者结局。Sipeleucel-T是一种应用前列腺癌细胞系的异基因疫苗(在澳大利亚不可用)。
➤致癌病毒疫苗是肿瘤免疫疗法中最常见和最重要的形式。
➤CAR-T细胞是自体患者衍生的T细胞,个别病例产生了很大的反应(如CD19+小儿B-ALL),但毒性相当大。
被动非特异性肿瘤免疫治疗
➤淋巴因子激活的杀伤(LAK)细胞和肿瘤浸润淋巴细胞(TIL)是取自外周血或肿瘤组织并在体外扩增的自体患者免疫细胞。TIL可以大幅扩增,然后再次注射入患者体内。
被动特异性肿瘤免疫治疗
➤人源化单克隆抗体通过多种机制导致癌细胞死亡,如抗体直接作用(受体阻断或激动剂活性,药物或细胞毒性制剂传递),补体依赖性细胞毒性,抗体依赖性细胞毒性。
➤放射免疫治疗应用与抗体结合的α发射放射性同位素(如177- l)特异性将放射治疗递送至肿瘤细胞沉积物。
➤抗原特异性T细胞可以以TIL类似的方式在体外扩增。
免疫检查点抑制剂
免疫检查点对于肿瘤免疫逃逸非常重要,因此免疫检查点抑制剂相关设计如雨后春笋般迅速展开。许多免疫检查点抑制剂已经应用于临床实践,多种药物正处于临床试验和早期研发阶段。
目前,免疫检查点信号传导调控主要集中于负性调控分子,检查点抑制剂作用机制相对简单。检查点被激活时,免疫系统处于平衡状态。如果肿瘤细胞增加检查点信号,免疫系统会被抑制。应用抗体阻断CTLA-4,PD-1/PD-L1信号传导通路可以纠正这种平衡,使得免疫系统能够重新建立对肿瘤的控制。
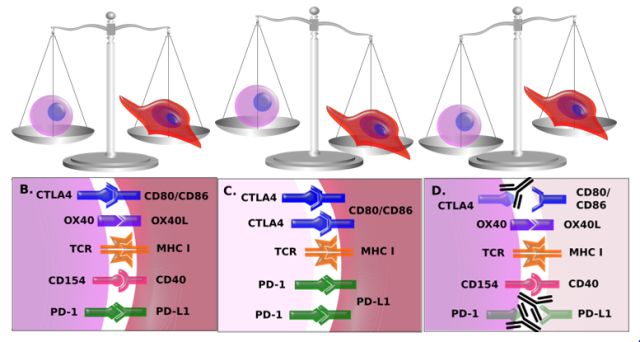
Ipilimumab(Yervoy®)是第一类检查点抑制剂,可阻断负调控检查点CTLA-4。细胞内CTLA-4分子表达于T细胞表面时,CTLA-4与B7结合,关闭T细胞活化。Ipilimumab与CTLA-4结合并抑制CTLA-4和B7结合。这意味着T细胞仍然被激活。Ipilimumab作用部位仍不明确,但可能有助于扩大肿瘤和远处淋巴结免疫应答。Tremelimumab是另一种抑制CTLA-4检查点蛋白的抗CTLA-4抗体。这两种抗体的活性和副作用可能类似。Pembrolizumab(Keytruda®)和nivolumab(Opdivo®)是抗PD-1抗体,可以阻断PD-1与PD-L1和PD-L2结合。PD-L1在癌细胞上过表达,从而被癌细胞利用逃避免疫系统的杀伤作用。Atezolizumab,avelumab和durvalumab是抗PD-L1抗体,可以阻断PD-L1与PD-1结合。PD-L1抗体的活性和副作用可能相似,但相较于PD-1抗体,可能疗效欠佳,但毒性较低。目前正在研究检查点抑制剂组合以及免疫检查点与其它抗癌药物组合的疗效。例如,ipilimumab和nivolumab组合使黑素瘤和肾细胞癌患者明显获益。
免疫检查点抑制剂的副作用
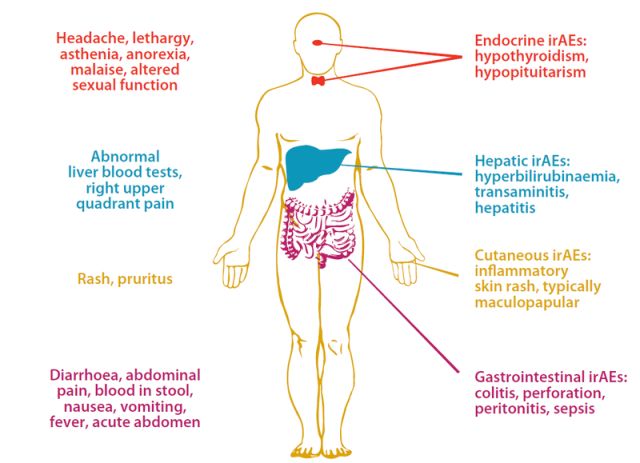
免疫检查点抗体的副作用是由于自身免疫过度激活。常见副作用包括腹泻和皮疹,多为轻度且易处理,但有时也会危及生命。免疫相关不良反应包括:
➤胃肠道免疫相关副作用:检查点抑制剂引发的结肠炎始于腹泻,但可能发展为穿孔和腹膜炎。
➤皮肤免疫相关副作用:躯干常出现斑丘疹,如果产生抗黑色素细胞抗原免疫应答,可发生白癜风。
➤内分泌免疫相关副作用:类似于产后自身免疫疾病,检查点抑制剂可引起甲状腺炎和垂体炎。
➤肝脏免疫相关副作用:肝炎和胰腺炎不常见。
➤呼吸道免疫相关副作用:检查点抑制剂与肺炎和鼻窦炎相关。
经免疫检查点抑制剂治疗的患者出现的任何疾病均应排除自身免疫性疾病。
免疫检查点治疗相关副作用管控
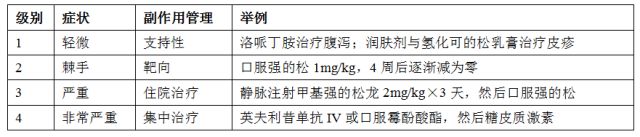
一般地,肿瘤治疗副作用通过其级别或强度表征:

检查点抗体相关副作用管理因症状而异,止于反应。就免疫相关副作用而言,进行支持性护理和免疫抑制,如下:
免疫检查点治疗的预期管理
➤检查点免疫抗体仅有助于某些患者。某些检查点抑制剂,如ipilimumab,pembrolizumab和nivolumab,疗效显著且持久,给患者和临床医生带来了极大的希望。
➤获益可能需要很长时间。检查点抑制剂不是直接抗癌剂,而是通过激活免疫系统发挥作用。正如副作用,获益也需要数周或数月。对于患者及其家属而言,这可能是一个非常紧张和困难的时刻。
➤稳定疾病较反应常见。许多患者的肿瘤会缩小,但常见的情况是肿瘤稳定。这不是一件坏事,患者可以获得很长的生存期和良好的生活质量。
➤许多癌症对检查点抑制剂无反应。目前尚不清楚检查点抑制获益人群。多数研究聚焦黑色素瘤,肺癌,肾癌和膀胱癌。结直肠癌可能不成功,但已确定可能有一小部分患者获益;乳腺癌(三阴性)同理。前列腺癌可能CTLA-4和PD-1靶向药物耐药。
➤检查点抑制剂治疗患者仍必须接受良好的姑息治疗和临终关怀咨询。虽然患者对单剂nivolumab或pembrolizumab有反应,但许多患者将继续进展并因癌症死亡。
参考文献:
1. Dr Craig Gedye, Cancer Council Australia Oncology Education Committee. Cancer Council Australia. Clinical Oncology for Students(2016).
2. Michael Postow, MDJedd Wolchok, MD, PhD.Toxicities associated with checkpoint inhibitor immunotherapy.UpToDate Terms of Use. Feb 22, 2018.
3. Cappelli LC, Naidoo J, Bingham CO 3rd, Shah AA. Inflammatory arthritis due to immune checkpoint inhibitors: challenges in diagnosis and treatment. Immunotherapy 2017; 9:5.(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发