阿尔兹海默症家庭的希望寄托—干细胞疗法
| 导读 | 随着老龄化进程的加快,老年期痴呆的患病率正逐年上升。 阿尔茨海默病(Alzheimer’sdisease,AD)是最常见的神经退行性疾病,也叫老年期痴呆。从目前研究来看,该病的可能因素和假说多达30余种,如家族史、女性、头部外伤、低教育水平、甲状腺病、母育龄过高或过低、病毒感染等。临床表现为进行性痴呆、 |

随着老龄化进程的加快,老年期痴呆的患病率正逐年上升。
阿尔茨海默病(Alzheimer’s disease,AD)是最常见的神经退行性疾病,也叫老年期痴呆。从目前研究来看,该病的可能因素和假说多达30余种,如家族史、女性、头部外伤、低教育水平、甲状腺病、母育龄过高或过低、病毒感染等。临床表现为进行性痴呆、记忆力的衰退和认知功能的减退,往往智力越来越退化,缓慢而痛苦地带走一个人的认知、思考,行动能力,最终尊严跌到谷底,病人及亲人都承受着巨大的痛苦。
在中国,阿尔茨海默病的发病率约为5%,多发于65岁以上人群,人数约为600万人,并以每年三、四十万人的数量增长。据美国最新国家统计数字显示:2018年将有570万名各年龄阶段的美国人患阿尔茨海默病,2025年,65岁及以上的老年阿尔茨海默病患者将达到710万,将增加近29%,也就是说,每65秒钟就会有人患上阿尔茨海默病。据最新阿尔茨海默病协会公布的“2018年阿尔茨海默病事实和数字”报告,连续两年,美国用于治疗阿尔茨海默症或其他痴呆症患者的总支出预计将超过2500亿美元(2770亿美元),这比去年增加近200亿美元。调查机构GlobalData预估,2023年阿尔茨海默病医疗市场可达130亿美元。
这是一个急需要解决的疾病,不仅仅是个人及家庭的问题,更是一个社会问题。
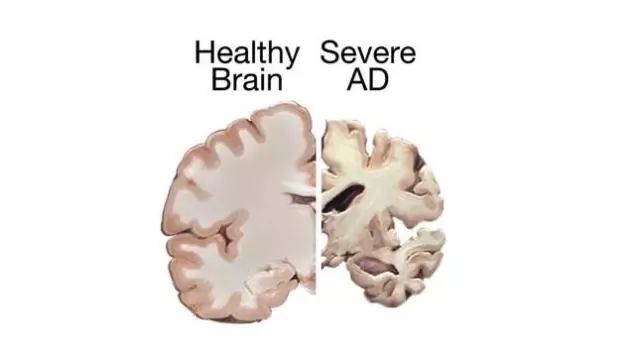
阿尔兹海默症标志性病变是患者大脑中β淀粉样蛋白的积累,细胞内神经元纤维缠结和神经元丢失等,在治疗上,传统的药物疗法尤其是胆碱酯酶抑制剂仍然是治疗AD的一线治疗方案,主要机制是维持退化的神经元功能,对早期的患者有一定的疗效,不过由于阿尔兹海默症起病隐匿,不易察觉,往往发现时已经处于中晚期,因此这类患者的药物疗效并不理想。除了药物治疗之外,还有免疫疗法,不过免疫疗法的副作用大也是待解决的问题。
但是无论是药物治疗还是免疫疗法,都只是缓解疾病的进展过程,不能根治,而干细胞疗法的出现似乎给根治阿尔兹海默症带来了希望。
干细胞疗法
自1998年人胚胎干细胞成功获得后,科学家们就开始研究用干细胞疗法治疗阿尔兹海默症。主要包括胚胎干细胞(embryonic stem cells,ESCs),骨髓间充质干细胞(mesenchymal stem cells,MSCs)、脑源性神经干细胞(neural stem cells,NSCs)和诱导性多能干细胞(induced pluripotent stem cells,iPSCs),基本思路是利用体外扩增的干细胞来修复和替代受损神经元,重建细胞环路和功能,神经保护和营养支持,抑制淀粉样蛋白形成等,干细胞治疗被认为是未来根治阿尔兹海默症的最具潜力疗法。
1、神经干细胞(neuralstemcells,NSC)在神经发育和修复受损神经组织中发挥重要作用。而且神经干细胞的旁分泌作用显示出了巨大的治疗潜力,在动物实验研究方面已经有了进展,有研究显示,移植分泌生长因子的神经干细胞能够增强神经和认知功能,而移植表达胆碱乙酰基转移酶的人类神经干细胞也能够逆转学习和空间记忆障碍;还有一些研究发现移植神经干细胞可以降低神经炎症。另外,施万细胞能够促进神经干细胞的增殖,将施万细胞与神经干细胞的联合移植疗效也十分明显,优于单独移植神经干细胞。另外,对神经干细胞进行基因修饰,改善神经干细胞的功能对于治疗AD也有不错的疗效。不过目前,神经干细胞移植治疗的背后机制尚未完全被确定,旁分泌释放神经保护因子和免疫调节因子以及直接分化为神经元被认为是可能性最大的两种机制;而且对于移植后神经干细胞的迁移速度和分化方向的调节等还不是太成熟,加之神经干细胞的免疫原性强,因此临床上很难应用。未来,可以选择免疫原性较弱的神经干细胞进行移植治疗。
2、诱导多功能干细胞来源稳定,免疫排斥也较少,其中神经干细胞和脑膜细胞具有高表达胚胎的调节因子Sox2,成为合适的选择。利用诱导的多分化干细胞衍生出结构和功能成熟的神经元,并形成具有电生理活性的突触网络。在诱导过程中使用一些额外的转录因子,也有可能直接分化为特定的神经元亚型,如多巴胺。诱导多能干细胞是一种比较新的技术,由于获取比较困难,而且体细胞诱导为多分化干细胞的诱导机制也不是很清楚,以及把控诱导的细胞数也是待解决问题,因此在阿尔兹海默症的临床研究中使用的也比较少。
3、胚胎干细胞,理论上分化潜能极佳,而且一些啮齿类模型动物研究也显示,胚胎干细胞移植具有恢复认知功能的作用,但是由于未分化的胚胎干细胞会带来细胞生长失控和形成肿瘤的风险,因此临床转化十分有限。
4、而间充质干细胞被认为是治疗AD最有前景的种子细胞,且有效性和安全性已经被很多临床前研究及临床试验证实,主要有骨髓间充质细胞,脐带间充质细胞和脂肪间充质细胞等。由于间充质干细胞来源丰富,采集方便,免疫排斥反应较弱,而且体外扩增迅速,分化方向也调控良好,在临床应用前景十分广泛,我国卫健委公布的20个干细胞临床研究项目中,间充质干细胞占据了13项,项目比达到了65%。

可喜的是,今年4月中旬,来源于间充质干细胞的全球首个干细胞治疗AD在日本诊所获批使用。
由韩国生物技术公司NatureCell及Rbio共同经营的生物之星干细胞研究所宣布,干细胞药物AstroStem获批在日本福冈三一诊所(TrinityClinic Fukuoka)商业化使用。也就是说4月12日起,该诊所就可开始使用干细胞药物治疗阿尔兹海默症。AstroStem属于静脉注射自体脂肪组织来源间充质干细胞,采用了具有13年研发史的技术。该疗法在美国开展的I期和II期试验已于2016年11月获得FDA审批准入,自2008年以来,该研究团队一直在评估静脉注射的安全性,并且静脉注射的安全性已经美国的临床试验中得到了证实。此外,已公布的临床研究表明,多次静脉注射并不太可能导致癌症。
这无疑给AD患者带来了新的希望。

政策方面
干细胞已经受到了世界越来越多的国家重视,各国纷纷加快干细胞的临床研究,列入国家科技的战略必争领域。据统计,全球约100多个重要的干细胞研究中心,主要分布在欧美和亚太地区。美国、欧盟、日本以及韩国等发展比较靠前,已有获批上市的干细胞疗法。
美国已经开始采取措施加速已经获得安全性和有效性证明的干细胞临床研究的发展,而且今年5月22日,美国国会众议院通过了“尝试权法案”,允许那些用尽当局许可疗法但都未见效的晚期病患尝试未经FDA批准的试验性疗法,紧接着,美国头脑风暴生物科技公司(Brainstorm)就宣布将通过“尝试权法案”为1名渐冻症患者提供试验性干细胞疗法NurOwn®;英国药品与保健产品监管局早在2010年就已许可针对视网膜黄斑变性开展干细胞人体治疗试验;日本政府已将再生医疗等尖端医疗技术作为“新经济成长战略”的重要支柱,致力于在2030年实现干细胞再生医疗的普及。韩国政府曾在2012年投入超过1000亿韩元以推动支持韩国在干细胞临床研究领域的发展,这些资金集中用于临床试验、干细胞治疗的安全性、干细胞研究的核心技术,以及干细胞领域相关人才的培养。今年3月,欧盟批准了干细胞疗法Alofisel用于成人非活动性/轻度活动性腔内克罗恩病患者复杂性肛周瘘的治疗,这也是欧盟批准的首个异体干细胞疗法;近日,越南也宣布开发出了首个干细胞产品,这意味着不仅发达国家,发展中国家也越来越重视干细胞技术。
我国高度重视干细胞技术的发展,干细胞被纳入《“十三五”国家战略性新兴产业发展规划》以及《“健康中国2030”规划纲要》中。近年来国拨经费超20亿元,且多项政策红利为我国干细胞产业的发展提供了有利条件。
截至目前,全球已经有十余款干细胞产品获批上市,而且据NIH管理的临床研究登记系统数据显示,未来5年全球范围将有更多干细胞药物获批上市。干细胞疗法是医学的必然且突破性的发展,相信随着临床试验的进展以及监管政策逐渐完善,不仅仅是阿尔兹海默症,还包括其他更多的难治性疾病,都有望通过干细胞疗法出现新局面!
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发