常见心血管药被爆"致癌",22国紧急召回!
| 导读 | 7月5日, 欧洲药品管理局(European Medicines Agency, EMA)发布公告[1],宣布调查我国浙江华海制药有限公司生产的缬沙坦(Valsartan)原料药。 |
调查原由是因为,在该原料药中发现一种可能的致癌杂质:N-亚硝基二甲胺(N-Nitrosodimethylamine,NDMA)。目前,欧盟22国政府正在召回含有该公司生产缬沙坦原料的药品。

图片来源:
http://www.ema.europa.eu/docs/en_GB/document_library/Press_release/2018/07/WC500251498.pdf
Valsartan和NDMA是干嘛的?
Valsartan
该药主要用于治疗轻、中度原发性高血压,心力衰竭和心肌梗死。是临床常用药。
也可用于糖尿病预防和糖尿病肾病治疗(具体用法用量及适应证,参见本文附录)。
NDMA
NDMA是一种半挥发性有机化学品,气味与味道很弱,易溶于水、醇、醚等,是一种有毒物品。主要用于火箭燃料、抗氧剂等制造。
忽然记起,2013年的“复旦投毒案”和“黄浦江死猪事件”,都和它有关。

NDMA由二甲胺与亚硝酸盐在酸性条件下反应而生成,微量存在于多种食品和消费品中,例如可食用腌制肉、鱼、啤酒和烟草烟雾中等,但是它不会在生物体中富集。
NDMA还是用于自来水消毒的氯或二氧化氯的副产物(如下图),而用臭氧作消毒剂则不会生成NDMA。它不容易降解、吸附或挥发,不能被活性炭吸附,因此不容易从饮用水中去除。

图片来源:http://jz.docin.com/p-1395663421.html
NDMA经消化道、呼吸道吸收迅速,经皮肤吸收缓慢。动物实验表明,它主要引起肝脏、肾脏和呼吸道肿瘤[2]。在2017年10月27日世界卫生组织国际癌症研究机构公布的致癌物清单中,属于2A类致癌物。
(如果还不清楚,请读者自行百度2013年的“复旦投毒案”,在本频道不展开介绍。)

国内市场有这种药流通吗?
据《中国证券网》昨日发布的消息称[3]:“目前华海药业的缬沙坦原料药主要销往北美、欧洲、印度、俄罗斯和南美等市场。该公司已停止了缬沙坦原料药的商业生产,对库存进行了单独保存,暂停所有供应。此外,目前该公司缬沙坦制剂在国内尚未上市销售;同时,该公司已对其他沙坦类产品进行了评估,因生产工艺不同,确认其他沙坦类产品中不存在该NDMA 杂质。”
浙江华海药业发布公告称其已收到国家食品药品监督管理总局签发的缬沙坦片药品注册批件。
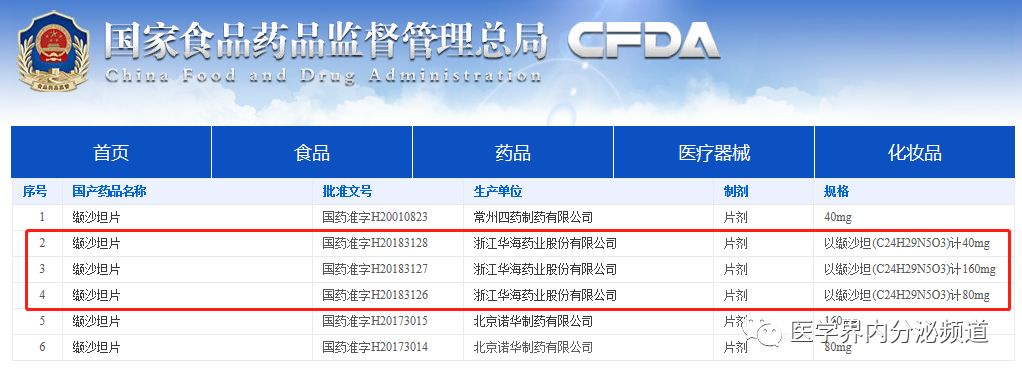
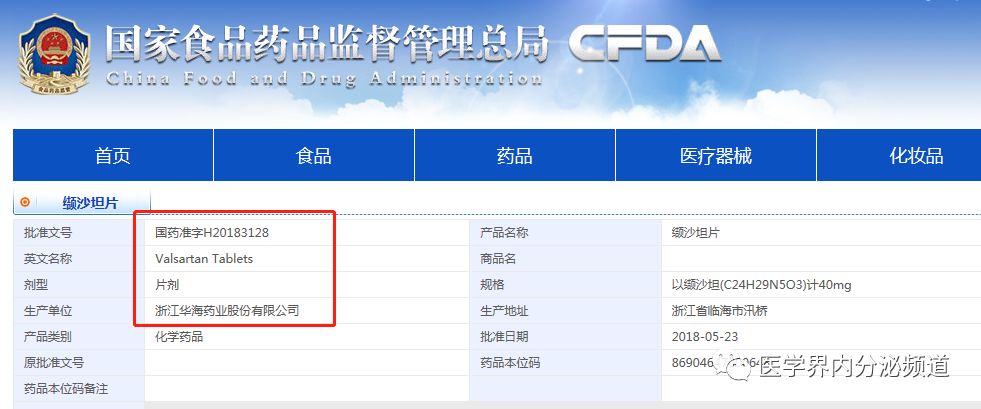
横屏查看大图,图片来源:http://app2.sfda.gov.cn/datasearchp/all.do?tableName=TABLE25&formRender=cx&searchcx=%E7%BC%AC%E6%B2%99%E5%9D%A6%E7%89%87&name=%E7%BC%AC%E6%B2%99%E5%9D%A6%E7%89%87
EMA的公告与建议
EMA在其7月5日的公告中敬告患者:

图注:
1.在用于制备缬沙坦药物的活性成分中发现了杂质;
2.欧盟只有一些缬沙坦药物受到影响,这些药物正在被召回;
3.除非你收到主治医生或药剂师提醒,否则不应该停止服用缬沙坦;
4.下一次给你开处方时,他们可能会给你开另一种缬沙坦药物(或备选治疗方案);
5.如果你对治疗有任何疑问,请向药剂师咨询,你服用的药品是否需要被召回;
6.如果你正在接受缬沙坦的临床试验,有任何疑虑可向主治医生提出;
7.EMA将继续跟进,评估NDMA杂质对患者造成任何可能的风险。有进一步消息会公布。
EMA表示,原料药中存在NDMA可能与原料的生产方式的变化有关。
接下来,EMA将调查这些缬沙坦药物中NDMA的含量水平,以及对服用它们的患者可能产生的影响;并研究采取何种有效措施来减少或消除未来在生产缬沙坦原料药中产生的NDMA杂质。作为预防措施,审查也将考虑其他缬沙坦药物是否会受到影响。
这个事情耐人寻味
据《中国证券网》昨日发布的消息称[3],此药品原料问题是由浙江华海药业主动上报给EMA等相关机构的。有意思的是,截止到公告发布之日,各国的注册法规对此类药生产工艺中产生的 NDMA 杂质的可接受控制限度尚未出台标准。

附录:缬沙坦临床用药说明[4]
美国食品药品监督管理总局(FDA)批准适应证及用法用量
1. 心力衰竭:每次40mg,口服,每天2次,可增加至320mg/d。
2. 高血压:每日80~160mg,口服,可增加至320mg/d。
3. 心肌梗死:每次20mg,每天2次,可增加至320mg/d。
超说明书用药
1. 糖尿病预防用药:每日80~160mg,口服。
2. 糖尿病肾病:每日40~80mg,口服。
不良反应
-
常见(>10%):头晕。
-
少见(1%~10%):背痛,咳嗽,腹泻,困倦,头痛,高钾血症,低血压,恶心,肾毒性,皮疹,心动过速等。
-
罕见但严重( <1%):血管性水肿,出生缺陷,肝毒性,横纹肌溶解症。
本药治疗前和治疗中需监测血常规、电解质和肾功能检查。
禁忌
对该药过敏者、妊娠期及哺乳期妇女禁用。
药物相互作用
临床没有发现明显的药物相互作用。已对以下药物进行了研究:西米替丁、华法令、呋塞米、地高辛、阿替洛尔、吲哚美辛、氢氯噻嗪、氨氯地平和格列本脲。
虽然缬沙坦大部分与血浆蛋白结合,但是体外实验没有发现它在这一水平与其他血浆蛋白结合药物(如双氯芬酸、呋塞米、华法令)发生相互作用。
与保钾利尿剂(如螺内脂、氨苯喋啶、阿米洛利)联合应用时,补钾或使用含钾制剂可导致血钾浓度升高和引起心力衰竭患者血清肌酐升高。因此,联合用药时需要注意。
注意事项
-
不要突然停药。
-
在有医学监护下使用补钾药或钾盐。
-
本药可能引起头晕,避免开车、操作机械、从事需要警觉的危险活动。
-
建议服药期间避免饮酒和服用非甾体抗炎药(如阿司匹林)。
贮藏
遮光,密封,在30℃以下保存。(转化医学网360zhyx.com) 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发