非编码RNA出人意料的新才能
| 导读 | 之前的研究认为,非编码RNA不编码蛋白质,属于“垃圾”RNA。而随着研究的深入,科学家逐渐发现,非编码RNA含有丰富的信息,是生命体中有待探索的“暗物质”。 |
在《来自基因组暗物质的lncRNA、ciRNA和miRNA》一文中我们提到:人类基因组中也存在大量被称为基因组“暗物质(dark matter)”的非编码序列,包括基因间非编码序列、内含子非编码序列等。所谓基因组“暗物质”,其实就是基因组中的非编码RNA——不包含用于制造蛋白质的版图,构成了超过 95% 的人类基因组。之前的研究认为,非编码RNA不编码蛋白质,属于“垃圾”RNA。而随着研究的深入,科学家逐渐发现,非编码RNA含有丰富的信息,是生命体中有待探索的“暗物质”。
目前已发现很多非编码RNA具有的重要生物学功能。随着研究的不断深入,RNA的“才能”也被逐一挖掘,它可以是具有催化作用的酶类物质,可以抵抗感染,可以作为基因调控因子。同时,越来越多的证据表明,一系列重大疾病的发生发展与非编码RNA调控失衡相关。最近科学家又发现了非编码RNA出人意料的新才能——维护基因组稳定和维持细胞核的完整性。
首先看看非编码RNA维护基因组稳定的功能:
基因组稳定性的维持是一切生命活动的基础,多种外源和内源因素产生的DNA损伤和复制应激,构成了基因组不稳定的主要来源。有最新的研究指出,人类肿瘤的发生中有高达三分之二的因数要归咎于DNA修复的失调。著名的肿瘤抑制因子p53能够参与DNA修复和维护基因组的稳定,从而抑制肿瘤的形成。长非编码RNA是近年来生命科学领域研究的热点分子,它介导了细胞内各个方面的生物学功能。但是,是否存在长非编码RNA参与DNA修复和维持基因组稳定,如果存在,它又是如何介导了肿瘤抑制因子p53的DNA修复功能,这些问题的答案迄今仍然不是很清楚。
2018年 3月 28日,中国科技大学吴缅教授研究组和澳大利亚纽卡斯尔大学张旭东教授合作,在国际著名学术期刊《自然 -细胞生物学》(Nature Cell Biology)在线发表题为“GUARDIN is a p53-responsive long noncoding RNA that isessential for genomic stability”的研究论文。
吴缅研究组发现,受p53调控的长非编码RNA GUARDIN(这个RNA由吴缅研究组的实验室命名,含义是指它像卫士一样护卫基因组的完整),不管在生理稳态或在遭遇毒性应激的条件下,都能参与维护基因组的稳定。GUARDIN同时通过两种机制发挥这种维护作用:
1.GUARDIN作为“海绵分子(sponge molecule)”吸附微小RNA 23a (miRNA-23a),促进端粒重复序列结合因子2(TRF2)的表达,以此来维持染色体末端结构的完整性;
2.GUARDIN可以作为“分子支架”增加BRCA1(乳腺癌1号基因)的稳定性,而BRCA1是基因组双链断裂的修复酶;具体分子机制是GUARDIN可以作为一个支架促进BRCA1与BARD1(BRCA1相关的RING结构域蛋白1)的结合而稳定BRCA1,维持细胞的DNA修复能力。
去除GUARDIN表达后会触发细胞凋亡和衰老,同时当GUARDIN表达被激活后,肿瘤细胞对于靶向DNA损伤的化疗药物(例如Olaparib,一种PARP抑制剂)敏感性会增加,移植瘤的生长被抑制,这意味着GUARDIN具有潜在的抑癌效应,可能成为癌症临床药物治疗的潜在靶标。
中国科大吴缅教授和澳大利亚纽卡斯尔大学张旭东教授是本文的共同通讯作者,吴缅实验室已经毕业的胡汪来、金雷和徐安为该论文的共同第一作者。该研究得到了基金委、科技部和中科院的基金资助。
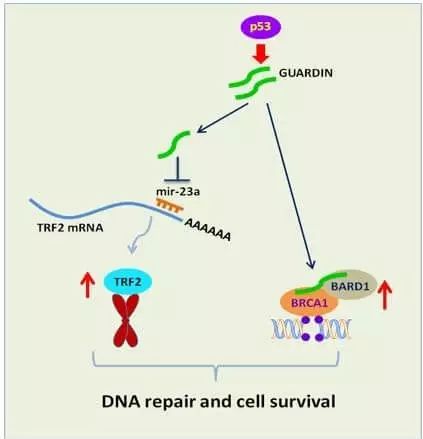
GUARDIN 维护基因组稳定的功能示意图
论文链接:https://www.nature.com/articles/s41556-018-0066-7.pdf
再来看看非编码RNA维持细胞核的完整性的功能:
我们已经知道大多数真核生物基因组被转录成ncRNAs,包括microRNAs(长度为21-25个核苷酸的miRNA)和长的非编码RNAs(lncRNAs,> 200个核苷酸长)以及非编码环形RNA(ciRNA)。虽然miRNA被认为在细胞质中主要通过抑制翻译起作用,lncRNAs是细胞核中不同生物过程的重要调节因子。与其他因素一起,lncRNA为特定位点定义的染色质结构的组装提供了框架,从而调节基因表达,着丝粒功能和沉默重复DNA元件。此外,ncRNA介导的异染色质形成与RNA干扰机制或外来体诱导的RNA衰变相关。 RNA外泌体复合物(以下简称exosome)是真核生物中结构和功能高度保守的大分子多亚基RNA降解复合物。外泌体存在于细胞核和细胞质中,参与RNA生物合成的各个方面,包括不同RNA生物型的成熟,降解和调节更新。然而,ncRNA功能的全部范围仍然难以捉摸。
虽然已经详细研究了miRNA在细胞质中的作用,但是对核miRNA的作用进行的研究还是较少,尽管以前在不同细胞的细胞核中检测到了成熟的miRNA。2018年6月4日,德国马克斯普朗克心肺研究所Barreto研究组在线在Nature Genetics发表题为“MiCEE is a ncRNA-protein complex that mediates epigenetic silencing and nucleolar organization”的研究论文,该论文破译了microRNA Mirlet7d作为双向转录基因的关键调控因子的功能。发现核Mirlet7d绑定从这些基因表达的ncRNAs。Mirlet7d-ncRNA双链体进一步与核DNA结合蛋白C1D结合,后者又将RNA外泌体复合物和多梳蛋白抑制复合体( pol ycom brepressi ve com pl ex2,PRC2)靶向双向活性基因座。外泌体降解ncRNA,而PRC2通过组蛋白-赖氨酸N-甲基转移酶EZH2诱导异染色质和转录沉默。此外,研究人员将其命名为MiCEE的多组分RNA-蛋白复合物,将受调节的基因系到核周区,因此是正确的核仁组织需要的。MiCEE复合体介导双向表达基因和基因组组织的表观遗传沉默。

我们一起看看这篇论文:
原文链接:https://www.nature.com/articles/s41588-018-0139-3
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发