基于微球辅助流式细胞术的细胞外囊泡检测用于乳腺癌的诊断和分子分型
| 导读 | 近年来,液体活检作为一种新兴的疾病检测方法受到极大的关注,与组织活检相比,其具有非侵入性、取样简单、高灵敏度、可多次反复检测等优势,在肿瘤的早期诊断和动态监控中发挥着重要的作用。 |
近年来,精准医学的提出和发展为肿瘤的精确诊断和个体化治疗指明了新方向。目前,组织活检仍然是肿瘤临床诊断和分子分型的“金标准”,也是乳腺癌靶向治疗的重要依据,但组织活检侵入性的特点造成组织标本难以获取,而且肿瘤异质性的特点也会造成诊断的局限性,从而导致无法对肿瘤进展过程中肿瘤细胞分子信息的变化进行动态和实时的监测和评价。近年来,液体活检作为一种新兴的疾病检测方法受到极大的关注,与组织活检相比,其具有非侵入性、取样简单、高灵敏度、可多次反复检测等优势,在肿瘤的早期诊断和动态监控中发挥着重要的作用。
细胞外囊泡是一类细胞分泌的囊泡状结构,广泛分布于各种体液中,且携带有来源细胞的多种蛋白质、脂类、核酸等信息,被认为是一类肿瘤液体活检的重要生物标志物。然而,其纳米级的尺寸使得针对它们的检测和分析异常困难。针对细胞外囊泡检测困难的问题,近日,国家纳米科学中心朱凌副研究员、杨延莲研究员联合北京大学肿瘤医院李惠平教授报道了微球辅助流式细胞术方法进行细胞外囊泡检测和分子分型的重要进展。
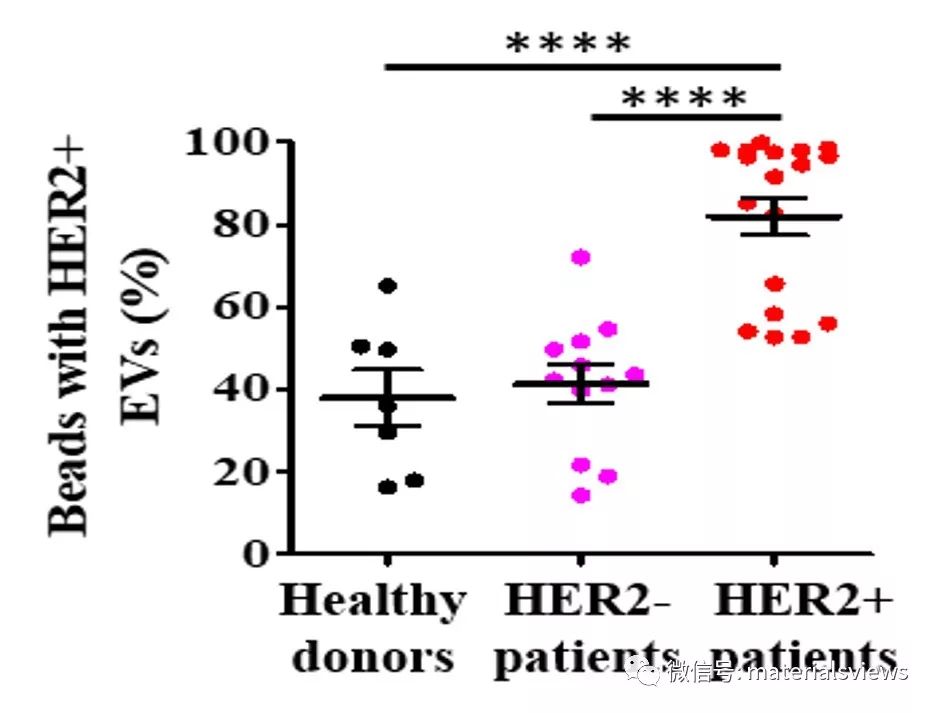
由于细胞外囊泡的纳米尺寸超出流式细胞术的检测极限,通过将细胞外囊泡富集在醛基化乳胶微球上并借助抗体的特异性识别,实现了对细胞外囊泡表面特定蛋白分子检测信号的放大,从而可通过流式细胞术对细胞外囊泡-微球复合物进行检测和分析。利用该方法对乳腺癌患者血清细胞外囊泡中两类重要的肿瘤相关蛋白标志物上皮细胞黏附分子(EpCAM)和人类表皮生长因子受体2(HER2)的表达量进行了检测,证明外泌体标志蛋白的表达量可有效反映来源细胞标志蛋白的表达状态。EpCAM和HER2阳性外泌体可有效用于乳腺癌的诊断和HER2分子分型,受试者工作特征曲线(ROC)显示曲线下面积高达0.972,证明了该方法的高灵敏度性和高特异性。除此之外,该方法对乳腺癌进行HER2分子分型的结果与临床“金标准”免疫组化的结果呈现出高度的一致性,进一步验证了该方法的准确性。该工作提供了一种非侵入性、低成本、快速的肿瘤诊断和分子分型方法,可应用于肿瘤早筛、实时监测、预后判断、疗效评价等领域,推进精准医疗的进程。
相关研究成果发表于Small Methods (Noninvasive Diagnosis and Molecular Phenotyping of Breast Cancer through Microbead‐Assisted Flow Cytometry Detection of Tumor‐Derived Extracellular Vesicles,DOI:10.1002/smtd.201800122)。第一作者为国家纳米科学中心博士生李文哲。(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发