“双上市”首日破发!手握最牛抗癌药的百济神州还有这些底牌
| 导读 | 百济神州成为首个在美股和港股同时上市的中国生物医药公司 |
自纳斯达克敲钟之后,“百济神州”于今日正式登陆港交所(股票代码为“06160”),成为首个在美股和港股同时上市的中国生物医药公司。该股以108港元平开,开盘后股价即跳水破发,盘中一度跌至103港元。截至收盘,百济神州报107.0港元,跌0.93%,港股市值821亿港元。
虽然百济神州在港交所交易首日表现差强人意,但其创新药物的开发能力还是很受业内人士青睐的。能否依靠这些底牌,扭转股票势头我们拭目以待。
1公 司 简 介
百济神州于2011年成立,创始人是王晓东博士(美国国家科学院院士),联合创始人欧雷强(保诺)。公司致力于分子靶向药物和免疫肿瘤药物研发,倾向于单药治疗与联合用药相结合治疗癌症。
公司近年大事件如下:
-
2013年,默克雪兰诺与百济神州签署协议,出资5亿美元购买了这两个药物的海外市场开发权,创造了我国新药研发历史上的一个里程碑;
-
2016年初,赴美IPO上市;
-
2017年,与新基达成战略合作,获得了新基公司在华获批药物——注射用白蛋白紫杉醇(ABRAXANE®),瑞复美(REVLIMID®)和维达莎(VIDAZA®)的独家授权,并接管其在华商业运营团队,百济神州从此开始获得产品销售收入;
-
2018年5月,任命吴晓滨博士为中国区总经理兼公司总裁;
-
2018年8月,港股再上市;
-
……
2产 品 线 简 介
无论是从成立伊始,还是当前已申报品种方向,肿瘤,无疑是百济神州主营且唯一的方向,研发方向可谓相当明确且专一。除了从新基公司获得的三个品种的独家授权外,其自研产品均为抗肿瘤药物,涉及靶点亦为肿瘤领域热门靶点,如PD-1、PD-L1、BTK、PARP、VEGFR等等。详情见下表。
表1:百济神州药物研发管线
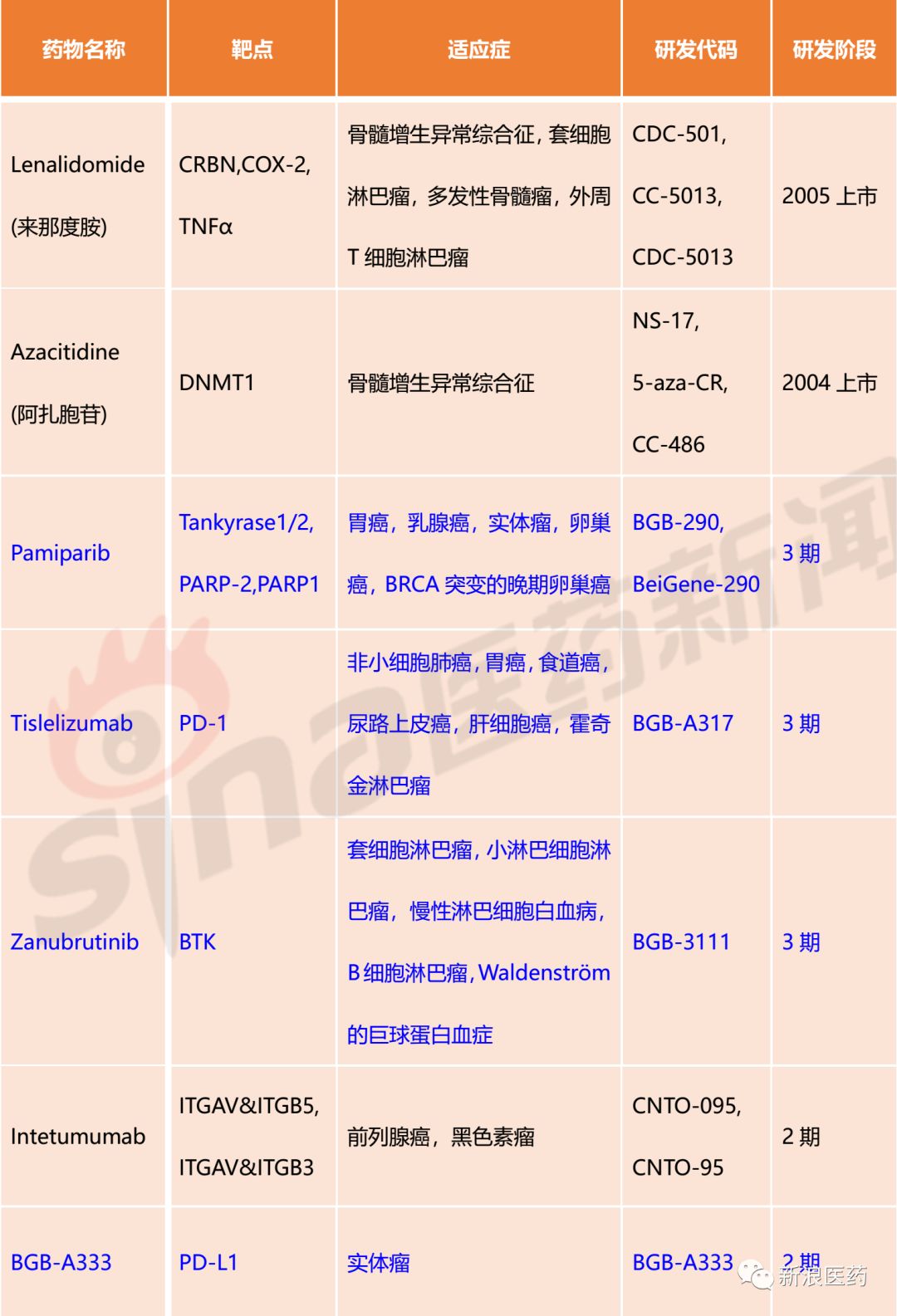
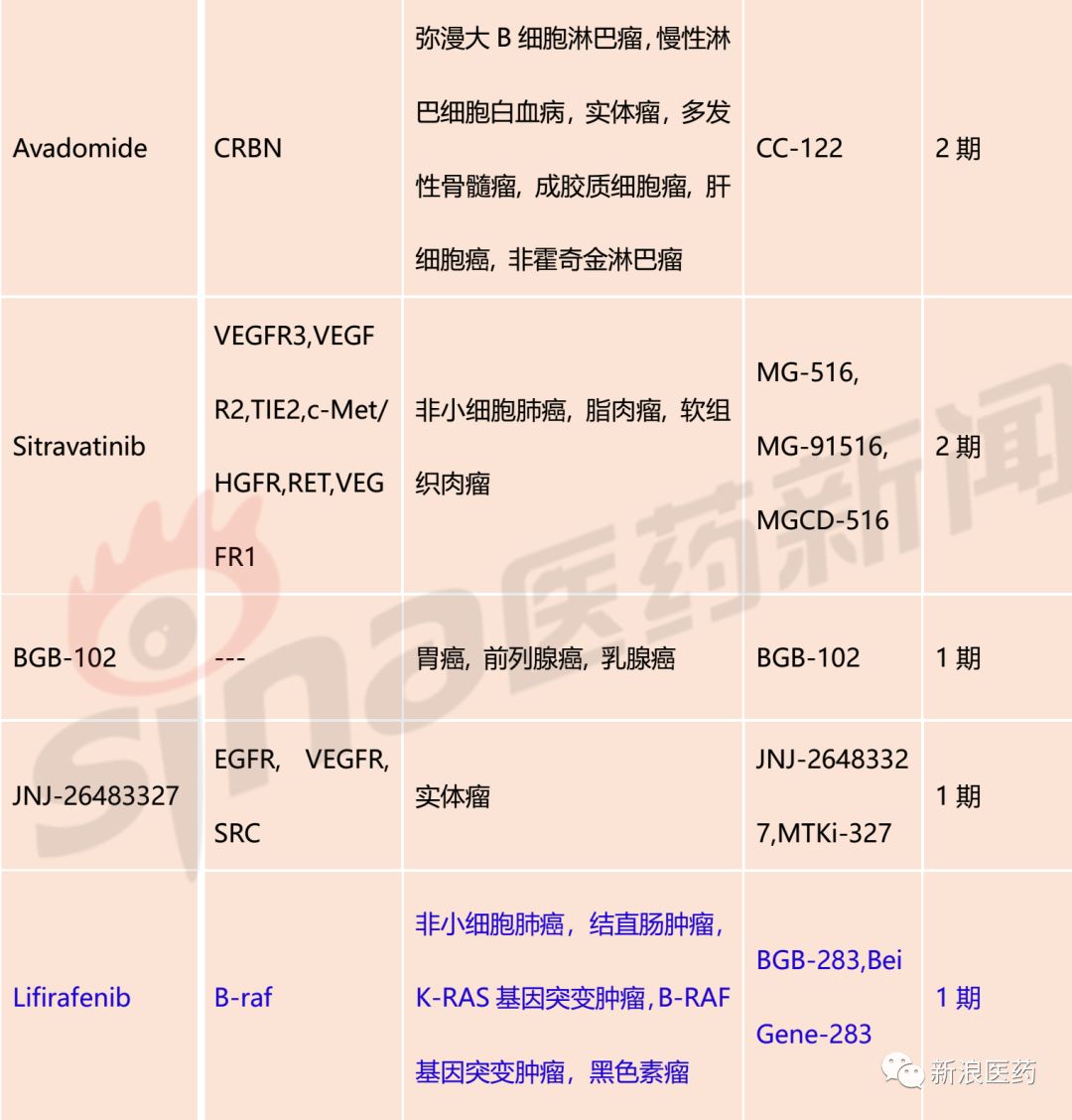
注:蓝色字体为相对比较重要的产品
3三款强大的III期临床品种
-
Pamiparib(BGB-290)
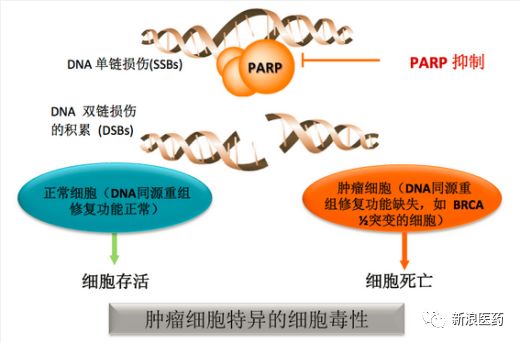
BGB-290,是一种针对PARP的强效高选择性抑制剂,具有良好的药物代谢和药代动力学特性。跟其他奥拉帕尼之类的PARP抑制剂相比,BGB-290显示出了在细胞增殖方面的改进特异性,增强的选择性可能比现有的PARP抑制剂具有更好的安全性和耐受性。
该化合物最初由百济神州研发,2013年与默克雪兰诺达成共同研发该化合物的协议。2015年11月申报中国化药1.1类临床研究,目前正在进行治疗卵巢癌和胃癌的临床三期试验,治疗乳腺癌的临床二期试验和治疗实体瘤的临床一/二期试验。
表2:BGB-290部分临床试验信息
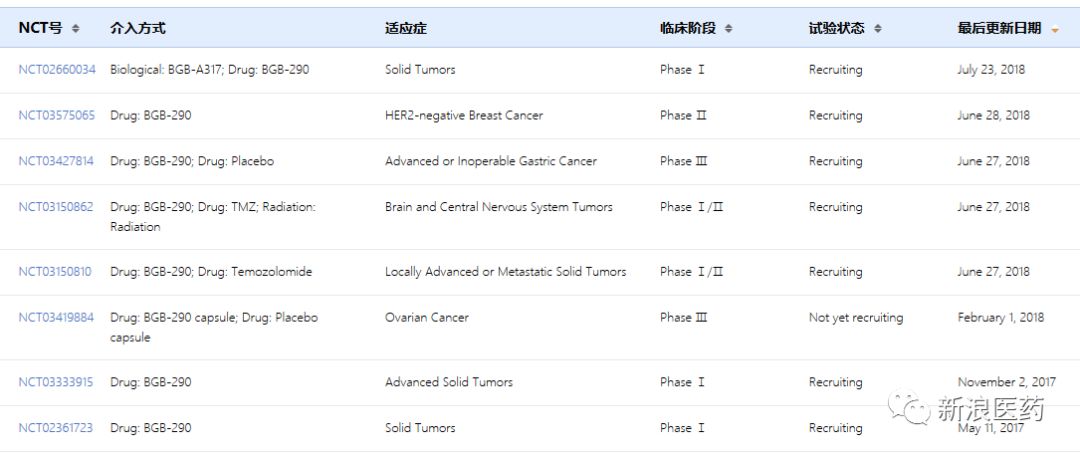
-
Tislelizumab(BGB-A317)
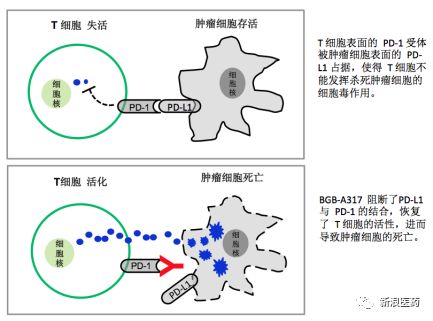
Tislelizumab,一种靶向于程序性死亡受体1(PD-1)的IgG4型单克隆抗体。此药研发是通过Fc段改造而与目前已获批的PD-1抗体存在潜在的区别,根据临床前数据,这Fc段的改造可最大限度地减少与其他免疫细胞潜在的负面相互作用。
Tislelizumab正在中国开展治疗非小细胞肺癌、肝细胞癌和食管鳞状细胞癌的临床3期试验,以及治疗霍奇金淋巴瘤、尿路上皮癌、胃癌或胃食管结合部癌的临床2期研究,并在全球开展治疗肝细胞癌的临床3期研究,同时也在新西兰、澳大利亚、中国、韩国、台湾和美国进行治疗实体瘤的临床1期研究。
2017年7月,新基公司和百济神州进行了战略合作,在美国、欧洲、日本和亚洲其它地区开发和商业化Tislelizumab。2018年1月,百济神州与勃林格殷格翰签署了一份商业协议,作为探索实践“药品上市许可持有人制度”的一部分,tislelizumab将在位于上海的世界一流的勃林格殷格翰生物制药生产基地进行生产。勃林格殷格翰将在数年内拥有该药的独家生产权(期限有可能延长),而百济神州也获得了未来勃林格殷格翰在中国为其扩大产能的数项优先权。
表3:BGB-A317部分临床试验信息
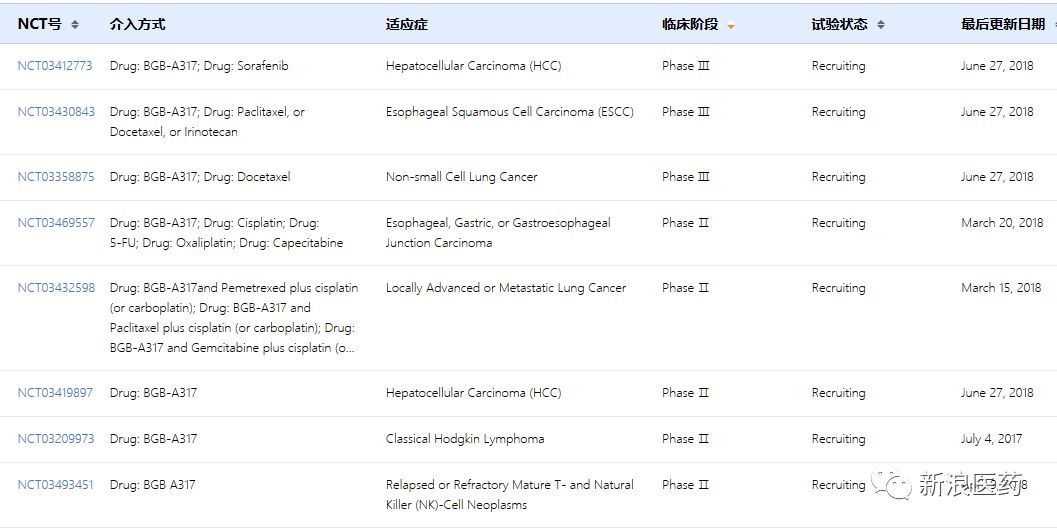
-
Zanubrutinib(BGB-3111)
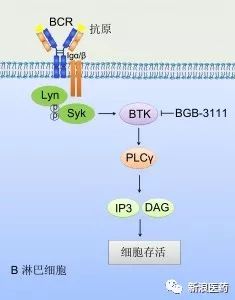
Zanubrutinib,一款在研小分子BTK抑制剂,其作为单药和与其他治疗手段进行联合用药,以针对多种淋巴瘤的注册性临床试验正在全球和中国广泛开展。根据我们的临床前和临床数据,BGB-3111与ibrutinib可能存在以下差异:更好的安全性和耐受性、良好的药代动力学特性、较好的口服生物利用度、与ADCC依赖抗体的结合性更好。
2016年,BGB-3111获得FDA的3项孤儿药资格认定,分别用于治疗套细胞淋巴瘤、华氏巨球蛋白血症和慢性淋巴细胞白血病。
2017年1月,BGB-3111对原发性巨球蛋白血症(WM)的全球三期临床 试验启动。
2017年12月11日,百济神州发布了BGB-3111与在研PD-1抗体tislelizumab(BGB-A317)联合用于B细胞恶性肿瘤患者的1b期临床试验(进行中)的初始数据。
2018年7月,BGB-3111获得FDA的快速通道资格用于治疗华氏巨球蛋白血症(WM)患者。
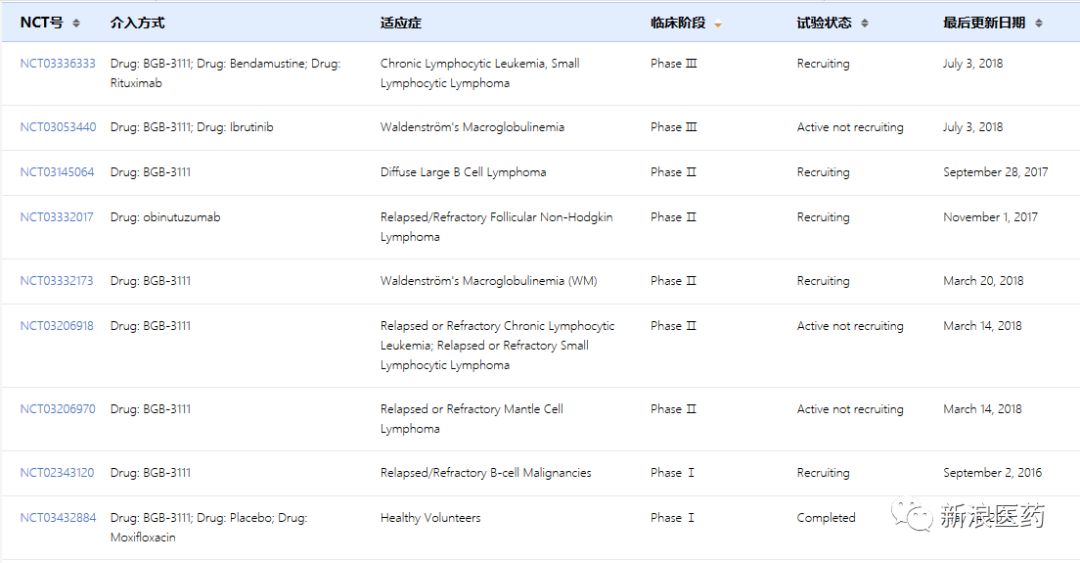
表4:BGB-3111部分临床试验信息
4进一步开发的联合用药
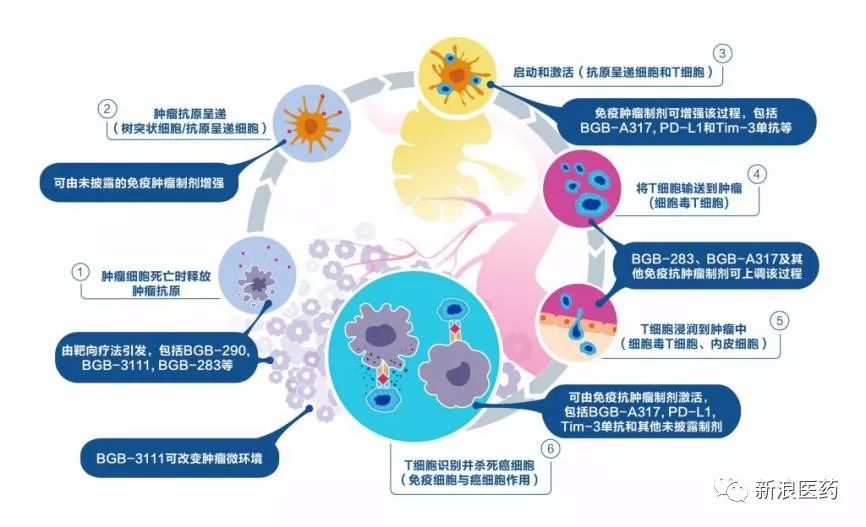
-
BGB-3111 & Obinutuzumab
公司在套细胞淋巴瘤模型中,研究了BGB-3111与第二代抗CD-20抗体Obinutuzumab联合用药的治疗效果。临床前数据,显示了BGB-3111具有潜在的肿瘤生长抑制效果,而Obinutuzumab在该模型中无活性。但同时也显示,BGB-3111与Obinutuzumab联合用药比单药治疗疗效更显著。
-
BGB-A317 & BGB-290
基于BRCA突变肿瘤细胞系通常具有基因组不稳定性的特点,且肿瘤中的效应T细胞的浸润较多,公司计划开展一项BGB-290与BGB-A317联合用药以治疗以下基因发生突变或缺陷的癌症的研究:乳腺癌基因(BRCA)、同源重组(HR)基因或错配修复(MMR)基因。相关癌症包括卵巢癌、乳腺癌、胰腺癌、前列腺癌、小细胞肺癌和恶性胶质瘤等。这将是百济神州专门针对研发管线内部候选药物开展的首个联合用药研究。
-
BGB-A317 & BGB-3111
基于在临床前研究模型中观察到的良好协同效果,公司于2016年6月30日启动了BGB-3111与PD-1抗体BGB-A317的联合用药研究。在原发性弥漫大B细胞淋巴瘤模型中,观察到BGB-A317联用BGB-3111后抗肿瘤活性得到提高,联合用药后PD-L1-和PD-L1+的弥漫大B细胞淋巴瘤模型中都可见到效果,而且在PD-L1+模型中抗肿瘤效果更加明显。因此我们推动了该联合用药的临床探索。
5笔 者 感 悟
客观讲,笔者在总结过程中,由衷羡慕百济神州的科研模式和组织结构。从科研模式来说,有专业的人去“找钱”,一线科研人员没有经济压力,可以一心扑在研发前沿,就这一点,就是许多国内从事新药研发的企业院所无法做到的。而组织结构,更是令国内新药研发企业所羡慕的,每个岗位的关键人员,都是业界大牛,把这样的一群人聚在一起,共同做着喜欢的事情,真心不易,这也足见公司的发展理念和创始人的人格魅力。故国内能有如此的创新型制药企业,能有如此的发展布局能力,真心不易,值得药界同仁长期关注!(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发