肿瘤甲基化:尘封基因的锁,蕴藏宝藏的矿
| 导读 | 它轻轻地给基因戴上了一顶美丽的帽子。这顶帽子如乐章的修饰音一样,让基因更加迷人,引无数科学家夜不成寐,相思断肠。1953年,美国人沃森和英国人克里克怀着激动的心情,狠狠地掐了一下自己。在确定不是做梦以后,他们就在《自然》杂志上发表了一份研究成果:双螺旋模型是DNA分子的存在形式,还是DNA自我复制的 |

它轻轻地给基因戴上了一顶美丽的帽子。这顶帽子如乐章的修饰音一样,让基因更加迷人,引无数科学家夜不成寐,相思断肠。
1953年,美国人沃森和英国人克里克怀着激动的心情,狠狠地掐了一下自己。在确定不是做梦以后,他们就在《自然》杂志上发表了一份研究成果:双螺旋模型是DNA分子的存在形式,还是DNA自我复制的途径。
这份举世闻名的报告,最终让他们分享了1962年的诺贝尔生理学或医学奖。
早在1909年“基因”概念就已经被正式提出,但直到DNA双螺旋结构被解封印以后,人们对基因的研究热情仿佛被一下子点燃,科学家开始如痴如醉地琢磨基因,不断解码双螺旋结构中隐藏的秘密,并尝试人为改造它,比如这导致了一度甚嚣尘上的转基因之争,以及在天使与魔鬼之间徘徊的基因魔剪crispr。
但是,在基因研究的历史长河中,还有几朵浪花。尽管当时水花很小,但现在发现,水花正在迅速扩大蔓延。它轻轻地给基因戴上了一顶美丽的帽子。这顶帽子如乐章的修饰音一样,让基因更加迷人,引无数科学家夜不成寐,相思断肠。
DNA甲基化,就是C位上一个毫不起眼的小修饰:胞嘧啶嘧啶环第5位碳原子上新增了一个甲基基团(-CH3)。它没有改变DNA序列,但它所起的作用无人可比,非同寻常。它能调节个体的生长、发育、基因表达模式以及基因组的稳定性,并且这种修饰还能被稳定传递下去。
一切的一切,只因为这顶帽子,其实是一把锁,一把尘封基因的锁。
如果我们心中有了秘密,我们会怎么做?我们会把写有这个秘密的日记层层上锁,放进只有自己才能找到的箱底。悄悄掩上心门尘封心中的秘密,不再开启。
同样,DNA上,也有许多秘密是不能被开启的。比如转座子,可以从原位上单独复制或断裂下来,环化后插入另一位点,调控后序的基因。转座子在基因组里跳来跳去的结果,就会把基因组搞得一团糟,会引起很多问题,如肿瘤、自闭症等。必须将其封印在原地。
DNA甲基化就是用来封印这些坏小子的“锁”。甲基化达到一定程度时常规的B-DNA会向Z-DNA过渡。由于Z-DNA结构收缩,螺旋加深,使许多蛋白质因子赖以结合的原件缩入大沟。说好的白首不分离,我却眼睁睁看着你离我而去,转录还没有起始,基因就被尘封失活。
另外,序列特异性甲基化结合蛋白(MBD/MeCP)可与启动子区的甲基化CpG岛结合,阻止转录因子与启动子作用,从而阻抑基因转录过程。
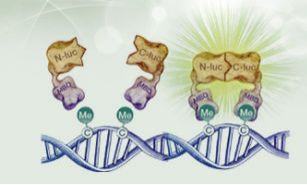
DNA甲基化在以下几个方面造成肿瘤发展、转移、恶化:一是甲基化的CpG岛二核苷酸中的胞嘧啶以较高的频率脱氨基变成胸腺嘧啶,造成基因突变;二是抑癌基因和DNA修复基因由于超甲基化而沉默;三是癌基因甲基化水平降低而活化;四是基因组总体甲基化水平降低使转座子、重复序列活化导致染色体稳定性下降。

近年,多篇重磅文章阐述了DNA甲基化在肿瘤风险预测,药物联合治疗等方面的重要进展。
DNA甲基化是理想的标记物
来自于加州大学圣地亚哥分校医学院、中山大学肿瘤防治中心、西京医院等研究机构的科研团队,发现DNA甲基化检测4种常见癌症(肺癌、乳腺癌、结肠癌和肝癌)准确率达到95%。此外,甲基化检测还能够准确识别97%大肠癌肝转移和94%的大肠癌肺转移病例。(《DNA methylation markers for diagnosis and prognosis of commoncancers》,《PNAS》,在线发表)
“由于10%的癌症属于转移性病变或者来源不明,所以癌组织的来源鉴定是选择有效治疗手段的关键。借助DNA甲基化检测,有望解决10%的未知,可确定肿瘤来源。”文章作者、加州大学圣地亚哥分校药理学教授Michael Karin解释。
DNA甲基化检测可以应用于更多不同种类的癌症诊疗中。只需要少量的组织就可以完成检测。
2018年2月《NATURE REVIEWS CLINICAL ONCOLOGY》发表了题为“Epigenome-based cancer risk prediction: rationale, opportunities and challenges”的综述,指出基于表观遗传,特别是DNA甲基化的检测,能够满足肿瘤风险预测的各项需求,为肿瘤风险筛查和预防提供了新的机遇。
文章详细罗列了有价值的甲基化标记物。
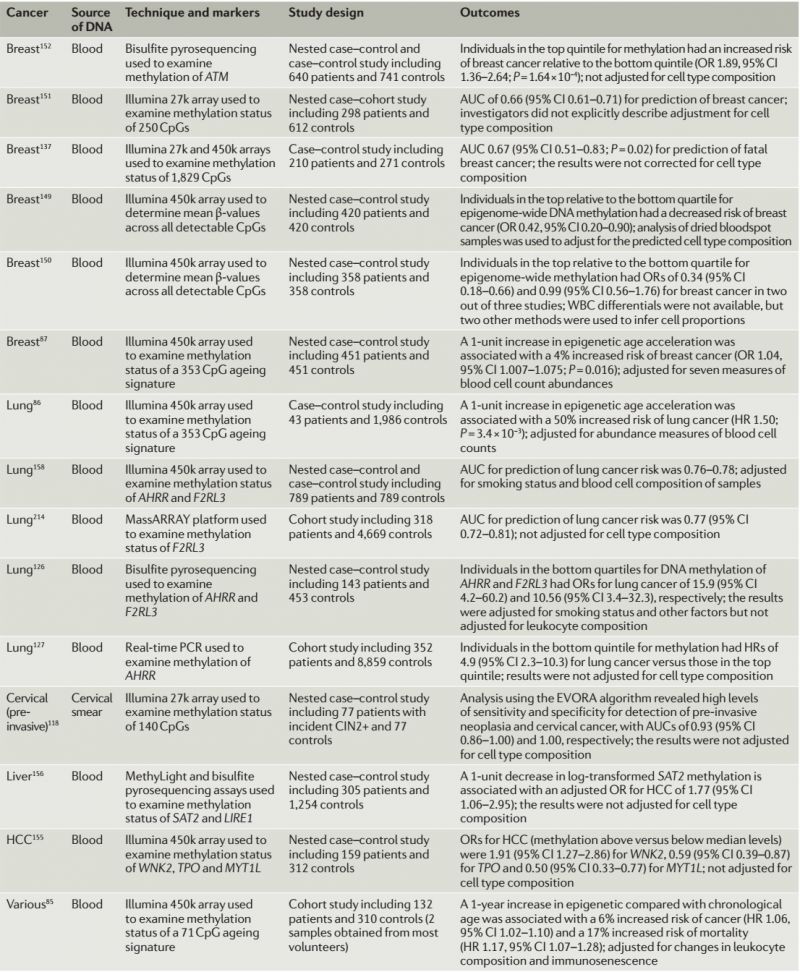 基于DNA甲基化标记预测肿瘤风险的研究汇总
基于DNA甲基化标记预测肿瘤风险的研究汇总
(NATURE REVIEWS CLINICAL ONCOLOGY 2018)
表观遗传药物治疗结果令人振奋
DNMTs抑制剂通过抑制DNMT活性以逆转异常的DNA甲基化。第一个表型修饰药物为5-azacytidine及其类似物5-aza-2'-deoxycytidine(5-aza-CdR),经FDA批准用于白血病前骨髓增生异常综合征的治疗。临床表明应用5-aza-CdR可提高部分IV期小细胞肺癌患者生存率,但该药也存在着不可忽视的毒副作用,如特异性不强,不能针对某一特定抑癌基因进行靶向治疗;高剂量的5-aza-CdR可能诱发肿瘤的转移,因此临床应用受到了很大限制。
2017年底,《Cell》发表了一项新型药物联合治疗肿瘤的研究成果。在NSCLC小鼠模型中,联合使用DNA甲基转移酶抑制剂(DNA methyltransferase inhibitors,DNMTis)联合组蛋白去乙酰化酶抑制剂(histone deacetylase inhibitors,HDACis)实现了强大的抗肿瘤反应,逆转了肿瘤的免疫入侵,并使T细胞由耗竭状态转为记忆和效应T细胞表型。在突变型NSCLC小鼠模型中,药物联合治疗给药三个月,抑制了良性肺腺瘤的恶性转化,肺部肿瘤面积减少了60%。和细胞系结果一致,癌细胞增殖被抑制。接受模拟治疗(mock treatment)的对照组小鼠则出现了肉眼可见的肺腺癌。在侵袭性NSCLC小鼠模型中,药物联合疗法给药1个月,不仅抑制了原发瘤的快速生长,而且显著降低了转移瘤的发生。
接下来,研究人员将开始在NSCLC患者中进行临床试验。让我们翘首以待好消息。
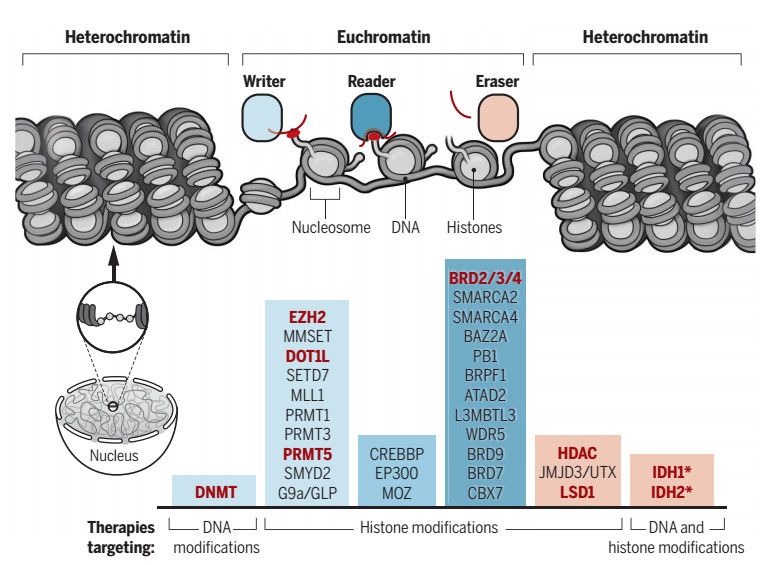 肿瘤表观治疗靶点,红色为已经在临床应用或正在临床试验中的靶点(Science 2017)
肿瘤表观治疗靶点,红色为已经在临床应用或正在临床试验中的靶点(Science 2017)
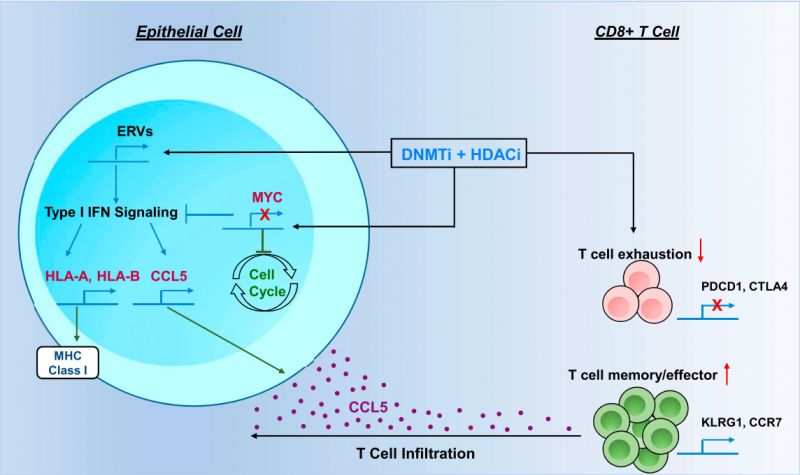 表观遗传药物联合治疗研究(Cell 2017)
表观遗传药物联合治疗研究(Cell 2017)
自生殖细胞形成开始,甲基化就调控着生命的每一个进程。
精子和卵子形成过程中,就存在甲基化。而在受精卵最初几次卵裂中,去甲基化酶大清洗DNA分子上几乎所有从亲代遗传来的甲基化标志;当胚胎植入子宫时,一种新的甲基化会快速塑整个基因组。错误甲基化模式的建立将引起如Prader-Willi综合征、Angelman综合征和脆性x染色体综合征等。
生命成长之中,各种异常甲基化又和肿瘤的发生发展密切相关。
还或许隐藏着衰老的生物学秘密。
DNA甲基化是一座蕴藏着无穷宝藏的富矿,科学家们正在努力地挖掘,破解基因的秘密,寻找对抗肿瘤的利刃,希冀变为现实的不老传说。
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发