全球首例人体内基因编辑疗法数据公布
| 导读 | 在美国加州大学旧金山分校贝尼奥夫儿童医院接受了一次前所未有的疗法:体内基因编辑.日前,该全球首例人类体内基因编辑治疗公布了首批数据。 |
2017年11月13日,44岁的美国男子、亨特氏综合征患者布莱恩•马德(Brian Madeux)在美国加州大学旧金山分校贝尼奥夫儿童医院接受了一次前所未有的疗法:体内基因编辑。日前,该全球首例人类体内基因编辑治疗公布了首批数据。
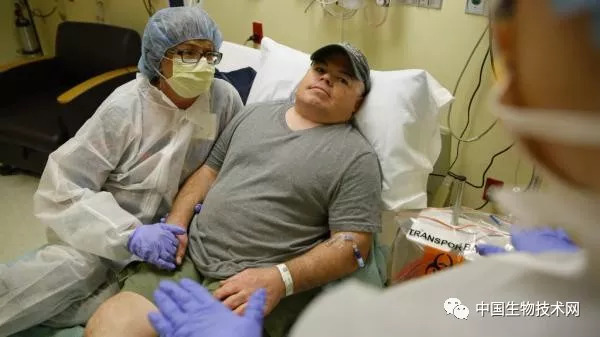
布莱恩·马德(Brian Madeux)正在接受治疗
9月5日,基因编辑老牌公司Sangamo Therapeutics(美国圣加蒙公司,NASDAQ: SGMO)在其官网公布了研究结果,公司代号“SB-913”在研疗法首例人体临床试验目前搜集的数据表明,疗法降低了用于评估亨特氏综合症严重性的生化指标水平。数据来源于参与人体临床试验的2组共4名患者,为期16周。
亨特氏综合征是一种罕见遗传病。发病者主要是男性,每10万个至17万个新生男孩中会有一位不幸罹患亨特氏综合征。亨特氏综合征患者缺少IDS基因,该基因功能是生成一种可分解有毒碳水化合物的酶。
因此,若患者IDS基因缺失,即上述扮演“清洁工”角色的酶缺位,导致细胞累积有毒的代谢物。这些“垃圾”堆得越来越多,损害包括肺、心脏和大脑在内的器官,给患者带来毁灭性打击。
在启动人体内基因编辑疗法之前,亨特氏综合征是一个全球性难题。一些患者靠注入本身缺失的IDS酶来缓解症状,但这种外来的酶很快就会被消耗掉,患者必须每周定期补充。这种酶替代疗法的开销在每人每年10万至40万美元。
早期治疗数据喜忧参半
2017年11月,圣加蒙公司启动代号“SB-913”疗法人体临床试验。
公司研究团队采用一种名为“锌指核酸酶” (Zic-Finger Nuclease,简称ZFN)的基因编辑工具。锌手指核酸酶被认为是第一代基因编辑工具,其研究可追溯至上世纪80年代。相比于眼下炙手可热的第三代工具“基因魔剪”CRISPR,锌手指核酸酶的操作更为复杂,但由于进行定位的序列更长,进行基因编辑的精准度也更高。
值得一提的是,美国食品与药品监管局(FDA)已批准锌手指核酸酶用于人体临床试验,而CRISPR尚且未被允许。圣加蒙公司则是锌手指核酸酶技术的主要专利持有者。
实施治疗的时候,马德等患者将接受三小时输液,输入的透明液体里装有腺相关病毒(AAV)、锌手指核酸酶和患者缺失的正常IDS基因,按照计划,正常基因会在肝部细胞内部被插入到安全的基因组区域。据此前介绍,仅需要1%的肝部细胞成功接收新的正常基因,亨特氏综合征就能得到有效治疗。
临床试验计划在36个月期间内评估三种不同剂量SB-913对患者的影响。圣加蒙公司最新的报告包括了第1组(低剂量)和第2组(中剂量)的早期安全性和有效性结果,每组均有2名患者。最近公司也完成了第3组治疗(高剂量,5倍中剂量)的登记和疗法实施。
公布的这份早期数据显示,在试验中,2名低剂量患者没有什么应答,但2名中剂量患者使用SB-913 16周后糖胺聚糖(重要生理指标,GAGs)水平有显著下降。具体来说,尿GAG下降51%,硫酸皮肤素下降32%,硫酸类肝素下降61%。
不过,虽然重要生理指标给出了积极数据,但在IDS酶本身的水平上,该疗法依然还充满不确定性。
研究人员在患者外周血中均没有检测到该基因表达的IDS酶增加。公司称,GAGs下降足以说明IDS基因被修复,IDS没检测到则可能有多重原因,包括现在检测方法不够灵敏、IDS可能合成后被需要的组织快速吸收等。
圣加蒙公司总裁兼首席执行官Sandy Macrae表示,公司正在研制一种更灵敏的检测方法,能够检测到低水平的酶。此外,随着公司测试更高剂量的治疗,可能会出现更明确的答案。
值得一提的是,这些数据目前尚很难解释,因为患者在试验中继续接受传统的酶替代疗法。一个安全小组将在今年晚些时候对这些数据进行评估,以确定试验参与者是否能摆脱酶替代治疗,让研究人员更清楚地了解“SB-913”效果。
圣加蒙公司的首席医疗官Edward Conner也提到,“如果这项研究的长期数据继续保持积极,治疗性基因组编辑有可能为MPS II和其他单原性疾病带来巨大的医学进步。”
圣加蒙公司计划在2019年2月于佛罗里达州奥兰多举行的2019年世界研讨会上,公布更长期的安全性和有效性结果。(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发