CAR-T细胞疗法进军实体瘤,抗癌我们是专业的!
| 导读 | CAR-T细胞疗法因为可以有效治疗恶性血液肿瘤这两年可谓是名声大噪,2017年FDA更是批准了两款CAR-T产品上市(Kymriah及Yescarta),用于治疗难治复发性急性B淋巴细胞白血病及B细胞非霍奇金淋巴瘤。然而CAR-T疗法有一个厉害的“劲敌”--实体瘤,CAR-T在实体瘤的领域可不像在血液肿瘤那么所 |
CAR-T细胞疗法因为可以有效治疗恶性血液肿瘤这两年可谓是名声大噪,2017年FDA更是批准了两款CAR-T产品上市(Kymriah 及Yescarta),用于治疗难治复发性急性B淋巴细胞白血病及B细胞非霍奇金淋巴瘤。
然而CAR-T疗法有一个厉害的“劲敌”--实体瘤,CAR-T在实体瘤的领域可不像在血液肿瘤那么所向披靡,经常败下阵来,治疗效果不好很重要的一个原因就是,回输进患者体内的T细胞很难在肿瘤组织定殖,发挥其强大的免疫功能。为此CAR-T不得不好找一群“小伙伴”来一起对付实体瘤,目前进展如何,跟随小转的脚步一起看看吧。
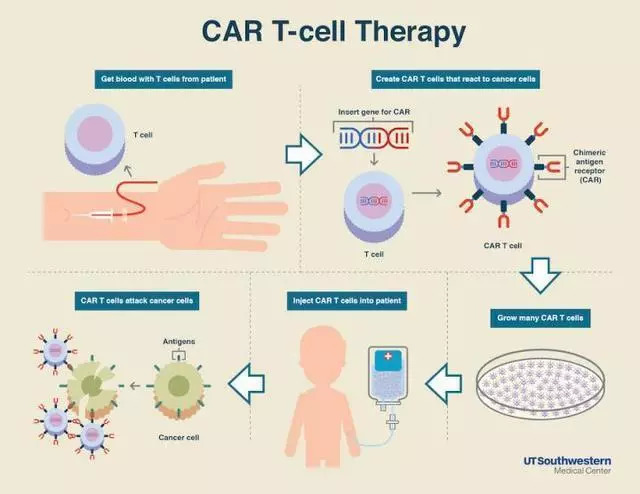
肝癌
美国华人科学家创办的生物医药公司优瑞科(Eureka Therapeutics)产品ET140202 ARTEMIS™ T细胞疗法,在治疗AFP阳性肝细胞癌(HCC)患者的概念验证研究结果显示,接受ET140202 T细胞疗法的6名患者中,3名患者的肿瘤缩小,其中1名患者达到完全缓解。ET140202 T细胞免疫疗法没有观察到任何细胞因子释放综合症(CRS)以及药物相关的神经毒性,显示了良好的安全性。
关于ET140202
ET140202携带靶向在HCC细胞表面的AFP肽链/HLA-A2复合体的人源TCR模拟抗体(TCR mimic antibody, TCRm),这是利用优瑞科公司独创的E-ALPHA抗体发现平台生成的。这种TCRm能够有选择性地与肿瘤细胞蛋白酶体降解的AFP多肽片段相结合,这些多肽片段会被主要组织相容性复合物(major histocompatibility complex, MHC)呈现在细胞表面。当TCRm抗体与这一复合体结合后,ET140202 T细胞能够被激活并且杀死肿瘤细胞。
电子显微镜下,ET140202 T细胞正在攻击肝癌细胞
生物医药公司科济生物的CAR-T产品GPC3-CAR-NK细胞在体内外均能够特异性地靶向并杀伤表达GPC3的肝细胞肝癌,并且不受血清水平可溶性GPC3、实体瘤低氧环境和TGF-β的影响。
试验结果显示,13名接受CAR-NK细胞治疗的患难治复发的肝细胞癌患者均耐受良好,未出现剂量限制性毒性(DLT)或3级以上不良反应。CAR-NK是CAR-T疗法的一个衍生技术,沿用了手枪+子弹的思路,并将原来的子弹T细胞替换为更有杀伤力的NK细胞(自然杀伤细胞),从而能够更安全、更有效的杀伤肿瘤细胞。
科济生物
科济生物是我国专注于嵌合抗原受体修饰的T细胞(CAR-T)免疫治疗的创新型企业。科济生物有:
-
针对肝细胞癌的 CAR-GPC3 T临床试验
-
针对胶母细胞瘤(GBM)的EGFR/EGFRvIII双靶点的CAR-T 的临床试验
-
针对胃癌、胰腺癌的Claudin18.2靶点治疗的CAR-T 的临床试验
-
应用人源化CD19 CAR-T治疗白血病及淋巴瘤临床研究。
胃癌
9月8日,科济生物在美国波士顿 CAR-TCR 峰会公布了 CAR-Claudin18.2 T 细胞治疗胃癌/胰腺癌的临床数据:在接受治疗的12名患者中,有8名患者出现不同程度肿瘤消退;特别是在一个经过改良的治疗亚组中,按照 RECIST 1.1 标准,6名患者有5名达到客观缓解(其中1名待确认客观缓解),包括1名完全缓解。
胶质母细胞瘤
在2016年底,研究人员对一名50岁脑瘤患者在手术、化疗、放疗6个月复发后,局部使用16次(6次手术病灶、10次脑室)针对IL13Rα2抗原的CAR-T后,颅内和脊髓肿瘤消失,应答持续7.5个月,同时中枢细胞因子和免疫细胞增加。且这个剂量(100万CAR-T细胞)没有发生3级以上毒副作用。
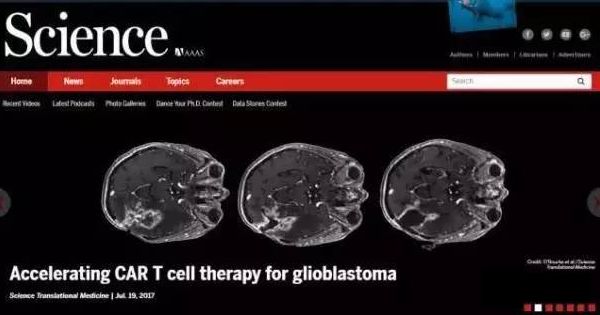
来自《Science Translational Medicine》的一项研究就对CART细胞治疗胶质母细胞瘤做出了I期临床试验的尝试。10例复发性胶质母细胞瘤(GBM)患者接受了靶向表皮生长因子受体变异III(EGFRvIII)的CART治疗,结果表明安全性很好,不过,实验中也发现了肿瘤EGFRvIII表达存在广泛变异,引发了免疫抑制肿瘤微环境导致出现耐药性等情况。要克服这些障碍,也许还需要靶向额外的抗原以及靶向免疫抑制等手段。
胰腺癌
胰腺癌会在肿瘤周围形成一个坚固的屏障,使免疫细胞无法识别,并且在血供不足的情况下,胰腺癌组织也能生存,并且非常容易转移,因此治疗比较棘手。间皮素是一种与肿瘤浸润有关的细胞膜抗原,研究发现很多肿瘤都有间皮素的高表达,以间皮素为靶点的CART细胞在胰腺癌的治疗中显示出良好的效果。有科学家设计了针对间皮素的带有CD3ζ和4-1BB共刺激结构域的二代CAR,他们用体外转录的mRNA使T细胞瞬时表达CAR分子,并用这种T细胞治疗2例不同的实体瘤患者(分别是恶性胸膜间皮瘤和转移性胰腺癌)。结果显示,这种CART细胞在外周血中短暂存在,并且可有效到达原发灶和转移灶,同时诱导体液免疫应答,显示出明显的抗肿瘤活性,而对正常组织没有明显的毒性,因此这种CART细胞用于实体瘤的治疗是安全可行的。
前列腺癌
前列腺特异性膜抗原(PSMA)特异性表达于前列腺癌组织,是一种理想的治疗靶点。科学家设计了针对人PSMA的CAR,特异性识别PSMA的CART细胞可在体外有效杀伤 PSMA阳性的前列腺癌细胞,并可在绝大多数的荷瘤裸鼠体内完全抑制肿瘤的生长,并有效延长小鼠的生存期。
小结
与血液瘤相比,实体瘤(如肺癌、胃癌、卵巢癌、乳腺癌等)和淋巴瘤中具有高度异质性的免疫微环境,因此,CAR-T疗法经常在实体瘤的治疗里败下阵来。但如果将免疫微环境与肿瘤靶点相结合,有了“小伙伴”的帮助,疗效将得到提高。
在临床试验中,CAR-T疗法用于实体瘤的治疗已经初见成效,我国的CAR-T实体瘤疗法更是走在了世界的前端。
CAR-T在恶性血液肿瘤治疗中取得的巨大成功推动了实体瘤CAR-T疗法的发展。对肿瘤发生和肿瘤进程更深入的理解可以促进未来的癌症治疗,并为癌症预防指明希望。
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发