CAR-T等免疫治疗在实体瘤的进展
| 导读 | 从2011年免疫检查点抑制剂CTLA-4抗体获批,到2014年PD-1抗体获批,再到2017年CAR-T细胞免疫疗法获批。免疫治疗已经让我们看到一个又一个奇迹。近三十多年,免疫治疗在国外曲折发展,而在包括中国在内的东亚、东南亚国家,也红火了十多年。这是一种备受争议的疗法,治疗过程危险重重。对原本无药可治的恶性 |
从2011年免疫检查点抑制剂CTLA-4抗体获批,到2014年PD-1抗体获批,再到2017年CAR-T细胞免疫疗法获批。免疫治疗已经让我们看到一个又一个奇迹。
近三十多年,免疫治疗在国外曲折发展,而在包括中国在内的东亚、东南亚国家,也红火了十多年。这是一种备受争议的疗法,治疗过程危险重重。对原本无药可治的恶性肿瘤,治疗后有人获得痊愈,而有些人迅速死亡。但是,随着成功病例的增多以及持久的效果,认同也在逐渐增加。从2011年免疫检查点抑制剂CTLA-4抗体获批,到2014年PD-1抗体获批,再到2017年CAR-T细胞免疫疗法获批。免疫治疗已经让我们看到一个又一个奇迹。被封神的PD-1抑制剂,让晚期非小细胞肺癌治愈率翻5倍。而最成功的CAR-T疗法CTL019,让90%复发性急性淋巴细胞白血病(ALL)患者得以完全缓解。
CAR-T的局限
但是,即使是获得巨大成功的血液肿瘤,CAR-T的风险依然很大。全身注射CAR-T可能导致严重的细胞因子释放综合症(CRS)以及其他毒性症状有关。谈CAR-T必谈的传奇病人Emily,现在已经健康度过了治疗后的八年。但当年她就差点因此丧命。她接受CAR-T细胞回输后,几天内就爆发了严重的炎症因子风暴(cytokine storm),濒临休克;后来,Carl June教授团队冒险给小姑娘使用了一种原本用来治疗类风湿性关节炎的IL-6拮抗剂药物,才将小姑娘从死亡的边缘挽救回来。
CRS症状从轻微的流感样表现到危及生命的炎症反应综合征(SIRS),可出现低血压、血管通透性增加和多器官系统衰竭。ALL治疗的所有入组患者均表现出某种形式的CRS,其中27%的患者需要使用妥西珠单抗(tocilizumab,IL-6受体中和单抗)治疗。
01
实体瘤患者经CAR-T治疗后,可能导致“靶点”(on target, off tumor)毒性,因为某些组织也表达靶抗原而被攻击。在转移性结直肠腺癌患者的一期临床试验中,CAR-T发生了对抗癌胚抗原而引起的严重结肠炎。还有一名伴有肺和肝转移的病人,在注入CAR-T对抗ERBB2(人表皮生长因子受体2/neu)后的12小时内,出现呼吸窘迫和心脏骤停。五天后患者死亡。尸检分析发现,肺上皮细胞ERBB2低表达。因此考虑,患者死因就是CAR-T的靶点毒性,以及大量细胞因子释放导致的CRS。
02
细胞免疫疗法成功的两个主要因素
细胞免疫疗法要成功进入肿瘤组织的两个主要因素是:局部血流动力学和配体受体相互作用(如细胞表面粘附分子和趋化因子受体)。实体肿瘤的一个特点是组织液压力(IFP)高,某些肿瘤中可高达100mmHg。估计这源于新生血管的无序生长。IFP通常在肿瘤中心最高。宫颈癌患者IFP升高是复发和患者死亡的独立预测因子。由于CAR-T的动脉内灌注根据的是平均动脉压,那么那些IFP升高的肿瘤就会阻碍CAR-T细胞的到位。
受体-配体相互作用也影响CAR-T进入肿瘤组织。目前的临床前模型,试图用“T细胞归巢机制”来克服低效的CAR-T转运。Moon等人将CCR2趋化因子受体共转导为间皮素CAR-T,观察到T细胞在肿瘤中的渗透量增加了2.5倍,而没有CCR2受体表达的CAR-T灌注小鼠则无此现象。
03
固体瘤的CAR-T治疗
肝肿瘤的血液供应来自于肝动脉,而正常肝细胞血液供应主要来自于门静脉循环。因此,通过动脉就可以输送化疗药、放疗和化疗栓塞剂治疗肝肿瘤。在结直肠发生肝转移情况下,通过肝动脉灌注泵(HAIP)注入氟尿苷,联合全身化疗,应答率达75%,手术完全切除转化率接近50%。至于无法切除的肝细胞癌,则可以采用选择性钇90内放疗(Y90-SIRT)和经动脉化疗栓塞。这些经动脉入路增加了药物到达肿瘤的剂量,同时减少了全身毒性。
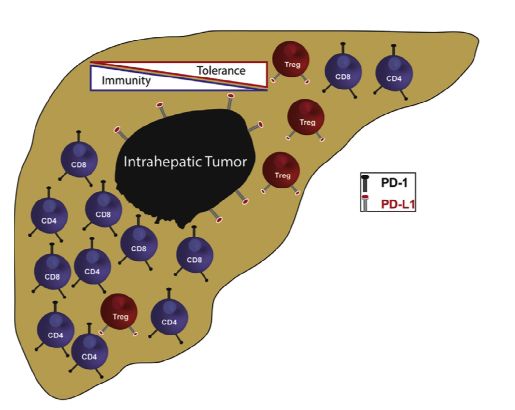
肝脏肿瘤渗透细胞技术(TIL,tumor infiltrating cells)。
左:大量T细胞渗透接近肝内肿瘤。通过高密度的细胞毒性CD8细胞,CD4细胞能杀伤肿瘤细胞。抑制性T细胞(Treg)很少。
右:不利于抗肿瘤的T细胞渗透。Treg对CD4和CD8细胞的比例增高,导致免疫耐受,影响肿瘤细胞清除。Treg和肿瘤细胞表面的PDL-1将与CD4和CD8 T细胞上的PD-1结合,抑制抗肿瘤免疫活性。
而一种Allogeneic white cell immunotherapy (AWIT)技术,显示无论在小鼠还是人类,都能将已发生的晚期固体瘤发生广泛坏死。AWIT耐受性好,副作用小,对晚期实体肿瘤具有抗肿瘤活性,代表了一种新颖、安全、有效的免疫疗法,可以在门诊癌症诊所使用。
在癌症的治疗上,也并不是CAR-T抢尽风头。溶瘤病毒(OVs)、癌症疫苗也让人刮目相看。
OVs是一种新型的抗癌药物,能直接杀灭癌细胞,同时刺激抗肿瘤免疫。
癌症疫苗也有不俗表现。去年7月份,美国达纳-法伯癌症研究所在同一期《自然》上背靠背发表了两项临床I期试验结果,显示针对黑色素瘤等肿瘤的个性化疫苗大放异彩。这是癌症疫苗首次在临床试验中取得成功。成果引起了全球范围内极大的轰动。
还不到一年的时间,个性化抗癌疫苗又在晚期卵巢癌上取得重大突破。对于这些回天乏术的病人,一旦T细胞被激活,两年生存率是100%;而那些没有被激活的患者,两年内只有25%。引人瞩目的是,CAR-T治疗领域的大牛Carl June和Bruce Levine教授也参与了该研究。
结语
1890年代,纪念斯隆-凯特琳癌症中心的外科医生William Bradley Coley(1862–1936 )在对癌症的常规治疗失去信心之后,开发了一种细菌疫苗,奇迹般地让肿瘤消退。
尽管他被学界称为“免疫治疗之父”,但当时放化疗的深入人心,在他有生之年,他也没能看到免疫疗法发扬光大。
现在,随着免疫治疗取得的一个个成果,以及规范的保驾护航,免疫治疗正在攻克癌症的道路上飞速跨越一道道障碍。“免疫治疗之父”为人类留下的巨大财富,在沉寂了大约百年之后,终于发出了耀眼的光芒,造福更多的患者。
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发