《Nature》子刊:脑子不够用?这种物质有助于逆转衰老,还你“年轻脑”
| 导读 | 近几年,衰老一直是人们热议的话题,人们在追求健康的同时,也越来越注重对长寿及抗衰老的探索。近日,来自英国剑桥大学的科学家们发现了一个有趣的现象:衰老会让脑组织变得僵硬,而这竟会影响大脑细胞的功能,进而发生大脑早衰。 |

作者:Paris
导 语:近几年,衰老一直是人们热议的话题,人们在追求健康的同时,也越来越注重对长寿及抗衰老的探索。现如今,衰老也不再是简简单单的生理现象,更多情况下它会引发某种身体疾病的发生,例如,糖尿病、心脑血管疾病、癌症等老年疾病的低龄化,恰恰是身体早衰老化的结果。
近日,来自英国剑桥大学(University of Cambridge)的科学家们发现了一个有趣的现象:衰老会让脑组织变得僵硬,而这竟会影响大脑细胞的功能,进而发生大脑早衰。相关文章以“Niche stiffness underlies the ageing of central nervous system progenitor cells”为题发表在《Nature》杂志上。

大脑是机体的指挥官,是一切生命活动的总指挥,脑衰则全身衰。曾有研究显示:胶质细胞与大脑衰老之间有着密不可分的联系,大脑和年轻大脑之间的差异主要在于一种被称作胶质细胞的支持细胞的存在。在本次研究中,一种称为OPC(少突胶质细胞)的胶质细胞引起了研究人员的注意,少突胶质细胞形成绝缘的髓鞘结构,能够协助髓鞘的再生,为神经元提供持续的营养支持及保护。研究发现,该细胞在年轻大脑及老年大脑中存在着明显的数量差异及功能差异。不仅如此,年轻大脑相比老年大脑而言,柔软得竟似海绵一样,大脑的僵硬程度会是这种差异存在的关键吗?那又怎样可以消除此种差异呢?
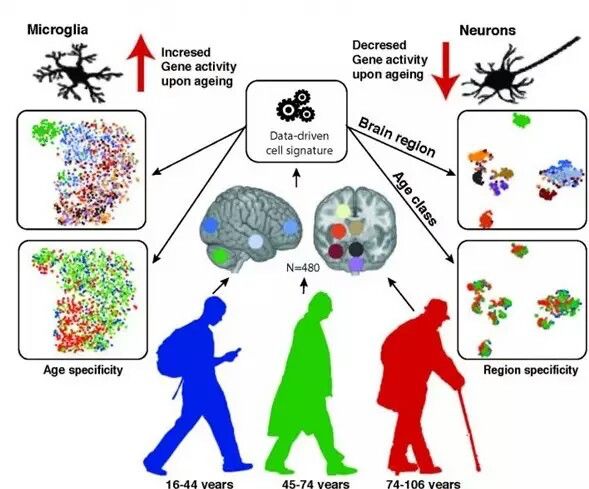
不同年龄层的脑胶质细胞分布
带着这一系列的疑问,研究人员开始了本次的研究,研究最初,他们从老年小鼠大脑中提取了少突胶质细胞并注入到年轻小鼠的大脑中,有趣的一幕出现了:这些少突胶质细胞竟重换活力,纷纷恢复了功能,比如,细胞增殖和分化的能力。研究人员不禁大胆猜测:或许,大脑周围环境是影响少突胶质细胞功能的关键。
为了验证以上假设,研究人员将老年小鼠的OPC分别放入含新生大鼠和老年大鼠的脱细胞神经细胞外基质的培养基中培养,结果发现,前者的OPC分化和增殖能力明显增强。这意味着,老年化可能损害了OPCs的功能。
紧接着,研究人员在实验室中开发了一种新材料,以便在受控环境中生长和研究大鼠的脑干细胞。巧妙的是,这些材料被设计成具有与年轻或老年大脑相似的柔软度。研究人员分别将新生小鼠和老年小鼠的OPCs放在软化的微环境和硬化的微环境中培养。结果,我们看到新生小鼠的大脑祖细胞生长在硬化的微环境里时,就会功能受损,失去再生的能力。而当老年小鼠的脑细胞生长在软化的微环境里时,它们会表现得和年轻细胞一样。换句话说,它们重返青春了。
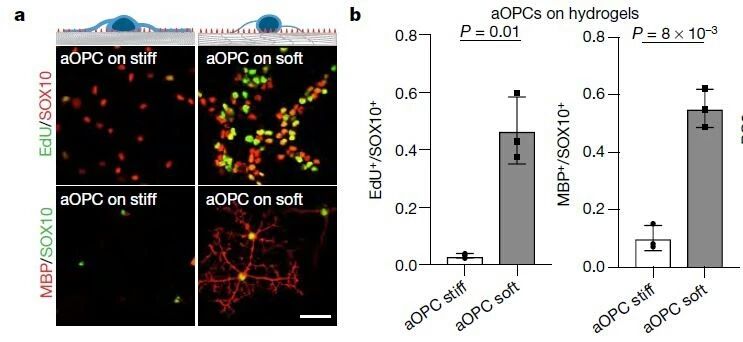
环境对OPC细胞的功能影响
实验进行的如此顺利,却一直存在着一个疑点:细胞是如何感知大脑周围环境的呢?一种叫做Piezo1的蛋白给了我们答案,这是一种可感知细胞周围的环境僵硬程度的蛋白质。在本次研究中,当我们在年老大脑的OPC细胞里敲除Piezo1蛋白后,即便是生长在硬化微环境中的老年小鼠,也保持着一定的功能,它们所感受的环境竟是柔软的,也就是说,失去了Piezo1蛋白,它们也失去了分辨能力。
如此看来,年龄相关的大脑微环境的硬化可能是OPCs功能衰退的主要原因,而微环境的改变则可能是成体干细胞衰老的主要原因。
从人类漫长的进化来看,我们会比人类史上任何时候的人都活得更长,人类或许都是第一次面临真正的衰老。而衰老的发生似乎也只是一瞬间的事情,由脑部衰老导致的神经退行性疾病对社会和医疗都是巨大的负担。本次研究揭示了大脑衰老的核心机制,为人类进一步对抗衰老提供了希望,也有望带来越来越多的“年轻脑”,让我们拭目以待!(转化医学网360zhyx.com)
参考文献
[1] Michael Segel, Björn Neumann, Niche stiffness underlies the ageing of central nervous system progenitor cells,Nature(2019).
[2]Giuseppe Lupo et al, Molecular profiling of aged neural progenitors identifies Dbx2 as a candidate regulator of age-associated neurogenic decline, Aging Cell (2018).

 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发