《Cell Reports》:双管齐下!铠甲加身的T细胞在免疫治疗领域所向披靡!
| 导读 | 近日,来自南卡罗来纳医科大学(MUSC)的研究小组在其最新发表在《Cell Reports》的研究中,通过抑制SphK1 / S1P途径的信号传导显著改善了T细胞免疫疗法的效率,铠甲上身,T细胞免疫疗法化身成全能战神,在癌症大军中所向披靡! |

作者:Paris
导语:近年来,Sphk-S1P-S1PR信号通路及其在炎症、肿瘤、动脉粥样硬化、自体免疫系统疾病、神经系统疾病等多种疾病中的作用越来越受到重视,其在多发性硬化症方面取得的突破更是给众多科学家以信心。
近日,受此启发,来自南卡罗来纳医科大学(MUSC)的研究小组在其最新发表在《Cell Reports》的研究中,通过抑制SphK1 / S1P途径的信号传导显著改善了T细胞免疫疗法的效率,铠甲上身,T细胞免疫疗法化身成全能战神,在癌症大军中所向披靡!

S1P是由鞘氨醇在鞘氨醇激酶(sphingosine kinase,SphK)的作用下生成的一种鞘脂类物质,通过介导S1P受体1(S1PR1)信号传导来调节淋巴细胞功能,并控制调节性T细胞(Tregs)的分化。
众所周知,调节性T细胞负向调节机体免疫反应,通过诱导和维持对自身抗原的耐受性来维持体内免疫平衡。肿瘤免疫抑制是肿瘤微环境的最重要特征之一,通过免疫抑制微环境,肿瘤细胞可以逃避机体免疫系统的识别和攻击,产生免疫逃逸。而在恶性肿瘤中,既往研究已经证实,调节性T细胞是其中重要的免疫抑制细胞。
那么,SIP是如何控制调节性T细胞的分化呢?SphK1在其中又扮演着怎样的角色呢?
已知三种不同的信号通路通过影响SphK1 / S1P途径参与T细胞的代谢:其一是细胞因子白细胞介素-15(IL-15),它能够促进中枢记忆样T细胞(Tcm)杀死机体有害细胞;其二是转化生长因子β(TGF-β),它可以推动T细胞分化为调节性T细胞(Tregs);其三是过氧化物酶体增殖物激活受体γ(PPARγ),其通过调节脂质代谢来向T细胞提供能量。
为了评估SphK1 / S1P途径对T细胞的影响,实验之初,研究人员使用化学药物抑制了SphK1的功能,不仅消耗了S1P的水平,还促进了Tcm细胞的表达,Tcm细胞是免疫应答中的上游细胞,它能起到纽带作用,免疫系统识别肿瘤抗原之后,Tcm负责长久记忆肿瘤抗原,并在肿瘤抗原刺激下源源不断地产生针对肿瘤的大量Tem(效应型记忆T细胞),进而分化成为大量的效应T细胞——强有力的杀伤肿瘤细胞。
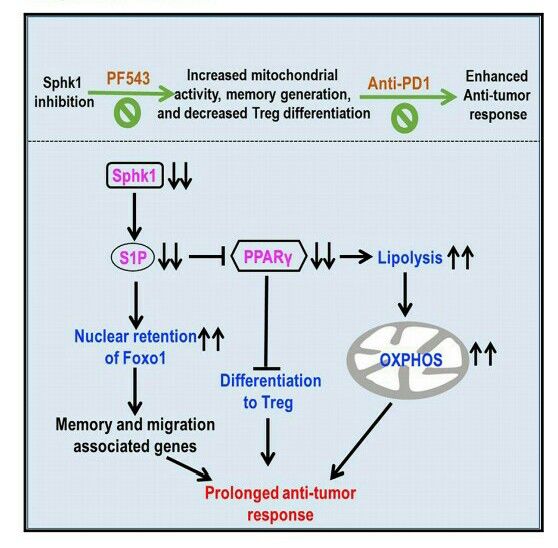
抑制Sphk1在T细胞免疫疗法中的影响
如此看来,通过抑制SphK1便能显著改善T细胞免疫治疗效果。当然,结果不是一蹴而就的,过程才是真正的魅力所在,这三种信号通路在本次研究中又如何发挥作用呢?
进一步探索发现,IL-15通过抑制SphK1和S1P表达Tcm表型,S1P水平的消耗增加了一种转录因子--TGF-β的活性,该转录因子诱导与记忆表型相关的基因表达。此外,S1P的缺失还降低了PPARγ的活性,从而阻止了T细胞分化为Tregs,并大大提高了脂质代谢的利用率。综上,这三种通路通力合作,协同调控T细胞功能。
Mehrotra教授表示:机体始终处于动态平衡中,为了对抗癌细胞,我们需要打破这种平衡,让T细胞过度活跃起来。
有趣的是,S1P在癌细胞中高水平表达,使癌细胞更好地适应周围环境,这恰恰是癌细胞的狡猾之处,大大影响了T细胞靶向癌细胞的能力。综上所述,抑制SphK1 / S1P具有双管齐下的功能,既抑制癌细胞存活又促进Tcm细胞的过度表达。
常见的癌症治疗通常以化疗为主,化疗不仅可以靶向并杀死癌细胞,还可以杀死免疫细胞。而靶向SphK1允许免疫细胞粘附以靶向并杀死癌细胞。这为癌症治疗开辟了新的格局。此外,Mehrotra教授和Ogretmen教授还发现,使用一种名为PD1的药物与抑制SphK1的化合物联合的新疗法能大大提高T细胞肿瘤杀伤力。
这项研究开创了癌症免疫疗法新领域,未来的工作旨在验证这一途径在几个临床前癌症模型的效果。(转化医学网360zhyx.com)
参考文献
Paramita Chakraborty,1 Silvia G. Vaena,2 Krishnamurthy Thyagarajan Pro-Survival Lipid Sphingosine-1-Phosphate Metabolically Programs T Cells to Limit Anti-tumor Activity
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发