白蛋白长出了“利爪”,死扣肿瘤基质!抗肿瘤药物成功累积
| 导读 | 抗肿瘤靶向给药系统是肿瘤靶向治疗的重要组成部分,血清白蛋白(SA)因其低免疫反应、组织相容性好等特点被当作理想的药物输送载体,但SA主要靠被动靶向输送药物,导致药物难以在肿瘤组织中累积,严重限制了该药物传递系统的应用。 |
导读:抗肿瘤靶向给药系统是肿瘤靶向治疗的重要组成部分,血清白蛋白(SA)因其低免疫反应、组织相容性好等特点被当作理想的药物输送载体,但SA主要靠被动靶向输送药物,导致药物难以在肿瘤组织中累积,严重限制了该药物传递系统的应用。
近日,芝加哥大学的研究人员对SA进行了改造,结合了主动靶向和被动靶向作用,将SA携带的抗肿瘤药物长时间保留于肿瘤组织中。他们让SA长出了“利爪”,紧紧“抓”住了肿瘤,让肿瘤组织中抗肿瘤药物大量累积,显著提高了肿瘤治疗效果!

靶向治疗——那些化被动为主动才能解决的难题
SA是血液中含量最丰富的蛋白,半衰期长且具有运输药物的功能,是疏水性分子体内输送的天然载体,以SA为材料制备的纳米药物载体载药量高、毒副作用小,并具有一定的肿瘤靶向性,是优异的药物输送载体。但是,传统SA制剂多为被动靶向制剂,只能利用特定组织、器官的生理结构特点,使药物在体内产生自然的分布差异来实现靶向效应。这就意味着其靶向性不高,抗肿瘤药物难以在肿瘤组织中最大限度累积,而药物副作用也成为了必须解决的一大难题。
既然靠环境差异决定的被动靶向难以满足需求,那自然要让SA制剂“主动”找到肿瘤组织了,这就是另一种重要的靶向作用——主动靶向。
主动靶向可将抗体、多肽、糖链、核酸适配体等能够与靶标分子特异性结合的探针分子通过化学或物理方法偶联到药物或其载体表面,进而赋予药物或其载体主动与靶标结合的能力。简单点说,主动靶向就是为抗癌制剂装上了“利爪”,让其牢牢“抓住”肿瘤组织,进而保证抗癌药物在肿瘤组织中最大限度聚集。
血管假性血友病因子胶原结合域(CBD)——SA长出的“利爪”
研究人员选择了CBD作为SA制剂的“利爪”。他们将SA与CBD重组融合得到CBD-SA,使SA在肿瘤血管外渗后与肿瘤基质中的胶原结合,同时保留了SA的被动靶向能力,双重作用将复合物紧紧固定于肿瘤组织中,提高了SA的肿瘤靶向能力和药物治疗作用。
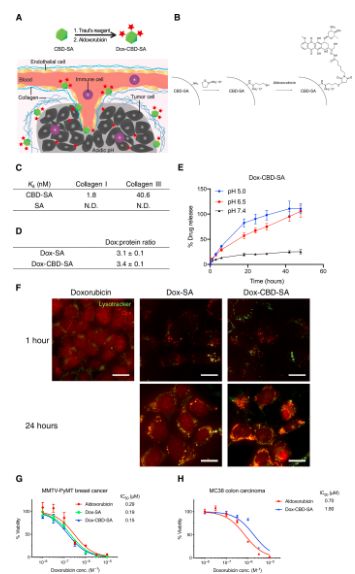
Dox-CBD-SA的合成和表征
进一步的药物实验中,研究人员将多柔比星(Dox)与CBD-SA缀合物偶联,发现在乳腺癌小鼠模型中,与Dox-SA和Dox相比,Dox-CBD-SA可显著抑制乳腺癌的生长。另一方面,Dox-CBD-SA还可增强肿瘤组织中的淋巴细胞浸润,有效刺激了宿主抗肿瘤免疫反应。
不仅如此,他们还发现淋巴细胞,特别是CD8 +细胞毒性T细胞的增强浸润可能有助于Dox-CBD-SA抗肿瘤作用的提高。而且,Dox-CBD-SA还显著降低了靶向治疗的不良反应!更令人惊喜的是,将Dox-CBD-SA与抗PD-1抗体组合应用于MC38结肠癌后,肿瘤细胞株被彻底消除,这实现了显示出等效剂量的Dox+αPD-1无法实现的进一步抗肿瘤作用!
这项研究开发了一种新型肿瘤药物递送系统,CBD的加入提供了 SA的主动靶向能力,实现了SA两种靶向功能的同时启动,最大限度保证了肿瘤组织中的抗肿瘤药物浓度,对各类肿瘤皆具有适用性。这也为更多抗肿瘤药物发挥最大作用提供了更多可能性。(转化医学网360zhyx.com)
参考文献:
Koichi Sasaki,et al.Engineered collagen-binding serum albumin as a drug conjugate carrier for cancer therapy.Science Advances 14 Aug 2019.
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发