【研究】通过测序和荧光原位杂交(FISH)数据评估肿瘤异质性
| 导读 | 癌症中克隆进化的计算重建已成为了解肿瘤如何开始和进展以及该过程在患者之间如何变化的关键工具。然而,该领域仍在努力发展,面临着将系统进化方法应用于癌症的特殊挑战,例如拷贝数改变(CNA)和结构变异(SV)事件在肿瘤进化中的普遍性和重要性,而这些问题很难通过主流测序准确地描述出来。 |
导读:癌症中克隆进化的计算重建已成为了解肿瘤如何开始和进展以及该过程在患者之间如何变化的关键工具。然而,该领域仍在努力发展,面临着将系统进化方法应用于癌症的特殊挑战,例如拷贝数改变(CNA)和结构变异(SV)事件在肿瘤进化中的普遍性和重要性,而这些问题很难通过主流测序准确地描述出来。
克隆系统发生学的方法引起了计算生物学界的极大兴趣,特别是随着该领域对肿瘤进化机制的复杂性以及从可用基因组数据中重建它们的算法挑战有了更深入的了解。在这方面,最近感兴趣的一个特定领域是开发更好的方法,以通过拷贝数改变(CNA)和产生它们的结构变异(SV)解决进化。尽管人们早已知道CNA和SVs在癌症中的重要性,并且一些克隆世系重建的首批方法集中在CNA驱动的进化上,但历史上许多肿瘤系统发生领域都集中在单核苷酸变异(SNV)上,而省略了CNA,或在很大程度上被视为推论SNV驱动的进化的混杂因素。迄今为止,为了推论CNA的肿瘤进化,目前已经建立了相对较少的计算方法,或者单独或与SNV联合,直到最近,才出现了更广泛地捕获SV进化的方法。然而,同时的生物学证据强烈表明,CNV和产生它们的SV在预测治疗反应方面优于SNV和其他局灶性变化,并且很可能是肿瘤发展的主要机制,并在功能上适应于逃避控制细胞生长。
CNA驱动的进化相对于SNV驱动的进化产生了很多复杂性。在某种程度上,对CNA进行建模是一个挑战,因为它在系统发育学中一般是较少被研究的一种机制,因此需要算法上的创新。在某种程度上,这是个挑战,因为CNA会造成特殊的复杂性,它们可能会在多个尺度上发生,有时会出现难以解决的重叠变化。对于系统进化学的反卷积方法,CNA也特别具有挑战性其中涉及从整体序列中计算分离出克隆混合物数据的缺乏,由于缺乏具有单细胞数据的大型队列,因此仍然是该领域的必要条件——因为在没有附加数据或问题约束的情况下,未充分确定CNA的基本反卷积问题。CNA方法还特别难以处理倍性变化,尤其是通过全基因组复制(WGD)处理,因为倍数性很难仅从序列数据中准确推断出来。尽管最近的方法表明可以使用多区域批量测序或单细胞测序进行准确的CNA构建,但这些方法需要有限的假设,例如,WGD在肿瘤的病史中只能发生一次。此外,大型群组仍然缺少多区域批量或单细胞测序的方法,并且仍然存在一个悬而未决的问题,如何最好地进行大规模肿瘤基因组研究将为克隆CNA的进化提供信息。
准确重建肿瘤演变倍性变化过程的问题令人担忧,部分原因是WGD现在被认为是一种侵袭性癌症的病理标志,但该观察结果缺乏明确的生物逻辑机制。WGD在肿瘤进化中的早期模型提出了一个早期的WGD事件作为染色体发生肿瘤的前提不稳定的癌症现在被认为过于简单,因为WGD在癌症的演变过程中既没有必要,也不一定是一次性事件。相反,可以将WGD视为对不同基因有活性的许多突变类型之一不同癌症的癌症程度,塑造可能的轨迹和患者特定各种进展过程的风险。
本工作开发了提高我们解决CNA-能力的方法遵循多组数据集成策略,推动癌症的进化。Malicik等人展示了整合大容量和单细胞数据用于改进SNV进化模型,这是我们之前的策略也证明了CNA驱动的进化也很成功。在这里,我们探索引入其他形式的数据的潜力,多相相流原位杂交(miFISH),提供了一种分析肿瘤的方法少量探针的单细胞进化纯倍体成为纯序列研究的一个挑战。而miFISH限制每个细胞一个到几个拷贝数标记,其易于扩展大量细胞使其成为CNV肿瘤系统发育的有力工具尤其是在将FISH探针策略性地放置在基因座上时在感兴趣的肿瘤类型中反复扩增。
在这里,我们开发了一种将批量序列与单个细胞序列(SCS)和/或miFISH,以结合各自的优势单拷贝数进化改进重建技术细胞水平。我们用半模拟数据显示这两种数据以独特和协同的方式做出贡献,以更准确地推断CNA-驱动进化,尤其是在非整倍体肿瘤中,并证明了它们的实用性通过批量,SCS和miFISH分析胶质母细胞瘤的价值。一起,这项工作证明了将miFISH或相关方法用于如果要进行基于序列的肿瘤系统发育研究的细胞计数分析准确重建CNA驱动的癌症进化机制。
1.估算F(约束|| B ? CP F || 1,约束F)
2.估算S(约束J(S,C,C0),系统发生成本)
3.估算C(约束C,约束 ||XTCP ? H0||1)
4.估算P(约束P,约束 ||XTCP ? H0||1)
5.胶质母细胞瘤数据
6.模拟数据
其中生成六个数据结构:
①~C:所有选定克隆的归一化拷贝数图谱的矩阵,使用组成大量肿瘤数据②?:~C中主要克隆的归一化拷贝数图的矩阵,使用评估表现③?P:所有选定克隆的半倍性对角矩阵
④?P:主要克隆的半倍体的对角矩阵
⑤?F:每个区域中所有选定克隆的混合级分的矩阵⑥?F:每个区域中主要克隆的混合部分的矩阵
这里描述的工作为进一步研究提供了许多途径。我们方法的局限性在于,目前很少有肿瘤能被这里讨论的技术组合研究到。我们建议在序列与miFISH配对的情况下进行进一步研究,或者提供类似能力来估计倍性和/或克隆的替代方法频率更准确,尤其是对于了解癌症的演变类型容易发生染色体不稳定和非整倍性。第二,目前的工作就像我们之前的工作一样,表明了一种准确的单细胞系统发育模型在改善解卷积中的价值。准确重建进化论即使具有已知的单细胞数据,拷贝数空间中的树仍然是一个挑战烦人的问题。虽然有先验的理论来重建拷贝数进化,没有模型可用于CNA的所有机制我们了解的进化过程以及开发规模化的综合模型能够处理大型单细胞的全基因组数据仍然是一个挑战。也有许多其他替代技术可能会纳入多组学数据以改善系统发育推断。在其他工作中,可能会为目前的问题。此外,可能还有改善的空间解决我们工作的核心优化问题。
参考文献:Haoyun Lei,et al. Tumor heterogeneity assessed by sequencing and fluorescence in situ hybridization (FISH) data. BioRxiv. 29 Feb,2020.
通过系统发育推断算法进行的后续重建是准确的。因此,本文开发了将测序与多重相间荧光原位杂交(miFISH)相结合的计算方法,以利用每种技术的互补优势,推断出在全基因组规模上考虑了局部改变和非整倍性的准确的克隆CNA进化模型。

克隆系统发生学的方法引起了计算生物学界的极大兴趣,特别是随着该领域对肿瘤进化机制的复杂性以及从可用基因组数据中重建它们的算法挑战有了更深入的了解。在这方面,最近感兴趣的一个特定领域是开发更好的方法,以通过拷贝数改变(CNA)和产生它们的结构变异(SV)解决进化。尽管人们早已知道CNA和SVs在癌症中的重要性,并且一些克隆世系重建的首批方法集中在CNA驱动的进化上,但历史上许多肿瘤系统发生领域都集中在单核苷酸变异(SNV)上,而省略了CNA,或在很大程度上被视为推论SNV驱动的进化的混杂因素。迄今为止,为了推论CNA的肿瘤进化,目前已经建立了相对较少的计算方法,或者单独或与SNV联合,直到最近,才出现了更广泛地捕获SV进化的方法。然而,同时的生物学证据强烈表明,CNV和产生它们的SV在预测治疗反应方面优于SNV和其他局灶性变化,并且很可能是肿瘤发展的主要机制,并在功能上适应于逃避控制细胞生长。
CNA驱动的进化相对于SNV驱动的进化产生了很多复杂性。在某种程度上,对CNA进行建模是一个挑战,因为它在系统发育学中一般是较少被研究的一种机制,因此需要算法上的创新。在某种程度上,这是个挑战,因为CNA会造成特殊的复杂性,它们可能会在多个尺度上发生,有时会出现难以解决的重叠变化。对于系统进化学的反卷积方法,CNA也特别具有挑战性其中涉及从整体序列中计算分离出克隆混合物数据的缺乏,由于缺乏具有单细胞数据的大型队列,因此仍然是该领域的必要条件——因为在没有附加数据或问题约束的情况下,未充分确定CNA的基本反卷积问题。CNA方法还特别难以处理倍性变化,尤其是通过全基因组复制(WGD)处理,因为倍数性很难仅从序列数据中准确推断出来。尽管最近的方法表明可以使用多区域批量测序或单细胞测序进行准确的CNA构建,但这些方法需要有限的假设,例如,WGD在肿瘤的病史中只能发生一次。此外,大型群组仍然缺少多区域批量或单细胞测序的方法,并且仍然存在一个悬而未决的问题,如何最好地进行大规模肿瘤基因组研究将为克隆CNA的进化提供信息。
准确重建肿瘤演变倍性变化过程的问题令人担忧,部分原因是WGD现在被认为是一种侵袭性癌症的病理标志,但该观察结果缺乏明确的生物逻辑机制。WGD在肿瘤进化中的早期模型提出了一个早期的WGD事件作为染色体发生肿瘤的前提不稳定的癌症现在被认为过于简单,因为WGD在癌症的演变过程中既没有必要,也不一定是一次性事件。相反,可以将WGD视为对不同基因有活性的许多突变类型之一不同癌症的癌症程度,塑造可能的轨迹和患者特定各种进展过程的风险。
本工作开发了提高我们解决CNA-能力的方法遵循多组数据集成策略,推动癌症的进化。Malicik等人展示了整合大容量和单细胞数据用于改进SNV进化模型,这是我们之前的策略也证明了CNA驱动的进化也很成功。在这里,我们探索引入其他形式的数据的潜力,多相相流原位杂交(miFISH),提供了一种分析肿瘤的方法少量探针的单细胞进化纯倍体成为纯序列研究的一个挑战。而miFISH限制每个细胞一个到几个拷贝数标记,其易于扩展大量细胞使其成为CNV肿瘤系统发育的有力工具尤其是在将FISH探针策略性地放置在基因座上时在感兴趣的肿瘤类型中反复扩增。
在这里,我们开发了一种将批量序列与单个细胞序列(SCS)和/或miFISH,以结合各自的优势单拷贝数进化改进重建技术细胞水平。我们用半模拟数据显示这两种数据以独特和协同的方式做出贡献,以更准确地推断CNA-驱动进化,尤其是在非整倍体肿瘤中,并证明了它们的实用性通过批量,SCS和miFISH分析胶质母细胞瘤的价值。一起,这项工作证明了将miFISH或相关方法用于如果要进行基于序列的肿瘤系统发育研究的细胞计数分析准确重建CNA驱动的癌症进化机制。
其中,我们选择了一种目标函数:
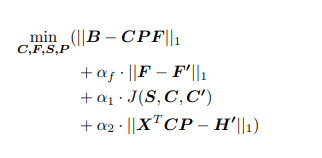
1.估算F(约束|| B ? CP F || 1,约束F)
2.估算S(约束J(S,C,C0),系统发生成本)
3.估算C(约束C,约束 ||XTCP ? H0||1)
4.估算P(约束P,约束 ||XTCP ? H0||1)
5.胶质母细胞瘤数据
6.模拟数据
其中生成六个数据结构:
①~C:所有选定克隆的归一化拷贝数图谱的矩阵,使用组成大量肿瘤数据②?:~C中主要克隆的归一化拷贝数图的矩阵,使用评估表现③?P:所有选定克隆的半倍性对角矩阵
④?P:主要克隆的半倍体的对角矩阵
⑤?F:每个区域中所有选定克隆的混合级分的矩阵⑥?F:每个区域中主要克隆的混合部分的矩阵
结果分为模拟数的评估和世纪GBM数据,前者分析了是否有倍数变化有倍性变化,后者如图显示 :

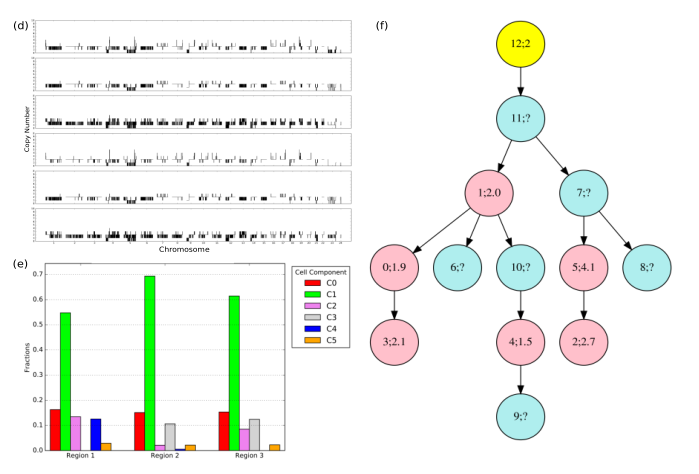
图为在实际GBM07((a)-(c))和GBM33((d)-(f))情况下的应用。
(a)(d)推断细胞成分C0(顶部)到C5(底部)中每个染色体的拷贝数,轴表示染色体,1-22表示常染色体,23表示X染色体24代表Y染色体。(b)(e)每个推论的相应分数细胞成分。(c)(f)观察到的细胞组成之间的系统发育关系-nents(粉红色)和推断的单元格成分(浅蓝色)。
我们已经扩展了肿瘤系统发生方法,以结合拷贝数测量除大量和单细胞序列数据外,还可通过DNA-FISH进行检测更精确地测量肿瘤倍性和克隆频率的来源。结果表明,每种数据源分别有助于获得更多的收益。结合所有这些因素,对癌症中拷贝数演变的准确描述三种数据类型提高了全基因组拷贝解析的准确性数字配置文件。我们通过对一对胶质母细胞瘤病例的应用证明新方法可以提供关于拷贝数进化作用的新颖见解单一癌症中的溶解。结果表明补充序列的价值数据与其他数据源(例如miFISH)一起准确重建CNA机制在肿瘤中表现出的染色体不稳定性。这里描述的工作为进一步研究提供了许多途径。我们方法的局限性在于,目前很少有肿瘤能被这里讨论的技术组合研究到。我们建议在序列与miFISH配对的情况下进行进一步研究,或者提供类似能力来估计倍性和/或克隆的替代方法频率更准确,尤其是对于了解癌症的演变类型容易发生染色体不稳定和非整倍性。第二,目前的工作就像我们之前的工作一样,表明了一种准确的单细胞系统发育模型在改善解卷积中的价值。准确重建进化论即使具有已知的单细胞数据,拷贝数空间中的树仍然是一个挑战烦人的问题。虽然有先验的理论来重建拷贝数进化,没有模型可用于CNA的所有机制我们了解的进化过程以及开发规模化的综合模型能够处理大型单细胞的全基因组数据仍然是一个挑战。也有许多其他替代技术可能会纳入多组学数据以改善系统发育推断。在其他工作中,可能会为目前的问题。此外,可能还有改善的空间解决我们工作的核心优化问题。
参考文献:Haoyun Lei,et al. Tumor heterogeneity assessed by sequencing and fluorescence in situ hybridization (FISH) data. BioRxiv. 29 Feb,2020.
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发