【Science Advances】对癌症递送纳米颗粒治疗的最佳方法是什么?
| 导读 | 虽然免疫治疗在对抗癌症方面有很大的希望,但由于免疫抑制肿瘤微环境和全身毒性的限制,其疗效有限,因此阻碍了癌症免疫治疗的广泛应用。纳米颗粒为癌症治疗和诊断提供了独特的机遇和挑战。尤其在精确定位癌细胞方面,纳米颗粒改进了目前传统的癌症治疗方式,旨在减轻患者痛苦。 |
近日,约翰霍普金斯金梅尔癌症中心的研究人员对小鼠和人类的肿瘤进行了一项新研究。研究结果“在乳腺癌模型中纳米颗粒与免疫细胞的相互作用决定了肿瘤的保留并诱导了T细胞介导的肿瘤抑制”,发表在《科学进展》杂志上。研究人员得出结论,宿主的免疫状态和实体瘤的微环境是癌症纳米医学研究的关键变量,纳米颗粒技术可能具有癌症免疫疗法的潜力。
全身性地暴露于两种纳米颗粒类型均会导致免疫反应,导致CD8 + T细胞浸润和肿瘤生长延迟,而与抗体治疗活性无关。这些结果表明,通过全身性暴露于纳米颗粒可以诱导抗肿瘤免疫反应,而无需治疗有效载荷。
约翰霍普金斯大学的西德尼·金梅尔综合癌症中心放射线学和分子放射科学副教授罗伯特·伊夫科夫(Robert Ivkov)博士解释说,很长一段时间以来,纳米粒子注射到血液中后会被类似清除剂的巨噬细胞和其他免疫系统细胞吸收。该领域的许多研究人员一直致力于减少与免疫细胞的相互作用,因为他们一直在努力增加纳米颗粒的循环时间及其在肿瘤细胞中的保留。但研究表明,肿瘤中的免疫细胞以刺激抗癌反应的方式聚集并与颗粒反应。这可能具有超越药物递送而发展癌症免疫疗法的潜力。
研究人员在他们的研究中进行了一些体外实验。首先,他们将一些普通的淀粉包覆的氧化铁纳米粒子和其他用曲妥珠单抗包覆的纳米颗粒应用于五种人类乳腺癌细胞系,发现曲妥珠单抗包覆的纳米粒子与细胞之间的结合量取决于癌细胞表达癌基因HER2的程度。在人类中,HER2阳性乳腺癌是对标准化学疗法最有抵抗力的癌症。
曲妥珠单抗(以赫赛汀(Herceptin)名称出售)靶向HER2阳性肿瘤细胞并触发免疫系统。
研究人员报告说,在动物模型中,反应也出奇地不同。在另外的实验中,研究小组在植入了五种人类乳腺癌细胞系的两种免疫缺陷小鼠中使用了纳米颗粒,其中两种细胞是HER2阴性的,而三种是HER2阳性的。当他们在24小时后研究动物的肿瘤时,发现在所有类型的肿瘤中,无论它们是否表达HER2蛋白,都涂有曲妥珠单抗的纳米颗粒的浓度是普通纳米颗粒的2至5倍。他们还发现,在具有完全功能的免疫系统并带有小鼠衍生肿瘤的小鼠中,曲妥珠单抗包被的纳米颗粒的数量甚至更高(高达十倍)。
这导致研究人员怀疑宿主动物的免疫系统是否与纳米颗粒强烈相互作用,并在确定是否将颗粒保留在肿瘤中中发挥作用,无论是否添加药物都是这样。
研究小组报告说,更多的实验表明,与肿瘤相关的免疫细胞负责收集纳米颗粒,与免疫功能不完全的小鼠相比,具有完整免疫系统的小鼠保留了更多的曲妥珠单抗包被的纳米颗粒。
此外,肿瘤周围环境或微环境中的炎性免疫细胞比普通纳米颗粒更多地捕获了包覆纳米颗粒。最后,在一系列为期30天的实验中,研究人员发现,暴露于纳米颗粒比对照组抑制肿瘤生长的速度是对照组的三至五倍,并增加了肿瘤中CD8阳性的杀死癌症的T细胞的数量。
暴露于普通或曲妥珠单抗涂层的纳米颗粒,抗癌免疫激活反应同样有效。T细胞缺陷的小鼠没有显示出肿瘤生长抑制作用。研究人员说,这表明全身性暴露于纳米颗粒可以引起全身性宿主免疫反应,从而导致抗癌免疫刺激,并且不需要纳米颗粒进入肿瘤内部。

癌症纳米医学界的科学家们进行了讨论,使用纳米颗粒是否可以最好地给肿瘤被动递送药物治疗,从而使纳米颗粒扩散到肿瘤中并固定在原位,或者主动添加靶向的抗癌分子与特定的癌细胞受体结合。从理论上讲,这可以使纳米颗粒在肿瘤中的保留时间更长。
实验室研究在6种乳腺癌模型中测试了这两种方法;在五种人类肿瘤细胞系和一种具有三种免疫系统变体的小鼠癌症,发现涂有曲妥珠单抗(针对人表皮生长因子受体2(HER2)阳性乳腺癌细胞的药物)的纳米颗粒,相比普通纳米颗粒,可以更好地保留在肿瘤中,甚至在不表达促生长HER2蛋白的肿瘤中也是如此。然而,暴露于纳米颗粒的宿主的免疫细胞通过激活侵袭并减慢肿瘤生长的T细胞,诱导了抗癌免疫反应。
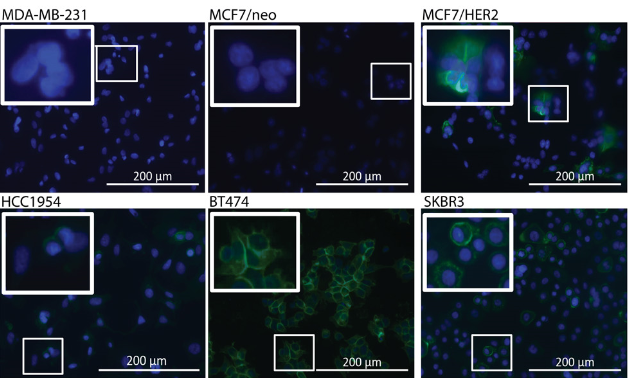
免疫荧光结果显示HER2蛋白在六个人乳腺癌细胞系中的表面表达。
全身递送后影响体内纳米颗粒命运的因素仍然是人们关注的领域。特别令人感兴趣的是,用癌症特异性抗体配体(“主动靶向”)标记是否优于未标记的对应物(“被动靶向”)。研究人员使用三种小鼠免疫变体中的乳腺癌模型,证明了抗体标记的纳米颗粒在肿瘤内的保留是由肿瘤相关的细胞(树突状细胞、嗜中性粒细胞,单核细胞和巨噬细胞)决定的,而不是由抗原抗体反应的相互作用决定的。全身性地暴露于两种纳米颗粒类型均会导致免疫反应,导致CD8 + T细胞浸润和肿瘤生长延迟,而与抗体治疗活性无关。这些结果表明,通过全身性暴露于纳米颗粒可以诱导抗肿瘤免疫反应,而无需治疗有效载荷。
约翰霍普金斯大学的西德尼·金梅尔综合癌症中心放射线学和分子放射科学副教授罗伯特·伊夫科夫(Robert Ivkov)博士解释说,很长一段时间以来,纳米粒子注射到血液中后会被类似清除剂的巨噬细胞和其他免疫系统细胞吸收。该领域的许多研究人员一直致力于减少与免疫细胞的相互作用,因为他们一直在努力增加纳米颗粒的循环时间及其在肿瘤细胞中的保留。但研究表明,肿瘤中的免疫细胞以刺激抗癌反应的方式聚集并与颗粒反应。这可能具有超越药物递送而发展癌症免疫疗法的潜力。
研究人员在他们的研究中进行了一些体外实验。首先,他们将一些普通的淀粉包覆的氧化铁纳米粒子和其他用曲妥珠单抗包覆的纳米颗粒应用于五种人类乳腺癌细胞系,发现曲妥珠单抗包覆的纳米粒子与细胞之间的结合量取决于癌细胞表达癌基因HER2的程度。在人类中,HER2阳性乳腺癌是对标准化学疗法最有抵抗力的癌症。
曲妥珠单抗(以赫赛汀(Herceptin)名称出售)靶向HER2阳性肿瘤细胞并触发免疫系统。
研究人员报告说,在动物模型中,反应也出奇地不同。在另外的实验中,研究小组在植入了五种人类乳腺癌细胞系的两种免疫缺陷小鼠中使用了纳米颗粒,其中两种细胞是HER2阴性的,而三种是HER2阳性的。当他们在24小时后研究动物的肿瘤时,发现在所有类型的肿瘤中,无论它们是否表达HER2蛋白,都涂有曲妥珠单抗的纳米颗粒的浓度是普通纳米颗粒的2至5倍。他们还发现,在具有完全功能的免疫系统并带有小鼠衍生肿瘤的小鼠中,曲妥珠单抗包被的纳米颗粒的数量甚至更高(高达十倍)。
这导致研究人员怀疑宿主动物的免疫系统是否与纳米颗粒强烈相互作用,并在确定是否将颗粒保留在肿瘤中中发挥作用,无论是否添加药物都是这样。
研究小组报告说,更多的实验表明,与肿瘤相关的免疫细胞负责收集纳米颗粒,与免疫功能不完全的小鼠相比,具有完整免疫系统的小鼠保留了更多的曲妥珠单抗包被的纳米颗粒。
此外,肿瘤周围环境或微环境中的炎性免疫细胞比普通纳米颗粒更多地捕获了包覆纳米颗粒。最后,在一系列为期30天的实验中,研究人员发现,暴露于纳米颗粒比对照组抑制肿瘤生长的速度是对照组的三至五倍,并增加了肿瘤中CD8阳性的杀死癌症的T细胞的数量。
暴露于普通或曲妥珠单抗涂层的纳米颗粒,抗癌免疫激活反应同样有效。T细胞缺陷的小鼠没有显示出肿瘤生长抑制作用。研究人员说,这表明全身性暴露于纳米颗粒可以引起全身性宿主免疫反应,从而导致抗癌免疫刺激,并且不需要纳米颗粒进入肿瘤内部。
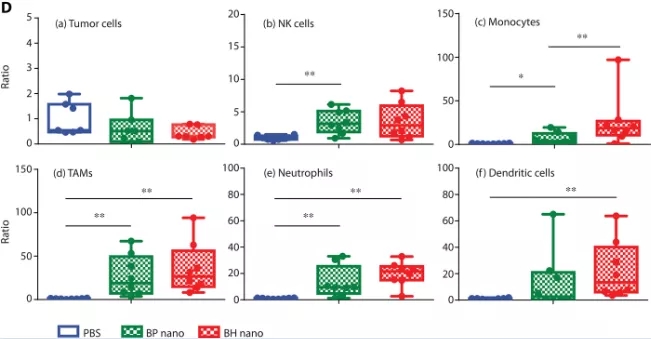
从体内肿瘤获得的磁性分选细胞的分析表明,纳米颗粒与免疫细胞相关,而不与肿瘤细胞相关。
总之,研究表明宿主与肿瘤对纳米颗粒暴露的免疫反应之间存在复杂的相互依赖性。这些结果为探索纳米粒子“靶向”肿瘤免疫微环境提供了可能性。同时还展示出开发纳米颗粒作为癌症免疫疗法的平台的新潜力。研究人员还计划研究非癌症疾病(例如传染病)是否可以产生相同类型的免疫反应。
参考:[1]https://www.genengnews.com/news/what-might-be-the-best-way-to-delivery-nanoparticle-therapy-for-cancer/[2]Robert Ivkov et al. Nanoparticle interactions with immune cells dominate tumor retention and induce T cell–mediated tumor suppression in models of breast cancer. Science Advances. 25 March, 2020.
(转化医学网360zhyx.com)
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发