《循环肿瘤细胞检测在结直肠癌中的应用专家共识》解读
| 导读 | 《循环肿瘤细胞检测在结直肠癌中的应用专家共识》解读 |

《2020年全球最新癌症负担》数据显示,在全世界范围内结直肠癌(Colorectal cancer, CRC)发病率排名第三(193万),死亡率第二(94万),而在中国结直肠癌的发病率排名第二(56万),死亡率第五(29万),结直肠癌已经对人类健康造成严重的威胁。随着手术、放化疗及靶向治疗等综合治疗手段的应用,CRC患者的预后得到有效改善。但目前,仍有一半以上患者在疾病进展过程中会出现肿瘤复发、远处转移,并最终导致死亡。对于如何有效监测疾病进展并准确判断预后,一直是CRC研究领域的热点和难点。
循环肿瘤细胞(Circulating tumor cells,CTCs)检测作为液体活检的主要代表,相较传统组织学活检,具有创伤小、可重复检测、敏感性及特异性高等优势,可提供关于CRC患者疾病状态的实时信息,有助于CRC的早期筛查、预后评估及治疗反应监测等。众多国内外权威研究证实CTCs可动态监测结直肠癌的进展状态。

肿瘤治疗过程CTC、血清标志物及影像学检测结果[1]
CTCs可作为结直肠癌化疗结果的预测生物标志物,化疗前后CTCs数量的变化可预测治疗效果。治疗后CTCs数量变化比影像学、血清标志物CEA和CA19-9,能更早地预测治疗效果。
现阶段循环肿瘤细胞检测应用于临床,仍面临一系列亟待解决的问题。因此,中国研究型医院学会微创外科学专业委员会组织多位临床专家共同讨论编写了《循环肿瘤细胞检测在结直肠癌中的应用专家共识》[2]。《共识》主要包括CTCs的定义及特性,CTCs的检测技术,CTCs的检测流程,CTCs的临床意义等内容。对CTCs进行了详细的介绍,并结合临床研究数据,探讨了CTCs在临床上的应用的意义,为CTCs后续研究提供参考。《共识》指出CTCs在血液循环中的数量、状态与疾病的早期诊断、肿瘤分期的细化、复发转移风险的评估及治疗效果的判断等密切相关,尤其对复发、转移性CRC具有更重要的意义。
循环肿瘤细胞检测在结直肠癌中的应用专家共识具体内容如下:
一、CTCs的定义及特性
1. CTCs的定义
CTCs是从原发或继发肿瘤脱离进入循环系统的肿瘤细胞。其中部分肿瘤细胞经历上皮—间质转化等过程获得高侵袭性,可形成转移性病灶。
2. CTCs的特性
(1)稀有性;
(2)异质性。
二、CTCs的检测技术
1.CTCs的分离富集技术
(1)基于物理特性的分离富集技术
其优势在于不破坏CTCs形态,不依赖CTCs的表面抗原,同时兼容多种下游分析技术,利于后续对单个CTCs进行形态学、免疫细胞学及遗传学特征的研究。其中芝友医疗CTCBIOPSY系统属于“微过滤”装置,核心部件是一个滤孔分布均一的纳米微筛,主要依据CTCs与正常的血源性及非血源性细胞体积大小和形变能力的差异,从外周血中分离富集CTCs。
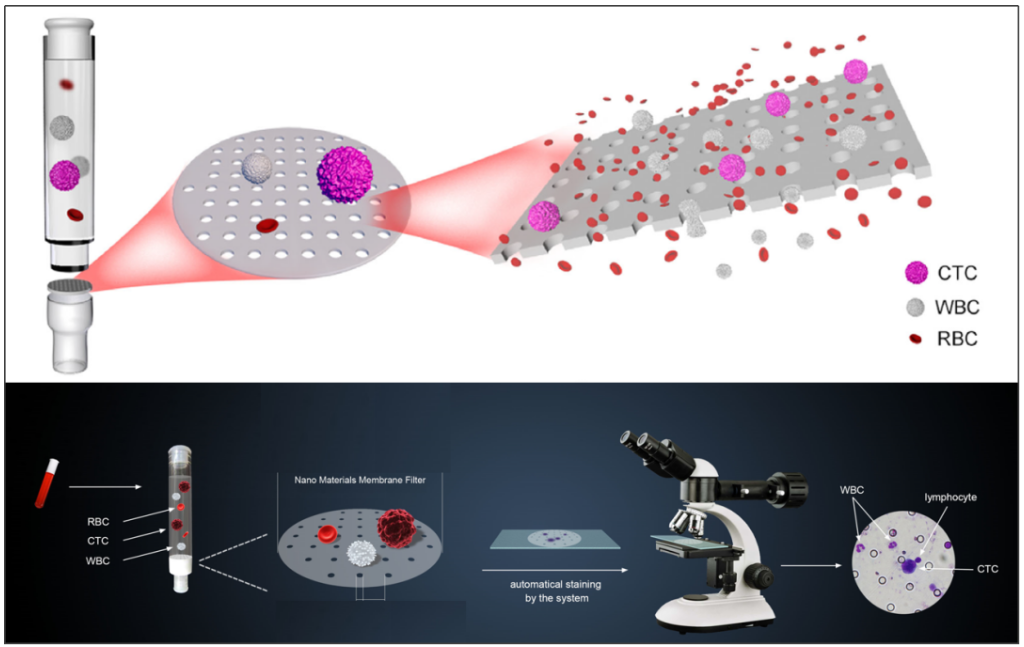
CTCBIOPSY原理及检测过程[3]
(2)基于肿瘤细胞免疫学特性的分离富集技术
主要依据免疫学原理,应用磁珠、黏附、白细胞去除等方法通过阳性富集或阴性富集进行CTCs的分离富集。如采用磁珠法的CellSearch系统是阳性富集的代表,采用EpCAM抗体标识的微磁珠捕获CTCs,但由于发生上皮-间质转化的CTCs表现EpCAM阴性且CTCs表面抗原的异质性,导致该方法灵敏度和特异度极大降低。
2.分离富集与鉴定技术的结合
目前鉴定方法主要有细胞水平和分子水平两个层面。常见CTCs检测平台及其特性如下图:

三、CTCs的检测流程
目前商品化的CTCs检测平台众多,下面将以具有代表性的基于生物学特性与物理特性的分离富集技术的Janssen公司CellSearchTM系统及芝友医疗CTCBIOPSY系统简述两种系统的检测方法。
1.美国强生CellSearchTM系统检测流程

2. 芝友医疗CTCBIOPSY系统检测流程
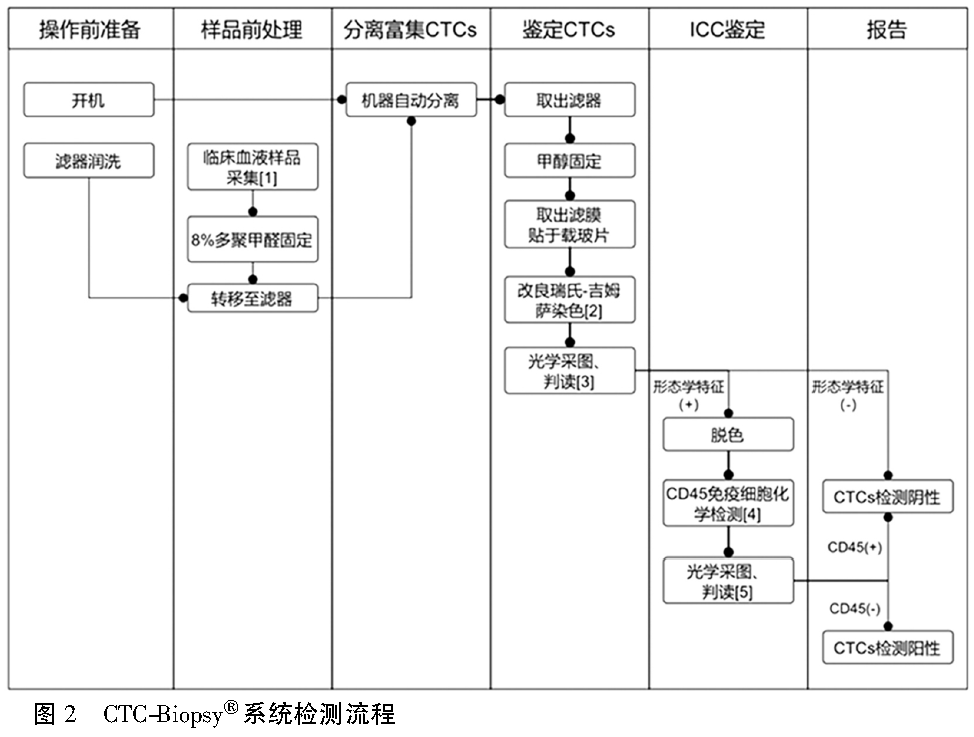
3.CTCs检测的推荐时间点及时限
对于术后随访,我们推荐根据NCCN结肠癌及直肠癌指南中所提到的随访时间,同时进行CTCs检测。结合病史及查体,术后前2年,每3-6个月复查一次;3-5年,每6个月复查1次;5年后,根据情况,决定是否需要继续行CTCs检测。
四、CTCs的临床意义
1.早期筛查
2018年ASCO会议的一项纳入620例受试者的前瞻性临床研究表明,通过CTCs检出CRC癌前病变的敏感性为76.6%,与结肠镜的筛查效果(76%-94%)接近;而对于CRC的敏感性高达86.9%,超过粪便潜血试验(FOBT)的筛查效果(62%-79%),与结肠镜检查的效果相同(75%-93%)。

CTCs检测的灵敏度和特异性[4]
因此,在合理选择CTCs检测平台、控制检测成本、制定并完善相应检测指征及判读标准的前提下,使用CTCs检测作为CRC早期筛查的方法是合理可行的。
2.预后判断
(1)非转移性CRC
研究表明,对于AJCC-Ⅲ期的CRC患者,术前外周血CTCs是患者总生存期及无进展生存期强效且独立的预测因子。与术前外周血中CTCs阴性患者相比,阳性患者的总生存期及无进展生存期均显著下降。对于CRC患者,术前外周循环检测到CTCs可视作肿瘤复发或远处转移的高危因素,术后应规律复查,密切随访,适当予以更为积极的治疗。
(2)转移性结直肠癌(Metastatic colorectal cancer,mCRC)
目前认为,CTCs是恶性肿瘤血行转移的基础。不论在基线水平抑或接受辅助治疗(包括化疗和/或靶向治疗)后,当外周循环CTCs≥3个/7.5mL血液或检测到CTM时,提示预后不良,相应的mCRC患者的总生存期及无进展生存期显著下降。外周循环CTCs与患者年龄、辅助治疗方案、癌胚抗原(CEA)水平及ECOG评分等均是mCRC患者总生存期及无进展生存期的独立预测因子,联合应用在提示预后方面具有重要的临床意义。
3.疗效预测
动态检测外周循环CTCs水平,有助于了解患者的治疗效果。对于接受根治性手术的CRC患者,术后24h内CTCs水平显著下降,提示手术效果良好,肿瘤复发的可能性低。对于接受化疗和/靶向治疗的mCRC患者,经过治疗后CTCs数量下降,表明治疗有效,患者总生存期及无进展生存期显著延长。治疗过程中或术后复查时规范检测CTCs可帮助判断疾病的状态,与影像学检查及肿瘤标记物(CEA)检测联合应用具有更高的临床指导价值。
五、展望
CTCs虽然很早就被发现,但由于技术条件的限制,其应用于CRC临床诊疗的过程困难重重。而近年,由于CTCs分离检测技术的发展与成熟,使其在临床应用中变得切实可行。本共识的制定旨在对CTCs检测在CRC中的应用起到初步的释疑及指导作用,从而为CRC的临床诊疗提供有效、可行的检测手段。

参考文献
1. Anticancer Res.2013 Feb;33(2):625-9.
2. 循环肿瘤细胞检测在结直肠癌中的应用专家共识(2018).腹腔镜外科杂志,2019,24(01):74-80.
3. Clin.Transl.Med.2021;11:e318.
4. Clin Transl Gastroenterol.2019 Oct;10(10).
附上芝友医疗CTCBIOPSY检测系统2021年结直肠癌的部分检测数据:
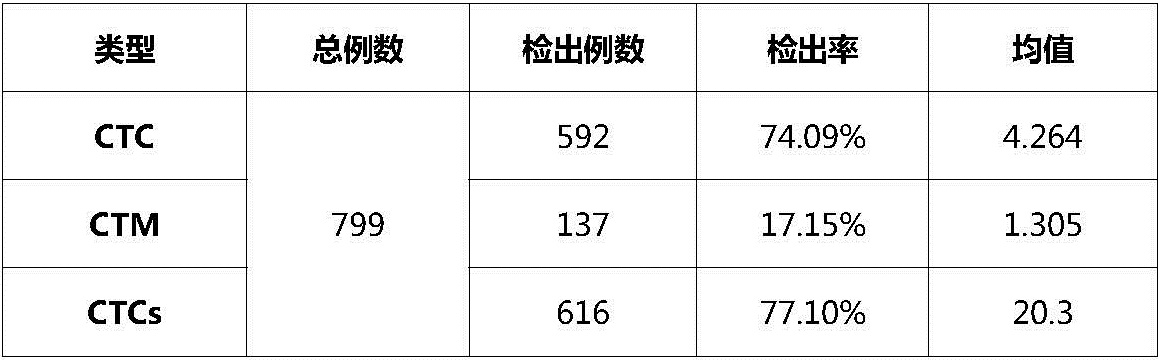


(转化医学网360zhyx.com)
 腾讯登录
腾讯登录
还没有人评论,赶快抢个沙发