“根除”致命实体瘤!Science 连发两篇:CAR-T细胞全新升级,克服肿瘤治疗障碍
| 导读 | 嵌合抗原受体T细胞疗法拥有光明前景,人类T细胞被设计成攻击肿瘤,提高了人们对基于细胞的疗法的兴趣。具有识别肿瘤抗原的修饰受体(嵌合抗原受体或CAR-T细胞)的T细胞已被证明可有效治疗B细胞恶性肿瘤,但实体瘤会产生限制其功能的免疫抑制微环境。 |
12月15日,波士顿大学研究团队在《Science》发表文章“Multidimensional control of therapeutic human cell function with synthetic gene circuits”,报道了研究团队开发出一个工具箱,包含11个可编程的合成转录因子。这些转录因子可以被一些已经获批临床使用的小分子药物激活,通过精确调控基因,启动特定的细胞程序,即通过定时给药,就可以实现按需激活细胞。

https://www.science.org/doi/10.1126/science.ade0156
12月16日,加州大学旧金山分校研究团队在《Science》发表文章“Synthetic cytokine circuits that drive T cells into immune-excluded tumors”,研究人员能够通过对肿瘤浸润的 T 细胞进行编程以在识别癌细胞时制造自己的 IL-2,从而保持癌症中包含的细胞因子。

https://www.science.org/doi/10.1126/science.aba1624
研究一
精确控制人体细胞功能的合成基因回路可以扩大基因和细胞的治疗能力。然而,目前缺乏用于在原始人类细胞中开发电路的平台,这些回路可以驱动体内强大的功能变化,并具有适合临床使用的成分。
研究人员开发了合成锌指转录调节剂(synZiFTRs),它结构紧凑,主要基于人类来源的蛋白质。作为原理证明,我们设计了基因开关和电路,允许使用美国食品和药物管理局批准的小分子诱导剂精确地、用户定义的控制初级T细胞中的治疗相关基因。我们的电路可以指示T细胞依次激活多个细胞程序,如增殖和抗肿瘤活性,以驱动协同治疗反应。该平台将加速在不同人类细胞类型和背景下合成基因电路的开发和临床转化。
研究人员还展示了一种双开关系统,该系统允许顺序控制免疫细胞功能。该平台可以适应在各种情况下设计细胞疗法。
研究二
许多实体瘤对T细胞疗法没有反应,因为它们的免疫抑制微环境阻断了T细胞浸润、活化和增殖。主要的肿瘤抑制机制包括抑制T细胞受体(TCR)信号传导和消耗炎性细胞因子。克服抑制性肿瘤微环境仍然是实体瘤免疫治疗的主要障碍。
为了设计能够感知肿瘤中细胞的 T细胞,研究人员使用了一种合成的Notch(或synNotch)受体,这是一种灵活的分子传感器。这些受体跨越细胞膜,末端突出细胞内外。外部部分识别并与肿瘤细胞结合,触发内部部分以启动IL-2的产生。
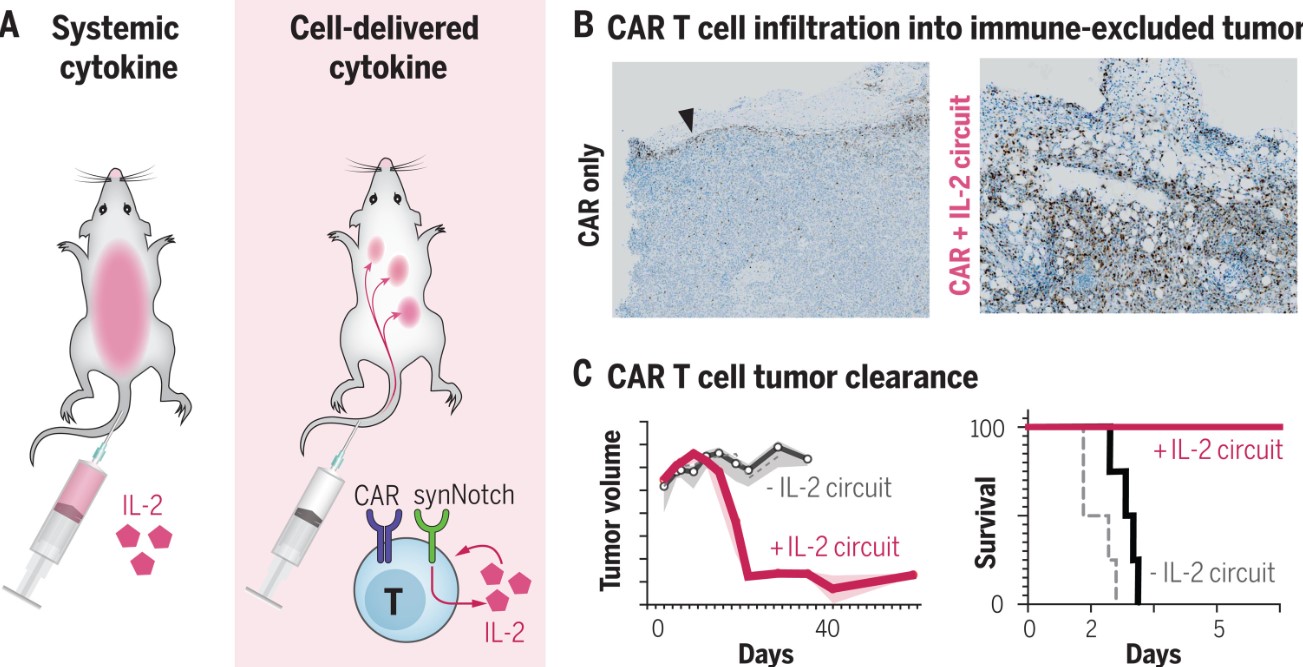
驱动T细胞进入免疫排除肿瘤的合成细胞因子回路
研究小组在许多致命肿瘤上测试了synNotch细胞,包括黑色素瘤和胰腺癌,发现这些细胞完全按计划工作。“我们能够设计这些治疗细胞来绕过肿瘤的防御屏障。一旦进入肿瘤,他们就可以站稳脚跟,并开始有效地杀死癌细胞,“艾伦(Allen)说。“我们掌握了这些肿瘤,并在某些情况下治愈了它们。
艾伦表示:最先进的免疫疗法在很多这些困难的实体瘤中不起作用,我们认为这种类型的设计可以克服主要障碍之一,并以安全且无副作用的方式进行。免疫疗法消除了小鼠的黑色素瘤和胰腺癌,没有重大副作用,它为对抗这些和其他难以治疗的癌症提供了一种有前途的新策略。(转化医学网360zhyx.com)
参考资料:
https://medicalxpress.com/news/2022-12-pancreatic-cancer-cells-supercharge.html
https://www.science.org/doi/10.1126/science.ade0156
https://www.science.org/doi/10.1126/science.aba1624
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录

还没有人评论,赶快抢个沙发