重大发现!北京大学詹启敏院士等最新发文
| 导读 | 重编程的细胞代谢对于维持癌症干细胞(CSCs)状态至关重要。一些研究证实,ESCC中存在CSCs种群。然而,ESCC-CSCs干性维持的机制仍然未知。 |
近日,北京大学詹启敏院士和张维敏副研究员共同在《Signal Transduction and Targeted Therapy》上发表研究论文“CDK7-YAP-LDHD axis promotes D-lactate elimination and ferroptosis defense to support cancer stem cell-like properties”,研究得出结论,食管CSCs采用依赖于CDK7-YAP-LDHD轴的D-乳酸消除和丙酮酸积累模式,这驱动了ESCC-CSCs的干性相关特征。那么,靶向代谢检查点可作为 ESCC 治疗的有效策略。

https://www.nature.com/articles/s41392-023-01555-9
研究背景
CSCs的代谢特征与块状肿瘤细胞的代谢特征不同。CSCs更多地依赖于线粒体氧化磷酸化(OXPHOS)和脂肪酸氧化,而分化的肿瘤细胞主要依赖于糖酵解。然而,一些研究表明,CSCs也可以利用糖酵解和谷氨解来维持能量需求,并且可以在代谢应激下从OXPHOS转变为糖酵解,表明CSCs的代谢灵活性。如上所述,CDK不仅对维持CSCs的干性至关重要,而且还参与细胞代谢过程的调节。CDK6/细胞周期蛋白 D3 已被证明可以磷酸化和灭活 PFK1 和 PKM2,从而抑制 G1 期的糖酵解,而 CDK6/细胞周期蛋白 D1 已被证明可以通过下调 G1 期线粒体基因的表达来抑制 PGC-1α和NRF1的转录活性以减弱OXPHOS。此外,在S期,CDK2/细胞周期蛋白E可能磷酸化IDH1/2并阻断三羧酸(TCA)循环,而CDK2/细胞周期蛋白A在G2相可以抑制IDH1/2。此外,CDK1/细胞周期蛋白B1通过增强OXPHOS促进G2/M转变。然而,以前关于CSCs的大多数研究都集中在代谢酶的异常表达或活性改变以及致癌驱动的代谢途径重新布线上,几乎没有支持CDKs偶联代谢调节在CSCs功能中的作用的证据。
研究进展
为了阐明调节CSCs干性的机制,我们首先对食管鳞状癌细胞谱系进行了球状形成分析,以确定其自我更新能力。KYSE410细胞在随后的连续繁殖中显示出显著增强的球体形成能力,表明它们提高了自我更新能力。CD90 已被指示在功能上决定ESCC-CSCs亚群。一致地,我们发现,由KYSE410细胞形成的球体比那些贴壁细胞具有更高的CD90富集度。此外,球体相对于贴壁单层的ABCG2、SOX9、SOX2、OCT4和NANOG的表达明显增强。
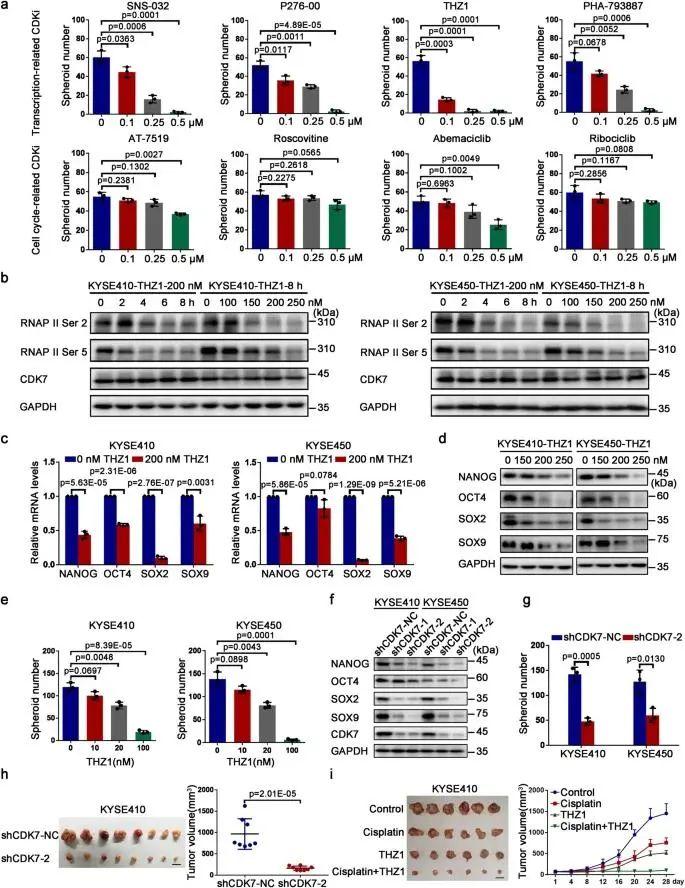
CDK7表达降低导致ESCC CSCs的茎样特性减弱
为了确定细胞周期相关激酶在ESCC-CSCs干性维持中的依赖性,我们使用小分子抑制剂在药物上抑制这些激酶并评估其球状体形成能力。为此,24种细胞周期相关激酶的小分子抑制因子(目前几乎都处于I期和II期临床试验中,涉及细胞周期和转录相关CDKs)的抑制因子,以阐明其抗CSCs活性。用这些小分子处理KYSE410细胞,并在72小时通过MTS测试测量细胞活力。接下来,在球状体形成测试的帮助下评估他们的抗食管CSCs效力。结果表明,新型共价CDK7抑制因子THZ1显示出强大的抗ESCC-CSCs效应,这反映在THZ1处理后KYSE410细胞的球状体形成电位受到显著抑制。这些结果有力地表明,CDK7可能是维持ESCC-CSCs干性的关键分子。先前使用转录组技术(RNA-Seq)的研究表明,一组转录本在低THZ1剂量下受到特异性抑制,其部分抑制了RNAPII功能。这些转录本被称为“THZ1敏感转录本”,它们基本上识别了癌细胞。
研究意义
总的来说,我们的研究结果揭示了一种新机制,即由CDK7介导的S127和S397位点的核YAP特异性磷酸化促进LDHD转录以驱动线粒体中的D-乳酸分解代谢,保护食管CSC免受铁死亡并产生丙酮酸,最终支持ESCC CSCs的干细胞样特征(图8k)。因此,CDK7-YAP-LDHD轴可能是ESCC治疗的一个有吸引力的候选者,通过靶向代谢检查点。

CDK7-YAP-LDHD轴驱动的D-乳酸分解代谢工作模型促进丙酮酸生成,帮助ESCC细胞从D-乳酸诱导的铁死亡中逃脱,进而支持ESCC-CSCs的性质。(转化医学网360zhyx.com)
参考资料:
https://www.nature.com/articles/s41392-023-01555-9
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发