溶瘤病毒抗癌症,用“魔法”打败“魔法”!国内研究发现非小细胞肺癌潜在治疗方法
| 导读 | 随着病毒与宿主相互作用机制的不断深入研究,病毒已成为一种很有前景的癌症治疗工具。事实上,许多具有选择性和有效性的溶瘤病毒已被用于癌症治疗。人类肠道病毒是产生溶瘤病毒的最方便的来源之一,但某些肠道病毒的高血清阳性率限制了其应用,迫切需要开发更多的溶瘤肠病毒。 |
近日,国家卫生健康委/国家药监局生物制品研究所/中国食品药品检定研究院梁正伦等研究人员在权威期刊《Signal Transduction and Targeted Therapy》上发表了题为“Non-small cell lung cancers (NSCLCs) oncolysis using coxsackievirus B5 and synergistic DNA-damage response inhibitors”的论文,该研究筛选柯萨奇病毒B5/福克纳(oxsackievirus B5/Faulkner, CV-B5/F)通过诱导凋亡和自噬对非小细胞肺癌(non-small cell lung cancer, nsclc)的潜在溶瘤作用。对于难治性NSCLC, DNA依赖性蛋白激酶(DNA-PK)或共济失调毛细血管扩张突变蛋白(ATM)抑制剂可与CV-B5/F协同促进难治性细胞死亡。本研究确定了一种溶瘤病毒CV-B5/F和DNA-PK或ATM抑制剂的协同作用,这是一种潜在的治疗NSCLC的方法。

https://www.nature.com/articles/s41392-023-01603-4#Sec10
研究背景
01
2019年全球肿瘤的伤残调整寿命年约为1.05亿年。目前,免疫治疗因其靶向性和安全性成为肿瘤治疗的热点,包括嵌合抗原受体T细胞免疫治疗、免疫检查点阻断和溶瘤病毒(OV)治疗。OVs是一种天然或经过基因修饰的病毒,只能识别和溶解肿瘤细胞,而不能吞噬正常细胞。例如,T-vec被构建用于治疗黑色素瘤,并于2015年获得FDA批准。此外,包括DNA病毒和RNA病毒在内的许多类型的OVs正处于研究阶段。
OV的目标和效力取决于许多方面。一方面,它依赖于特定受体在肿瘤上的表达,而不是正常细胞上的表达。然而,信号通路可以帮助或损害这种作用。此外,在基线中和抗体水平或由OV引发的抗体水平引起了有限的“一次注射”方法的担忧。因此,OV必须是低血清价的,并确定其明确的受体和溶瘤机制。
最近,有报道称溶瘤性肠病毒以受体依赖的方式对肿瘤细胞发挥溶瘤作用,包括柯萨奇病毒A21 (CV-A21)、柯萨奇病毒B3 (CV-B3)和Echovirus 7。对于CV-A21,黑色素瘤是最敏感的细胞类型,在欧美高度流行,II期临床试验已经启动。肠病毒似乎是一种更安全的模式,它在宿主细胞质中复制而没有DNA阶段。因此,它们与DNA病毒不同,缺乏病毒基因组整合到宿主DNA中所引起的遗传毒性。肠道病毒是引起婴幼儿手足口病(HFMD)的主要病原体,包括肠道病毒A71、柯萨奇病毒A16、柯萨奇病毒A6、柯萨奇病毒A10、CV-B3、柯萨奇病毒B5 (CV-B5)、埃可病毒30、埃可病毒25,其血清阳性率较高,可能是其应用的障碍。此外,这些在亚洲常见的肿瘤类型,包括肺癌和肝癌,在OV研究中并没有得到均等的重视。因此,迫切需要开发更多可根据预先存在的中和抗体选择并用于亚洲高发癌症的溶瘤肠道病毒。
研究过程及发现
02
在本研究中,研究人员报道了CV-B5/F通过诱导细胞凋亡和自噬对非小细胞肺癌具有较强的抗肿瘤活性。对于难治性NSCLC细胞,如NCI-H460, DDR抑制剂可通过加剧内质网应激相关的细胞死亡和病毒繁殖,与CV-B5/F协同作用,产生溶瘤作用。
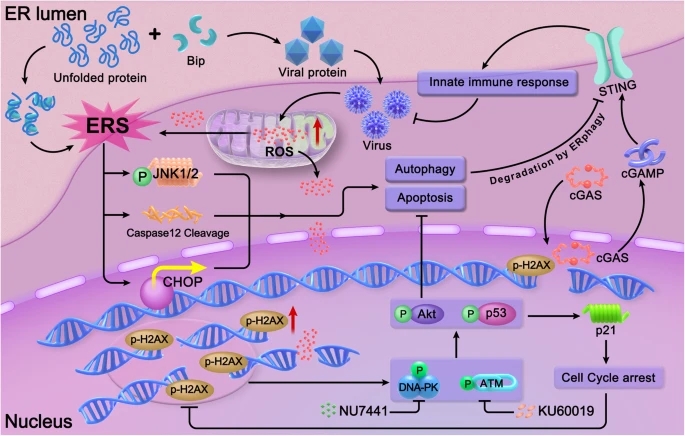
DNA-PK或ATM与CV-B5/F联合治疗的图形模型
在本研究中,在给药CV-B5/F后,凋亡和自噬不仅在多个NSCLC细胞中被激活,而且在免疫功能小鼠模型中也被激活,表明凋亡是细胞死亡的途径之一。
本研究通过一系列动物模型来评价溶瘤效果。对于免疫正常的BALB/c裸鼠模型,值得注意的是,瘤内注射CV-B5/F对A549和NCI-H1299移植瘤显示出显著的抗肿瘤作用,但对NCI-H460移植瘤无抗肿瘤作用。双侧皮下移植瘤内注射CV-B5/F可显著抑制远处未注射肿瘤的生长,这意味着传播的CV-B5/F可通过血液或淋巴系统循环并靶向远处肿瘤,有利于全身治疗转移或播散性肿瘤。
研究人员基于β2m敲除B-NDG和人pbmc构建人源化小鼠模型,通过消除MHC i类相关的移植物抗宿主病延迟发展,延长观察窗口期。
在本研究中,研究人员通过移植患者源性NSCLC肿瘤构建了PDX模型。5次注射CV-B5/F抑制(5/5)肿瘤生长,证实了CV-B5/F的溶瘤作用。
为保证安全,研究人员以高MOI感染正常肺细胞系,这些细胞没有表现出任何绝望。在体内安全性方面,对5次注射CV-B5/F的BALB/c裸鼠进行组织病理学分析,结果也证实了CV-B5/F的安全性。
为了阐明问题并应对难治性肿瘤,如NCI-H460,研究人员对具有协同治疗作用的药物进行了大规模筛选。研究人员观察到,CV-B5/F感染诱导的ROS引起DDR,修复DSB,促进细胞存活。结果表明,DNA-PKI或ATMI可恢复DDR并诱导内质网应激相关的细胞死亡。
在这项研究中,研究人员发现由病毒感染引起的加重的dsb将cGAS招募到细胞核中。相反,DNA-PK或ATM抑制剂加CV-B5/F可诱导吞噬降解STING,从而减弱过度激活的cGAS引起的抗病毒作用。
据研究人员所知,这些溶瘤作用仅在CDX模型中研究,一些研究观察到中度病毒诱导的疾病,包括胰腺炎、肝功能障碍和轻度心肌炎相比之下,CV-B5/F在CDX和PDX模型的nsclc中均表现出令人印象深刻的溶瘤作用,未观察到与治疗相关的死亡或疾病。
研究意义
03
综上所述,本研究确定了CV-B5/F是一种安全的、针对NSCLC的肿瘤特异性溶瘤病毒,并在多个CDX和PDX小鼠模型中得到了验证。此外,DDR抑制剂与CV-B5/F联合应用可通过加重病毒复制、DSB和细胞死亡的多种途径,为难治性癌症的治疗提供显著的治疗获益。(转化医学网360zhyx.com)
参考资料:
https://www.nature.com/articles/s41392-023-01603-4#Sec10
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发