调节免疫反应和肿瘤进展新机制!同济大学研究人员最新发文
| 导读 | CD24 在各种肿瘤中过表达,被认为是细胞迁移、侵袭和增殖的调节剂。最近的研究发现,卵巢癌(OC)和三阴性乳腺癌细胞上的 CD24 与肿瘤相关巨噬细胞(TAM)上的抑制性受体唾液酸结合 Ig 样凝集素10(Siglec-10)相互作用,以抑制巨噬细胞的吞噬作用。由于其在调节免疫反应和肿瘤发生方面的多重作用,CD24是一个非常有前途的治疗靶点。然而,CD24在OC中的调控机制尚不清楚。 |
2024年5月3日,徐韶华同济大学医学院徐韶华团队在《Cell Death & Disease》上发表题为“LncRNA IL21-AS1 facilitates tumour progression by enhancing CD24-induced phagocytosis inhibition and tumorigenesis in ovarian cancer”的研究论文,研究结果将 IL21-AS1 确定为调节 CD24 相关吞噬抑制和肿瘤发生的癌症生物标志物,并表明其作为 OC 治疗靶点的潜力。

https://www.nature.com/articles/s41419-024-06704-8
研究背景
01
上皮性卵巢癌(OC)的特点是复发率高,预后不良,是女性生殖系统最致命的癌症,这些特征促使人们努力确定这种疾病的潜在生物标志物和新疗法。长链非编码RNA(lncRNA)是一种非编码RNA,典型长度超过200个核苷酸。许多在各种癌症中表达异常的 lncRNA 已被证明参与肿瘤的发生、进展和转移。LncRNA作为癌症的治疗靶点具有巨大的潜力。因此,阐明lncRNAs在OC中的病理生理学贡献非常重要。
大量研究表明,肿瘤中分化簇 24 (CD24) 表达增加预示着预后不良。最近的研究表明,肿瘤中的表面 CD24 是一种新型抗吞噬蛋白,可与巨噬细胞上的唾液酸结合 Ig 样凝集素 10 (Siglec10) 相互作用。由于这种有趣的功能,CD24是癌症免疫治疗的新靶点。在临床前动物模型中,单克隆抗体 (mAb) 介导的 CD24 阻断已被证明是一种很有前途的 OC 治疗策略。然而,CD24 在许多不同类型的正常细胞上表达并调节。例如,它通常在免疫系统和神经系统的细胞上表达。树突状细胞上CD24的缺乏导致T细胞在诱导淋巴细胞减少时快速同质增殖,从而导致免疫功能正常的小鼠死亡。因此,直接使用抗CD24单克隆抗体可能会对患者产生意想不到的副作用。因此,有必要进一步探索CD24的分子调控机制,特别是在肿瘤微环境(TME)中,即实体瘤的局部生物环境。
TME由癌细胞、脉管系统、附近的基质细胞和免疫细胞组成。TAM 是 TME 最主要的免疫群体,占造血细胞的 ~50%,与人类恶性肿瘤的不良预后相关。在 OC 中,TAM 是最丰富的免疫细胞群,并通过多种机制在 OC 中组织极度免疫抑制的 TME。TAM 可以表达 Siglec10,这是一种抑制性的 I 型凝集素,可结合不吃我信号 CD24,并通过抑制吞噬作用促进免疫逃避。随着肿瘤的快速和不受控制的增殖,大面积的氧气和营养被剥夺,这使得缺氧成为几乎所有实体瘤的典型微环境特征。M2样TAM可以在缺氧肿瘤区域富集,其数量随着肿瘤的进展而增加。
研究结果
02
本研究,我们专注于 IL21 反义 RNA 1 (IL21-AS1),这是一种从 IL21 基因位点的反义链转录而来的 lncRNA,尚未在肿瘤中报道,在 OC 样本中的表达高于在正常卵巢组织中的表达。我们发现在OC中上调的长链非编码RNA(lncRNA)IL21-AS1抑制巨噬细胞介导的吞噬作用,促进OC细胞增殖和细胞凋亡抑制。更重要的是,在IL21-AS1敲除后,在移植肿瘤的小鼠中观察到显著的生存优势。从机制上讲,我们将 IL21-AS1 鉴定为缺氧诱导的 lncRNA。此外,IL21-AS1 在缺氧条件下增加了 HIF1α 诱导的 CD24 表达。同时,我们发现 IL21-AS1 作为 miR-561-5p 的竞争性内源性 RNA (ceRNA) 来调节 CD24 的表达。最后,IL21-AS1 增加了 OC 中 CD24 的表达并促进了 OC 的进展。我们的研究结果为CD24的调控提供了分子基础,从而突出了靶向治疗OC的潜在策略。
研究结论
03
这项研究表明,IL21-AS1是一种以前在癌症中未报道的lncRNA,在OC组织中上调,并且在晚期疾病患者中表达更高。功能性细胞试验表明,IL21-AS1 可以通过 IL21-AS1-HIF-1α-CD24 和/或 IL21-AS1-miR-561-5p-CD24 轴保护癌细胞免受巨噬细胞介导的吞噬作用并促进卵巢肿瘤发生(图 7J)。IL21-AS1 是一种新型缺氧反应性 lncRNA,可调节膜和细胞质 CD24 的表达,因此是 OC 的潜在诊断和预后标志物。
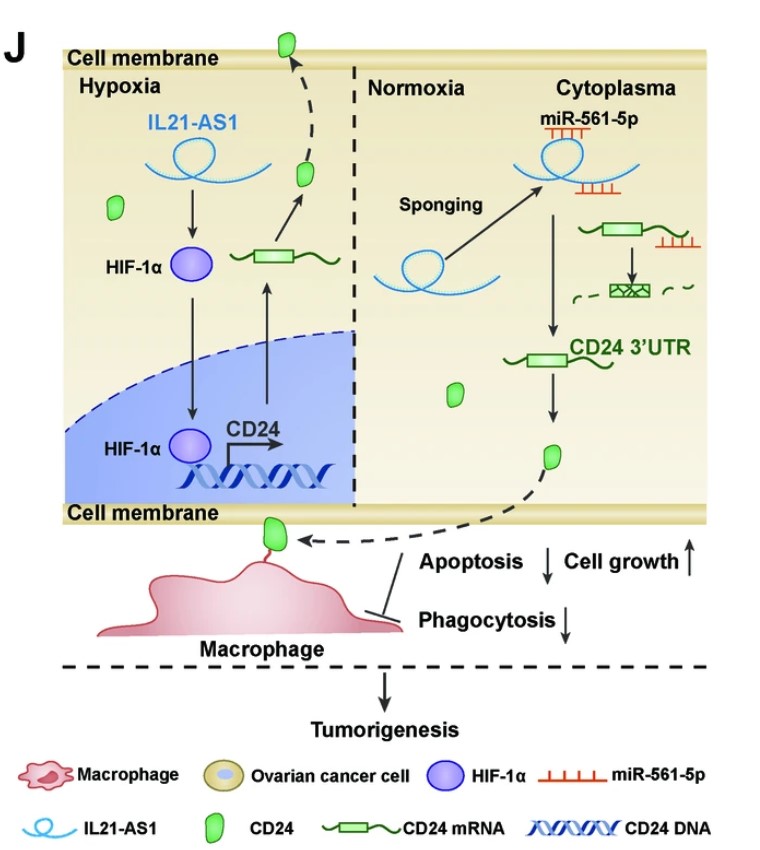
IL21-AS1通过上调CD24表达促进OC免疫逃逸和肿瘤发生的模型。(转化医学网360zhyx.com)
参考资料:
https://www.nature.com/articles/s41419-024-06704-8
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发