新发现!中山大学李建明团队揭示克服免疫检查点阻断治疗耐药性的新方法
| 导读 | DNA错配修复缺陷(dMMR)癌症中的超突变新抗原是对免疫检查点阻断(ICB)治疗产生良好临床反应的先决条件。然而,TMB与临床前和临床研究的良好预后没有显著相关性。这意味着除了TMB,还需要其他机制来促进成功的癌症免疫治疗。 |
5月13日,中山大学李建明团队在期刊《Cell Death Discovery》上在线发表题为“Tumors cells with mismatch repair deficiency induce hyperactivation of pyroptosis resistant to cell membrane damage but are more sensitive to co-treatment of IFN-γ and TNF-α to PANoptosis”的研究论文,研究结果表明,可以激活免疫细胞释放IFN-γ和TNF-α,以克服对ICB治疗的耐药性。研究结果揭示了dMMR癌症宿主对ICB治疗耐药的其他机制,并为未来的临床实践提供了方向。

https://www.nature.com/articles/s41420-024-01984-7
研究背景
01
患有DNA错配修复缺陷(dMMR)的癌症容易积累大量的体细胞突变,这些突变本身会诱导高免疫细胞浸润,因此对免疫检查点阻断(ICB)治疗具有高度敏感性和良好的预后。 然而,TMB与临床前和临床研究的良好预后没有显著相关性,抗PD-1治疗的客观缓解率(ORR)差异很大,从28%-53%不等。这些观察结果表明,除了TMB之外,还有其他未知的机制需要阐明成功的癌症免疫治疗。
成功的癌症免疫治疗不仅需要各种免疫细胞的良好配合,还需要对T细胞和NK细胞释放的杀伤分子(如proforin、granzyme、TNF-α、INF-γ)敏感的癌症。穿孔素可以在靶细胞的外质膜上形成孔隙,让颗粒酶进入胞质溶胶并启动泛凋亡。TNF-α和IFN-γ共同使细胞敏感,使其发生泛凋亡,而不会抑制TNF-α诱导IFN-γ细胞死亡。如果癌症在泛凋亡通路中出现缺陷,它们就会对包括ICB治疗在内的癌症免疫治疗产生耐药性。
研究进展
02
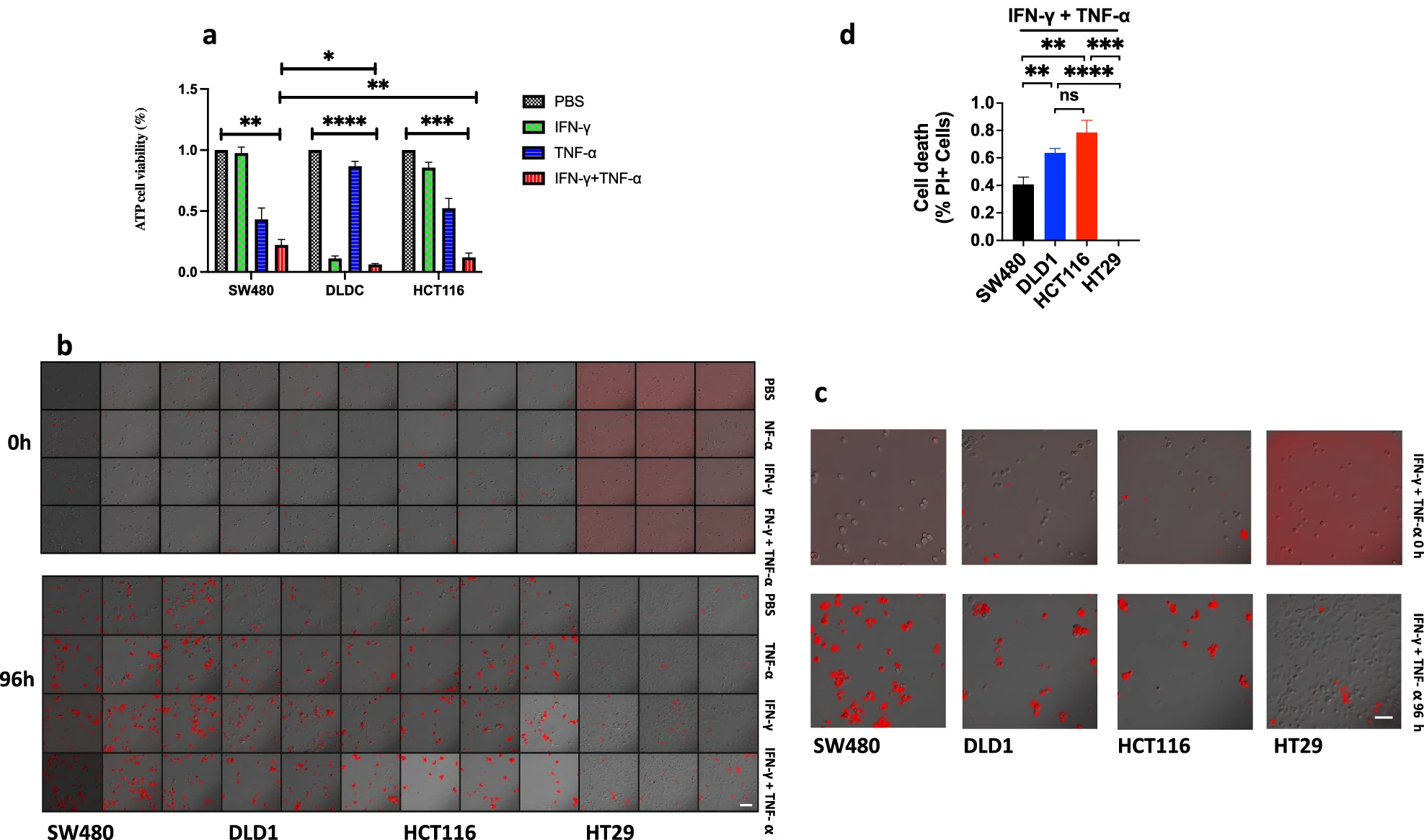
与pMMR肿瘤细胞系SW480或HT29相比,研究人员用IFN-γ、TNF-α或IFN-γ和TNF-α的共同处理诱导dMMR肿瘤细胞系DLD1或HCT116细胞泛凋亡。ATP释放结果显示,IFN-γ在SW480和HCT116中诱导的死亡很少,但在DLD1中诱导的死亡很多;在SW480和HCT116中,TNF-α可以诱导比IFN-γ更多的细胞死亡,但在DLD1中几乎没有死亡;ATP释放和PI染色结果显示,IFN-γ和TNF-α共同处理诱导的DLD1、HCT116、SW480和HT29细胞死亡最多,DLD1和HCT116的死亡细胞数多于SW480和HT29,DLD1、HCT116为dMMR癌细胞系,SW480和HT29为pMMR癌细胞系。结果表明,在IFN-γ和TNF-α共同治疗的情况下,dMMR肿瘤细胞比pMMR肿瘤细胞对泛凋亡更敏感。

研究发现
03
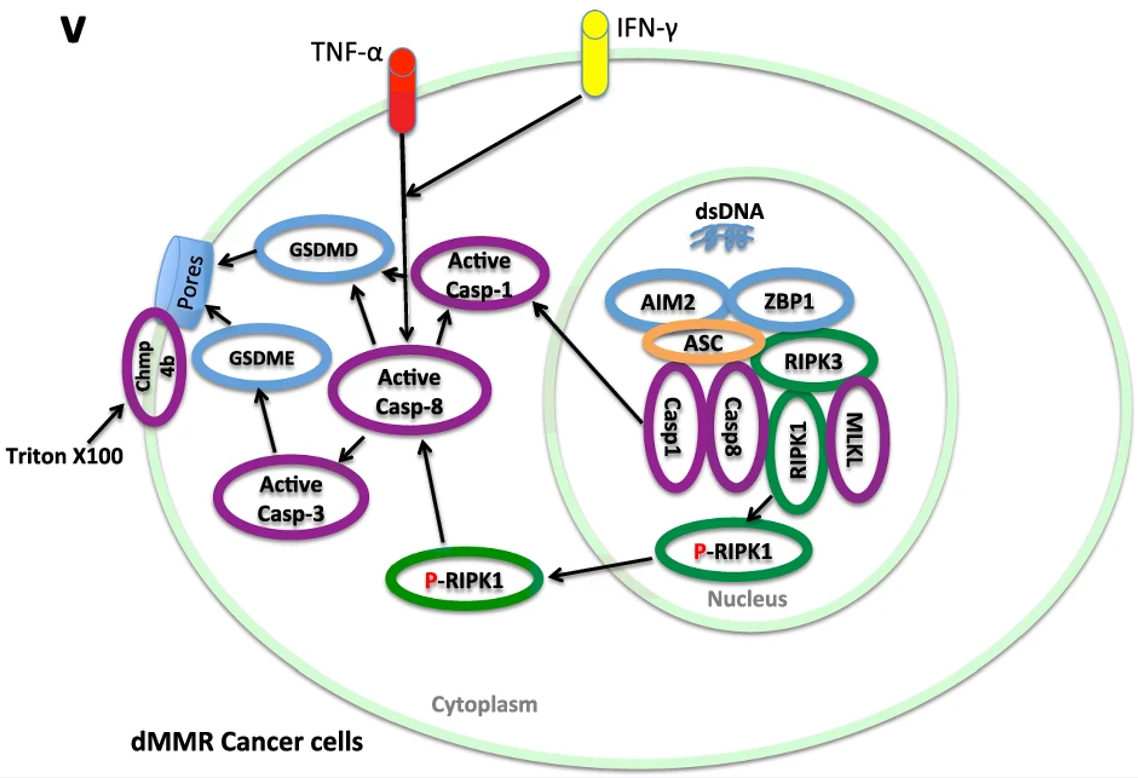
在研究中,研究人员发现MLH1的缺乏和随后的核DNA积累激活了AIM2-ZBP-ASC-RIPK1-RIPK3-CASP8-CASP1-GSDMD-GSDME-MLKL通路,有助于抵抗Triton X-100引起的细胞膜损伤,但对IFN-γ和TNF-α共同处理诱导的泛凋亡更敏感。研究结果揭示了dMMR癌症宿主对ICB治疗耐药的其他机制,并为未来的临床实践提供了方向。
研究结论
04
综上所述,研究结果表明,可以激活免疫细胞释放IFN-γ和TNF-α,以克服对ICB治疗的耐药性。研究结果揭示了dMMR癌症宿主对ICB治疗耐药的其他机制,并为未来的临床实践提供了方向。(转化医学网360zhyx.com)
参考资料:
https://www.nature.com/articles/s41420-024-01984-7
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录








还没有人评论,赶快抢个沙发