Adv Sci丨中山大学唐玲珑和赵银合作发现支架蛋白DCAF7促进鼻咽癌顺铂耐药和转移的新机制
| 导读 | 尽管多西他赛联合顺铂和5-氟尿嘧啶(TPF)已成为治疗晚期鼻咽癌(NPC)的标准方案,仍有部分患者对此治疗形式反应不佳。然而,这种治疗耐受机制尚不清楚。 |
文章要点
02
2024年7月8日,中山大学唐玲珑及赵银共同通讯在Advanced Science杂志上发表了题为“DCAF7 Acts as A Scaffold to Recruit USP10 for G3BP1 Deubiquitylation and Facilitates Chemoresistance and Metastasis in Nasopharyngeal Carcinoma”的研究论文,该研究发现DCAF7是一个化疗耐药基因,减弱了NPC患者对TPF治疗的反应。DCAF7在体外和体内均能增强NPC细胞的顺铂耐药性和转移能力。
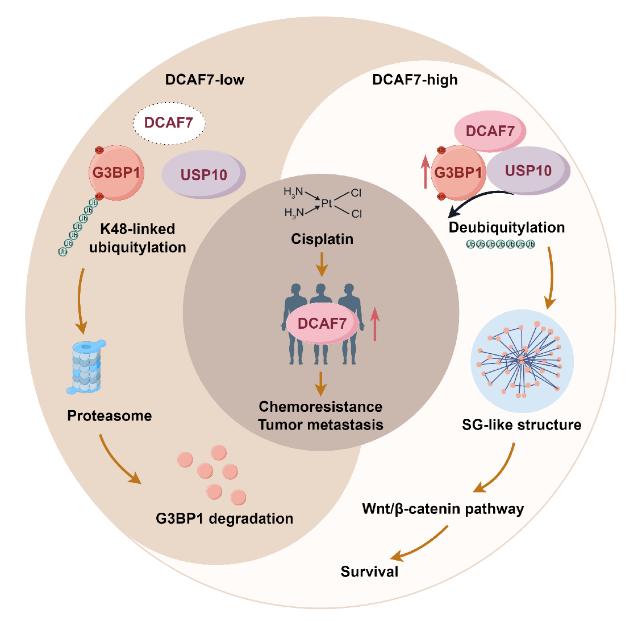
在机制上,DCAF7作为支架蛋白,促进了USP10和G3BP1之间的相互作用,导致G3BP1上K48连接的K88位点泛素化被去除。此过程有助于通过泛素-蛋白酶体途径防止G3BP1被降解,并促进应激颗粒(SG)样结构的形成。此外,敲低G3BP1成功逆转了SG样结构的形成和DCAF7的致癌效应。临床上,DCAF7高表达的NPC患者肿瘤转移率较高,生存率较低。总之,该研究揭示了DCAF7是促进顺铂耐药的重要基因,DCAF7-USP10-G3BP1轴为NPC的治疗提供了潜在靶点和生物标志物。

https://onlinelibrary.wiley.com/doi/10.1002/advs.202403262
鼻咽癌(nasopharyngeal carcinoma, NPC)是一种常见于东南亚,尤其是中国南部的头颈部肿瘤。目前,多西他赛、顺铂加5-氟尿嘧啶(TPF)诱导化疗是局部晚期鼻咽癌(LA-NPC)患者的标准治疗方案。然而,大约10%的NPC患者在接受这种治疗后效果不佳,主要原因是化疗耐药性的出现。因此,阐明化疗耐药的分子机制至关重要,为完善NPC治疗策略提供可能。
支架蛋白可作为分子枢纽,可与其他蛋白质对接,组建信号传导级联功能单位,在细胞周期、细胞生长、免疫反应和细胞骨架重构等多种生物过程中起作用。支架蛋白的失调可导致多种疾病(如癌症、糖尿病和阿尔茨海默病等)。值得注意的是,泛素化的调控对控制支架蛋白介导的信号传导级联反应至关重要。例如,NEMO在泛素化后会发生构象变化和液-液相分离,从而增加其对其他底物的结合亲和力。TRAF2招募cIAP1/2泛素化IKKε,导致NF-κB信号的激活。ZMIZ2招募USP7去泛素化并稳定β-连环蛋白。DCAF7是一种属于DDB1和CUL4相关因子(DCAF)家族的支架蛋白,该家族成员通常作为E3泛素连接酶底物受体,调控包括YAP-Hippo通路、组蛋白甲基化和HIPK2-MAPK信号在内的多种信号级联反应和事件。然而,DCAF7是否在NPC发生或进展中发挥作用尚不清楚。
应激颗粒(SG)是大量mRNA、RNA结合蛋白和翻译起始因子在热休克、渗透压和药物等应激条件下形成的细胞质凝结物。Ras GTP酶激活蛋白结合蛋白1(G3BP1)及其与USP10和Caprin1的相互作用对于SG的形成和调控非常重要。G3BP1通过与RNA和蛋白质的相互作用,响应细胞内外刺激,调节mRNA稳定性、rasGAP信号、泛素化和mRNA代谢等一系列细胞过程,这些相互作用的失调可导致神经系统疾病、癌症进展及细菌和病毒感染。USP10与G3BP1相互作用,阻止其他RNA和蛋白质的招募以形成SG。然而,G3BP1介导的SG是否包含其他结合因子,以及这些潜在结合因子如何与USP10和G3BP1相互作用,仍然知之甚少。
通过分析鼻咽癌耐药组织芯片数据,该研究发现DCAF7在TPF耐药的NPC患者中高表达,并促进NPC细胞对顺铂耐药和转移。进一步的质谱分析鉴定了G3BP1和USP10是DCAF7的结合蛋白。在机制上,DCAF7促进了USP10与G3BP1的结合,去除了G3BP1的Lys76上的K48泛素链,从而防止G3BP1通过泛素-蛋白酶体途径的降解,并促进SG样结构的形成。此外,敲低G3BP1逆转了SG样结构的形成以及DCAF7的致癌效应。临床上,DCAF7高表达的NPC患者具有高转移风险和较差的预后。本研究确定了G3BP1新的结合蛋白,拓展了对G3BP1介导的SG样结构形成的理解。更重要的是,我们确定了DCAF7是顺铂耐药的关键基因,并深入了解了TPF耐药在NPC患者中的发生机制,从而确定了NPC的潜在治疗靶点,为改善鼻咽癌治疗策略提供理论基础。
中山大学肿瘤防治中心博士生黎庆杰、方学良、林嘉仪和黎映琴副研究员为该论文的共同第一作者,中山大学肿瘤防治中心唐玲珑教授和赵银副研究员为共同通讯作者。
通讯作者简介
03
唐玲珑:教授,主任医师,博士生导师,中山大学肿瘤防治中心放疗科副主任、党支部书记,教育部长江学者特聘教授,华南恶性肿瘤防治全国重点实验室PI,主要从事鼻咽癌的临床诊治及基础转化研究。近5年来,作为第一或通讯(含共同)作者发表SCI论文29篇,包括JAMA 、Lancet、Lancet Oncol、BMJ、J Clin Oncol(2篇)、Adv Sci、Cell Death & Dis等,2篇论文入选ESI高被引论文,主持国家自然科学基金面上项目3项。学术兼职包括中国抗癌协会青年理事会理事、广东省抗癌协会鼻咽癌专业青年委员会主任委员,中国抗癌协会鼻咽癌专委会委员及中国肿瘤学会鼻咽癌专委会委员。因团队发展需要,现招聘特聘副研究员1名、博士后2名,感兴趣的老师同学请发邮件至唐老师邮箱tangll@sysucc.org.cn。
赵银:博士、中山大学肿瘤防治中心副研究员、硕士生导师,围绕“表观遗传修饰和泛素化修饰调控鼻咽癌转移和治疗抵抗机制”开展了系列基础研究,共发表第一/通讯(含共同)SCI论文11篇,包括Adv Sci(3篇)、Nat Commun(3篇)、Cell Rep、Cancer Commun、Cell Death & Dis等;主持国家自然科学基金面上项目、青年项目和中国博士后科学基金多项。(转化医学网360zhyx.com)
参考资料:
https://onlinelibrary.wiley.com/doi/10.1002/advs.202403262
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发