【Nature子刊】香港中文大学毛传斌团队利用病毒灵活性,精准解析癌症亚型
| 导读 | 在本研究中,团队提出了一种利用细菌病毒(噬菌体)纳米纤维的灵活性的解决方案。 |
2024年7月12日, 香港中文大学生物医学工程系毛传斌团队在期刊《Nature Communications》上发表了题为“T Harnessing virus flexibility to selectively capture and profile rare circulating target cells for precise cancer subtyping”的研究论文。本研究揭示了病毒修饰固体表面的机械特性,在分离稀有细胞(如CTC)方面的重要作用,包括靶细胞结合亲和力和减轻与非靶细胞(如 WBC)的非特异性相互作用。

https://www.nature.com/articles/s41467-024-50064-y#Sec1
研究背景
01
基于亲和力的表面生物检测,如酶联免疫吸附检测 (ELISA) 和免疫磁隔离,在临床诊断、环境监测和药物筛选中,具有至关重要的意义。这些检测的初始阶段,取决于配体和受体之间的相互作用,决定了检测的亲和力。通过调整配体类型、密度、分布和构象等参数,科学界已经做出了相当大的努力,来增强结合亲和力。其中,非靶细胞或生物分子的非特异性吸附,会显著破坏检测性能。这是通过占据活性靶标结合位点,或阻碍表面信号转导而发生的。因此,迫切需要推进表面屏蔽策略。
M13噬菌体(也称为噬菌体)表现为一种纳米纤维样细菌特异性病毒,长度为880nm,直径为6nm。M13纳米纤维的表面,可以通过基因工程或化学修饰轻松定制。因此,将M13组装到支架中,已经在各种应用中,取得了显著的成功。包括组织再生疗法、传感、甚至能量收集。团队最近发现,M13噬菌体由于其摇摆运动,而能够加速液固界面的质量传递。
CTC起源于实体瘤并进入血液,在诊断肿瘤转移和评估预后方面,作为液体活检的靶标,具有重要前景。鉴于它们在血液中的稀有性,开发有效的基于亲和力的分离表面,势在必行。团队利用实验和模拟技术的混合,来展示适应性柔性M13噬菌体,在构建磁珠中的应用,形成可以紧密捕获CTC的可变形表面。这种设计,通过允许噬菌体扭曲,以最大限度地与CTC上的受体结合,并在熵上阻止WBC在该表面上结垢,来增强CTC的捕获。
简而言之,噬菌体侧壁上携带许多pVIII蛋白拷贝,使噬菌体修饰的珠子,能够提供充足的反应性位点,以呈现许多亲和配体。纳米纤维固有的柔韧性,使其能够自由扭曲,从而调整配体构型,使其与靶受体在CTC表面上的分布模式,最佳地对齐。此外,由于其低刚度和杨氏模量(其柔韧性的量化),M13噬菌体在流动溶液中,具有变形性。这种基于噬菌体的CTC捕获物理屏蔽策略,消除了对防污聚合物额外涂层的需求。通过这种物理屏蔽方法,植根于噬菌体结构的可变形表面,为构建高效和抗污的表面生物检测,提供了一条有前途的途径。
研究进展
02
灵活的M13有助于更好地捕获CTC
通过将柔性Apt-M13纳米纤维,固定在Ni-IDA MB上,以锻造A-f-M13-MB,使用MCF-7作为模型MUC1 CTC,评估了其与CTC的结合亲和力。适应性强的CTC捕获A-f-M13-MB表面的CTC结合亲和力,显著增加了。此外,A-f-M13-MB表面的CTC结合亲和力,比将适配体直接固定在MBs(即A-MB)上形成的表面的亲和力,高出约19,200倍。这凸显了柔性Apt-M13噬菌体的关键作用。有趣的是,用其他刚性噬菌体,替换柔性Apt-M13噬菌体,导致A-r-M13-MBs(A 代表“适配体”,r 代表“刚性”)的CTC结合亲和力,大幅降低了22.8倍。很明显,Apt-M13的灵活性,是CTC结合亲和力增强的主要驱动因素。
为了更深入地研究M13的灵活性,在影响CTC群体和亲和力固体表面之间的粘附力方面的作用,团队进行了基于离心的细胞粘附检测。实验结果揭示了柔性M13的粘附力,至少比刚性M13高18%。这一结果再次强调,M13固有的灵活性,有助于实现与CTC受体的稳健结合。
为了更深入地了解,由于灵活性而增强的多价相互作用,团队采用了耗散粒子动力学(DPD),探索CTC和MB之间复杂的分子水平相互作用。在模拟中,构建了3种不同类型的MB,即A-MB、A-f-M13-MB和A-r-M13-MB。实验结果显示,CTC受体可以同时与大量适配体,相互作用。与其他两种MB类型相比,CTCs和A-f-M13-MB之间的相互作用,在能量上最有利。这归因于M13锚定的适配体和CTC受体之间的接触增加。
值得注意的是,M13噬菌体和适配体的自由度,在MB表面的CTC吸附时,受到限制。这种还原,增加了相互作用的熵项(-TΔS),从而对吸附产生了熵威慑作用。然而,鉴于特异性受体-适配体相互作用的明显强度,在吸附过程中,相互作用能量优于这些熵因子。
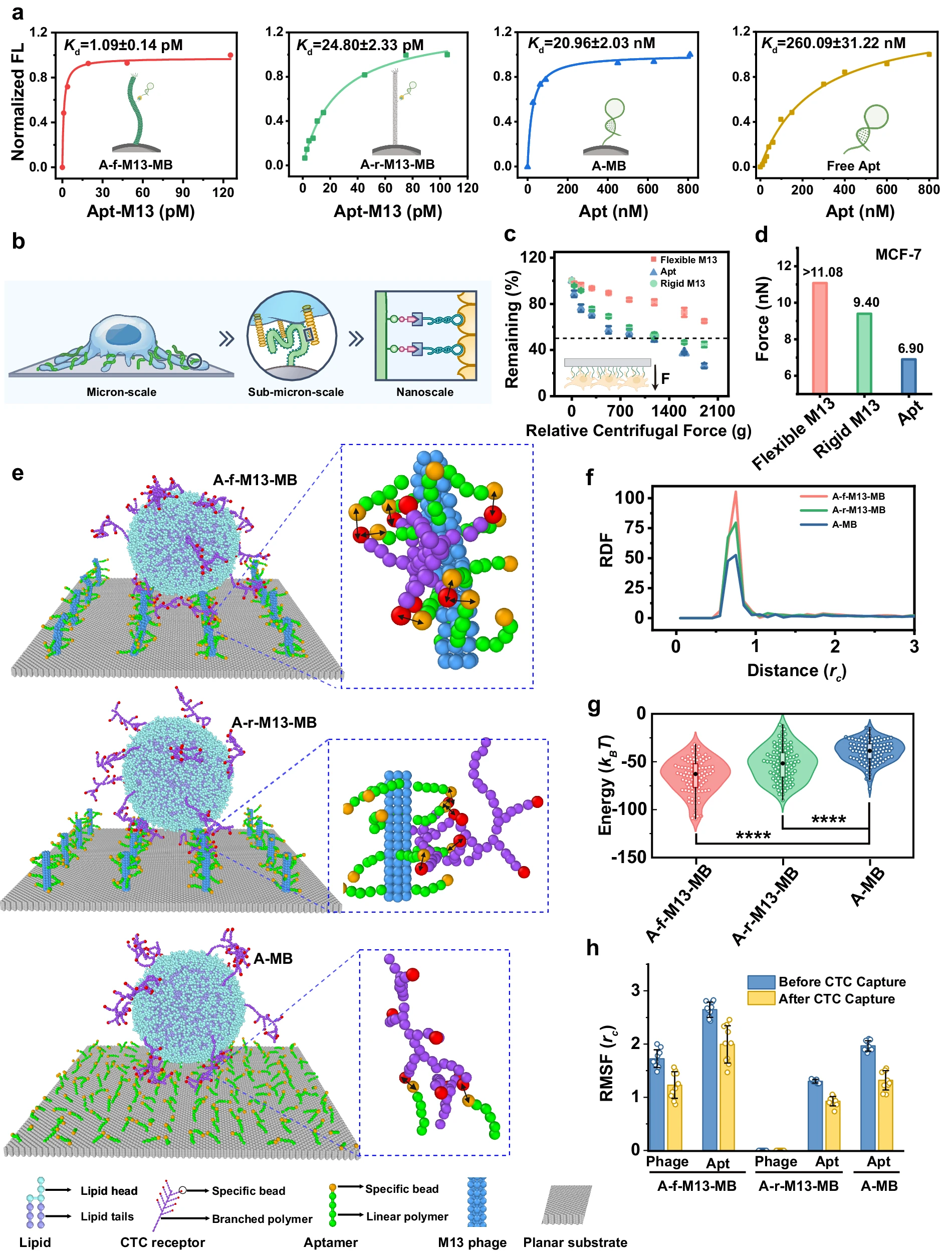
灵活的M13增强型CTC捕获性能。
Twisty M13有助于减少 WBC吸附
为了评估工程表面的防污性能,团队采用了人类伯基特淋巴瘤拉莫斯细胞,作为白细胞(WBC)的模型。实验结果显示,在孵化30分钟后,只有大约1,354个白细胞粘附在A-f-M13-MB上。与此形成鲜明对比的是,与A-r-M13-MB和A-MB结合的白细胞数量,分别高出7.5倍和8.9倍。相应地,基于离心的细胞粘附检测,揭示了A-f-M13-MBs的白细胞结合力,显著降低至8.64pN。值得注意的是,该力仅占观察到的A-r-M13-MB和A-MB结合力的1/3和1/6。
为了在分子水平上,更深入地了解这3个表面的不同防污特性,团队采用了DPD模拟。A-MB的RDF峰最高,而相互作用最低,从而使白细胞吸附在能量上,对A-MB最有利。另一方面,A-f-M13-MB和A-r-M13-MB的RDF峰和相互作用的能量几乎相同。这意味着白细胞吸附的能量概率相似。然而,当白细胞吸附到MB表面时,M13噬菌体和配体的自由度,都受到限制。重要的是,对于A-f-M13-MB,M13噬菌体和适配体的自由度都降低了;而对于A-r-M13-MB,只有适配体的自由度被削弱了。因此,A-f-M13-MB的熵项(-TΔS)高于A-r-M13-MB。熵项在决定相互作用自由能方面,比能量项更重要。这种动态,导致白细胞吸附在A-f-M13-MB表面上的熵优势,不如A-r-M13-MB。
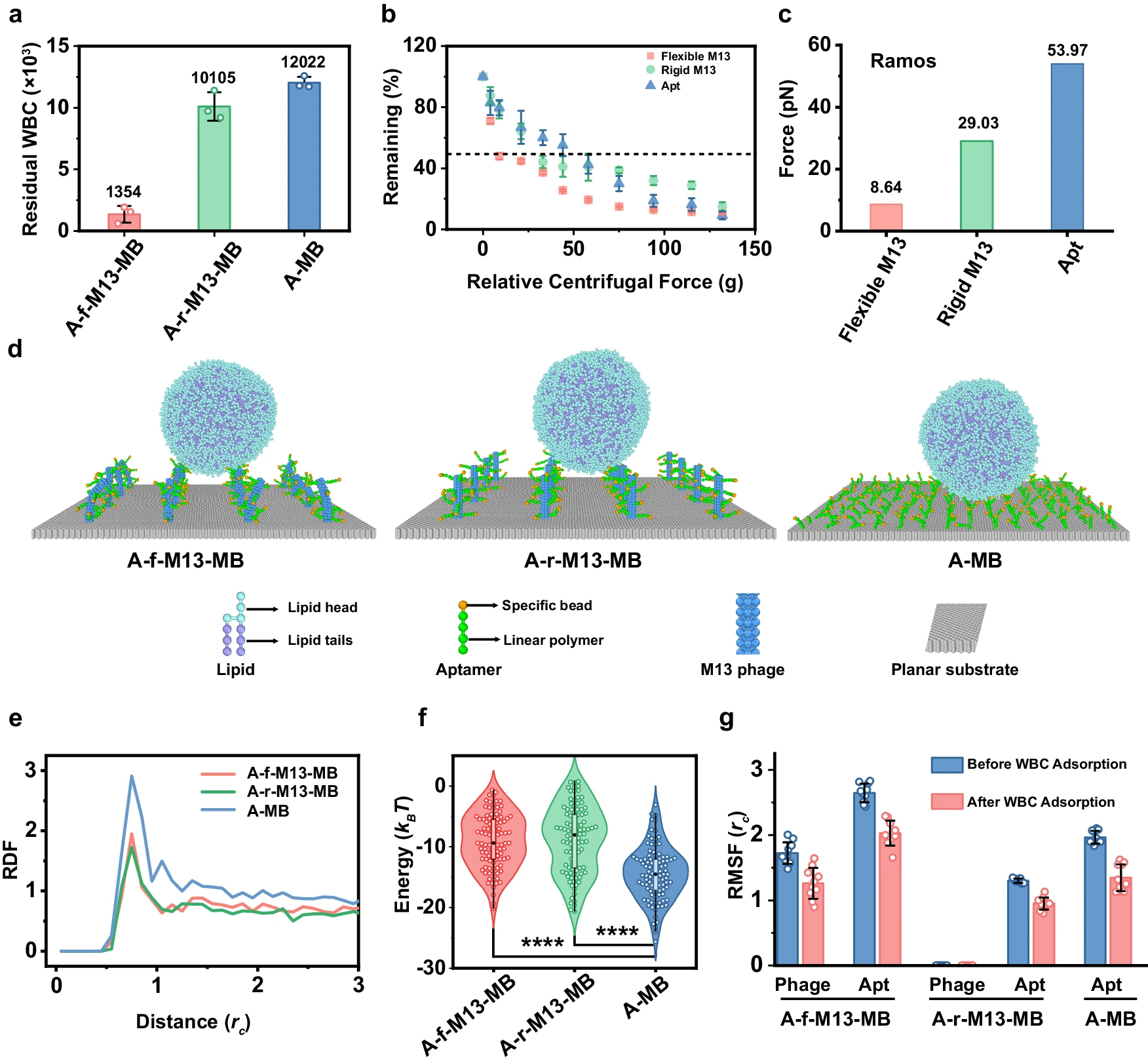
柔性M13减少了白细胞的非特异性吸收。
研究结论
03
本研究揭示了病毒修饰固体表面的机械特性,在分离稀有细胞(如 CTC)方面的重要作用,包括靶细胞结合亲和力,和减轻与非靶细胞(如 WBC)的非特异性作用。病毒纳米纤维固有的柔韧性和可变形性,赋予固体表面自调节能力,从而通过能量驱动的过程,放大纳米纤维上的适配体,与靶细胞上的受体之间的多价作用。此外,与刚性纳米纤维相比,固体表面的这些柔性病毒纳米纤维,对非靶细胞的非特异性吸附,显著减少。这归因于熵驱动的机制,这是由于柔性纳米纤维,相对于刚性纳米纤维的自由度,损失更大。团队的方法,依赖于柔性病毒纳米纤维,优于基于防污聚合物的传统方法。因为它避免了与此类聚合物相关的潜在缺点,同时在固体表面,为靶细胞的特定配体识别,提供了必要的空间。这种基于噬菌体的策略,不仅引入了基于亲和力的固体生物检测;而且,还利用了对靶-配体相互作用的更深入的机理理解,从而提高了CTC分离的效率。
参考资料:
https://www.nature.com/articles/s41467-024-50064-y#Sec1
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发