靶向“最毒乳腺癌”!南京医科大学合作发文:揭示乳腺癌治疗新策略
| 导读 | 在哺乳动物中,赖氨酸甲基转移酶2D (KMT2D)介导组蛋白H3赖氨酸4 (H3K4me1)单甲基化。H3K4me1标记参与建立活性染色质结构以促进基因转录。然而,在三阴性乳腺癌(TNBC)进展中,kmt2d介导的H3K4me1标记调控基因表达的确切分子机制尚不清楚。 |
近日,南京医科大学与南京大学研究人员合作共同在期刊《Clinical And Translational Medicine》上发表了题为“KMT2D-mediated H3K4me1 recruits YBX1 to facilitate triple-negative breast cancer progression through epigenetic activation of c-Myc”的研究论文,研究结果表明,kmt2d介导的H3K4me1招募YBX1,通过表观遗传激活c-Myc和SENP1促进TNBC的进展。这些结果揭示了组蛋白标记和基因调控在TNBC进展中的关键相互作用,从而为靶向KMT2D-H3K4me1-YBX1轴治疗TNBC提供了新的见解。

https://onlinelibrary.wiley.com/doi/full/10.1002/ctm2.1753
背景知识
01
三阴性乳腺癌(TNBC)是全球女性中最常见的癌症,也是癌症相关死亡的主要原因。经济发展带来的各种潜在危险因素使乳腺癌的发病率和死亡率迅速上升。这些因素包括生殖模式的变化、早期筛查方法不足以及获得治疗选择的机会有限。近几十年来,人们对三阴性乳腺癌的发病机制进行了大量研究,尤其关注与癌基因激活和抑癌基因失活相关的表观遗传事件。例如,肿瘤抑制基因,如p16INK4A, CCND2, CDH1, BRCA1, ER和RARβ2的启动子区的CpG岛表现出高甲基化,从而导致基因表达沉默,促进肿瘤的发生和发展。组蛋白H3第4、9和27位赖氨酸残基甲基化在TNBC的基因激活或失活中起关键作用。需要进一步的研究来充分把握基因调控中的表观遗传变化,开发TNBC的新治疗方法。
赖氨酸甲基转移酶2D (KMT2D),也称为混合谱系白血病4 (MLL4),在哺乳动物中催化组蛋白H3第4位赖氨酸(H3K4me1)的单甲基化,参与建立活跃的染色质结构和调节特定基因的转录。KMT2D与各种转录因子和辅调节因子相互作用,以维持不同类型细胞中活跃的染色质状态。敲低KMT2D可以阻碍H3K4me1在特定染色质区域的沉积,从而导致抑制性染色质状态和随后的转录失活。功能研究表明,KMT2D通过与h3k4me1相关的转录调控以及PI3K/Akt、Notch和Wnt通路积极参与多种细胞过程的调节,如细胞生长、胚胎分化和肿瘤的发生。KMT2D在多种人类恶性肿瘤中异常表达和突变,包括淋巴瘤、卵巢癌、前列腺癌、膀胱癌、乳腺癌和肺癌。
作为一种多功能转录因子,YBX1在基因调控、RNA加工和染色质破坏中发挥作用。它被认为是一种致癌因子,促进肿瘤的发生和发展。研究人员发现YBX1在癌细胞中通过与ABCB1启动子区结合来激活ABCB1基因的表达,从而促进恶性进展和耐药。最近,研究人员报道蛋白质精氨酸甲基转移酶5 (PRMT5)催化的YBX1甲基化是NF-κB激活和结直肠癌进展所必需的。YBX1在膀胱癌、卵巢癌和乳腺癌等多种肿瘤中高表达,提示YBX1可能是不良预后的预测指标。敲低YBX1导致乳腺癌细胞周期调控基因的抑制,从而抑制肿瘤的生长。
KMT2D和YBX1促进TNBC细胞增殖和迁移
02
鉴于H3K4me1在哺乳动物中主要由KMT2D催化,研究人员接下来探究了KMT2D在乳腺癌细胞中的作用。使用两个TNBC细胞系,研究人员沉默了KMT2D,并发现KMT2D敲低细胞的生长、迁移和侵袭显著减少,这与先前报道的结果一致。为了研究KMT2D对其甲基转移酶活性的依赖性,研究人员根据先前发表的方案生成了一系列截短的KMT2D表达载体。如图1A所示,KMT2D- c包含KMT2D的c端4507 ~ 5537个氨基酸,KMT2D- f是包含PHD结构域和KMT2D的c端的融合蛋白,KMT2D- fc1523a是KMT2D- f的失功能突变体。与之前的研究结果一致,在MDA-MB-231细胞中,过表达KMT2D-F显著提高了H3K4me1水平,而在KMT2D-C和KMT2D-FC1523A中没有观察到这种作用。与过表达KMT2D-C和过表达kmt2d - fc1523a的MDA-MB-231细胞相比,过表达KMT2D-F促进了细胞的生长和迁移。基于这些结果,KMT2D以甲基转移酶活性依赖的方式促进TNBC细胞的生长和迁移。
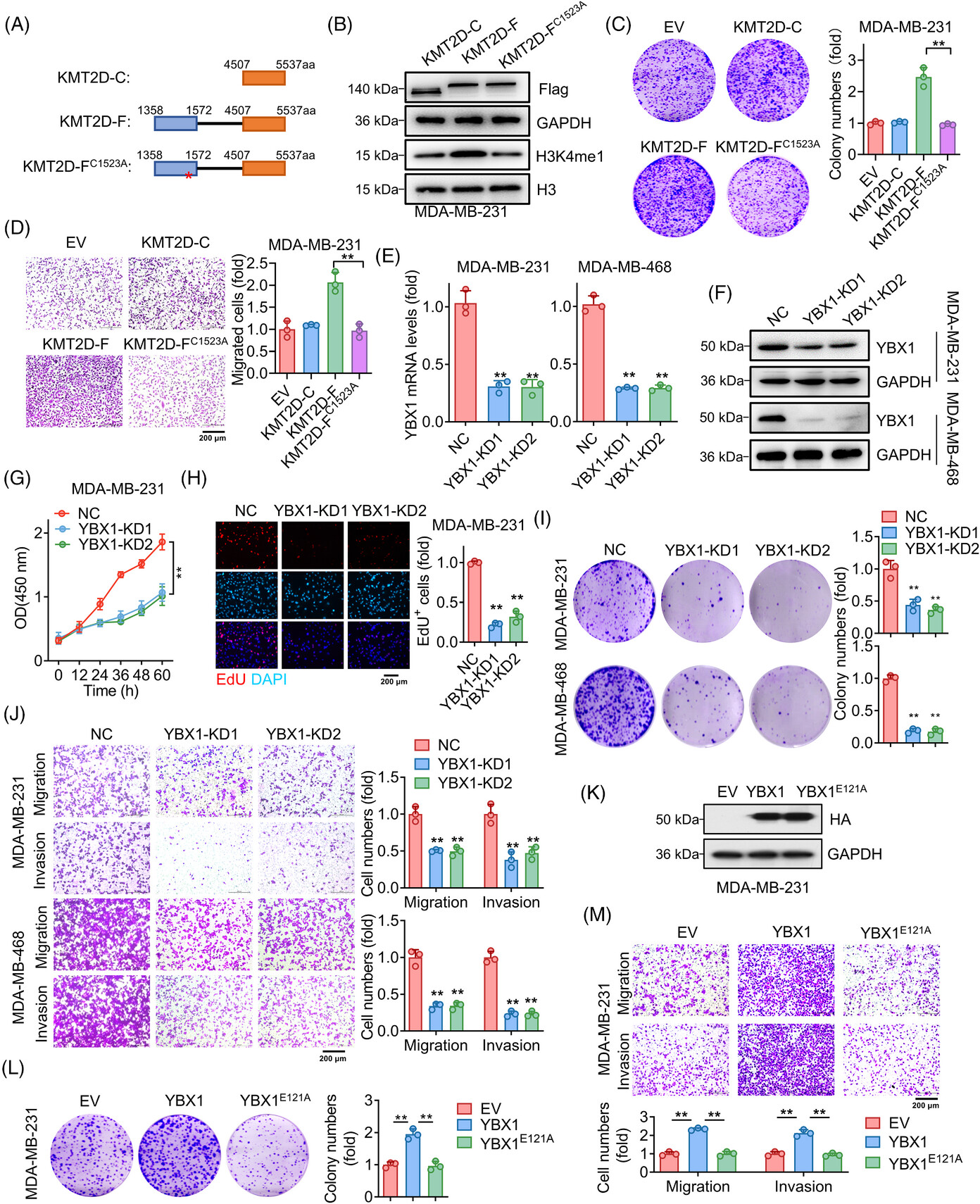
图1:KMTD和YBX1促进TNBC细胞增殖和迁移
由于研究人员发现YBX1是kmt2d介导的H3K4me1的潜在“读取器”,研究人员接下来研究了YBX1在TNBC细胞中的作用。沉默YBX1对TNBC细胞增殖有明显抑制作用。此外,在迁移实验中,YBX1敲低降低了TNBC细胞的迁移和侵袭。相反,过表达YBX1而非YBX1- e121a的MDA-MB-231细胞的迁移和增殖能力增强。KMT2D和YBX1参与影响H3K4me1标记的书写和读取对三阴性乳腺癌细胞的增殖、迁移和侵袭至关重要。
敲低KMT2D或YBX1减弱乳腺肿瘤的生长和转移
03
接下来,研究人员利用小鼠乳腺癌模型研究了KMT2D和YBX1的作用。在小鼠异种移植模型中,敲低KMT2D或YBX1抑制肿瘤生长。敲低KMT2D或YBX1基因后,MDA-MB-231移植瘤的重量显著下降。此外,来自KMT2D和ybx1敲低细胞的异种移植瘤中,c-Myc和SENP1的表达水平显著降低。此外,KMT2D-或ybx1 -敲低组的肿瘤组织显示Ki-67表达降低,Ki-67是细胞增殖的一个明确标志物。
研究人员利用AAV病毒在MMTV-PyMT转基因小鼠(MMTV-KMT2D-KD或MMTV-YBX1-KD)的乳腺组织中敲低KMT2D和YBX1,以测试它们在乳腺癌中的治疗潜力。研究人员通过检测GFP荧光来确认AAV感染的效率。令人惊讶的是,AAV-KMT2D-KD和AAV-YBX1-KD小鼠均表现出肿瘤生长和肺转移的减少。此外,H&E染色和显微镜检查显示,与对照组小鼠相比,MMTV-KMT2D-KD和MMTV-YBX1-KD小鼠的肺转移结节显著减少。同样,MMTV-KMT2D-KD和MMTV-YBX1-KD小鼠的乳腺肿瘤组织中SENP1、c-Myc和Ki67的表达水平均降低。总之,这些发现表明敲低KMT2D和YBX1可抑制乳腺癌的生长和转移。
研究小结
04
总之,研究人员发现YBX1是TNBC细胞中的H3K4me1-结合蛋白。KMT2D与YBX1协同作用,通过表观遗传激活c-Myc和SENP1转录促进TNBC进展。这些发现揭示了TNBC进展过程中重要的表观遗传调控与转录调控之间的相互作用,从而支持靶向KMT2D-H3K4me1-YBX1轴治疗乳腺癌的策略。(转化医学网360zhyx.com)
参考资料:
https://onlinelibrary.wiley.com/doi/full/10.1002/ctm2.1753
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发