【Nature子刊】华西医院李艳萍团队揭示靶向肠道调节肥胖和胰岛素抵抗的新途径
| 导读 | 团队的研究结果表明,肠道选择性PXR激活,调节B3galt5表达并维持代谢稳态,使其成为肥胖症的潜在治疗策略。 |
2024年7月14日,四川大学华西医院国家老年疾病临床医学研究中心李艳萍团队在期刊《Nature Communications》上发表了题为“B3galt5 functions as a PXR target gene and regulates obesity and insulin resistance by maintaining intestinal integrity”的研究论文。团队的研究数据表明,选择性激活肠道PXR,通过上调肠道B3galt5,来缓解饮食诱导的肥胖和胰岛素抵抗。

https://www.nature.com/articles/s41467-024-50198-z
研究背景
01
肥胖症的患病率,在世界范围内不断上升,大大增加了其他相关慢性代谢疾病的全球负担,如2型糖尿病、非酒精性脂肪性肝病和心血管疾病。越来越多的证据表明,肥胖和相关代谢综合征的发生,主要集中在众多遗传基因和环境因素之间的复杂相互作用上。
孕烷X受体(PXR)最初被确定为调节药物代谢的异生素受体,因为它在肝脏和肠道中高度表达。科学界已经证明PXR在葡萄糖、脂质和胆汁酸代谢中,起着至关重要的作用,使其成为肥胖症和2型糖尿病的潜在治疗靶点。实验结果表明,PXR在不同组织中,可能具有多种调节机制或不同的功能。尽管PXR在肠道中高度表达,但肠道PXR对代谢疾病的功能,在很大程度上仍是未知的。
本研究提供了第一个证据,证明TBC对PXR的肠道选择性激活,可以缓解HFD喂养的小鼠的肥胖和胰岛素抵抗。从机制上讲,团队发现B3galt5介导粘液O-糖基化,并使其抵抗蛋白水解,从而支持肠道屏障的完整性和功能。B3galt5的全身和肠道特异性敲除,均加重了HFD诱导的肥胖、胰岛素抵抗和炎症。B3galt5敲除,也消除了TBC对肥胖和胰岛素抵抗的保护作用。团队的结果,证明了PXR-B3galt5轴在维持代谢稳态中的重要性,使其成为肥胖症的潜在治疗策略。
研究进展
02
肠道PXR的激活,可改善HFD诱导的肥胖和胰岛素抵抗
为了探索肠道PXR对代谢疾病的潜在功能,团队首先测试了柠檬酸三丁酯(TBC)是否是先前报道的肠道选择性PXR激动剂。实验结果表明,TBC仅增加肠道中著名的PXR靶基因Cyp3a11的表达。相比之下,孕烯醇酮16α-甲腈 (PCN) 是一种全身PXR激动剂,可增加肝脏和肠道中Cyp3a11的表达。TBC增加Cyp3a11,似乎依赖于PXR,因为PXR的消融,完全消除了其作用。这些结果证实了,TBC确实是肠道PXR的选择性激动剂。
为了评估肠道PXR对代谢紊乱的作用,团队以0.05%(w/w)的浓度,喂食补充了HFD的TBC的WT小鼠12周。在HFD喂养时,TBC处理,导致体重显著降低。TBC治疗还改善了葡萄糖耐量和胰岛素耐量。TBC的作用依赖于PXR,因为PXR的消融,完全消除了TBC降低的体重,并提高了胰岛素敏感性。这些结果表明,肠道PXR的选择性激活,可以缓解HFD喂养小鼠的肥胖和胰岛素抵抗。
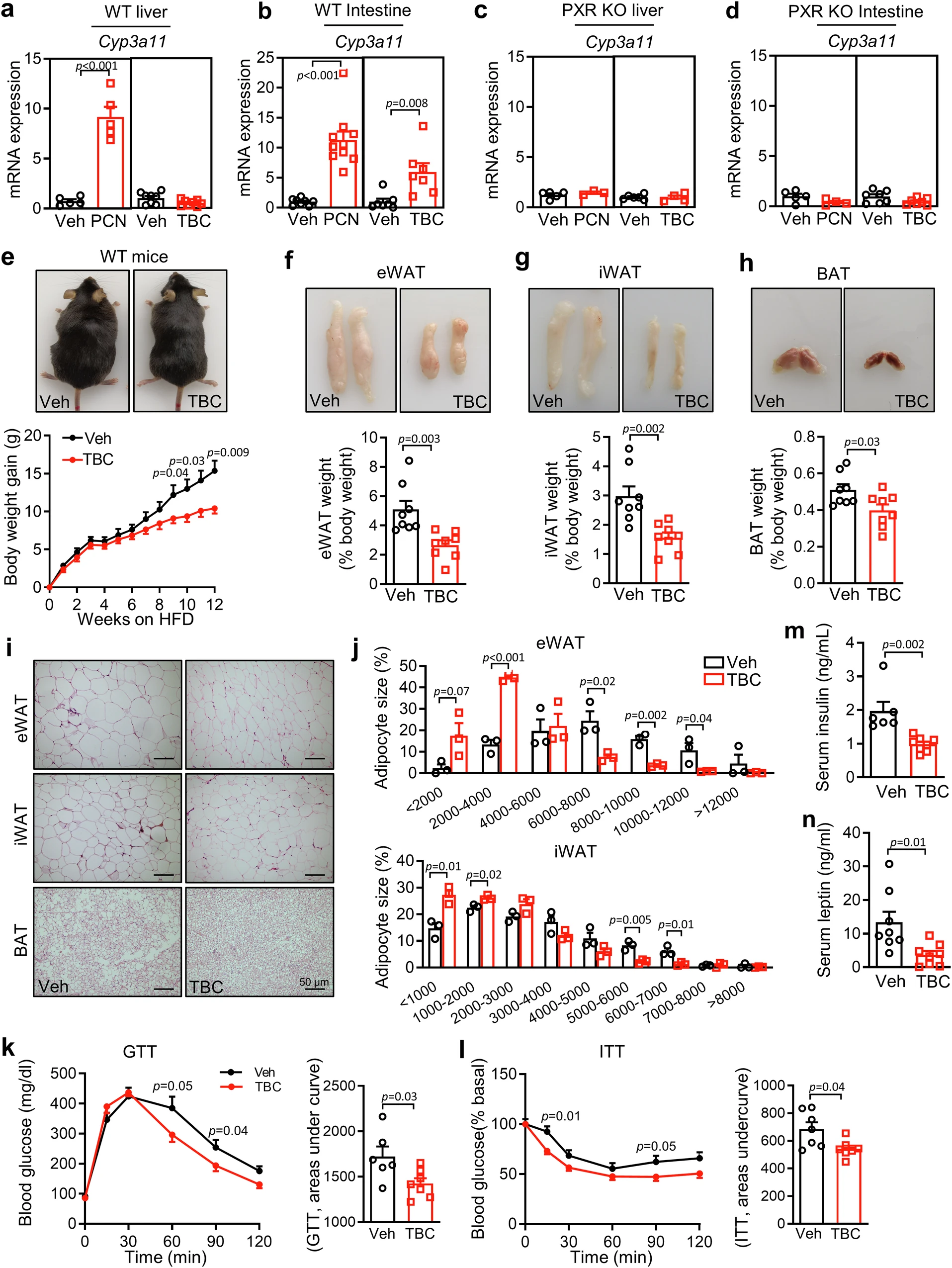
TBC是一种肠道选择性PXR激动剂,可改善HFD诱导的肥胖和胰岛素抵抗。
肠道特异性B3galt5敲除,会加重HFD诱导的肥胖、胰岛素抵抗和炎症
在B3galt5 中,B3galt5在肠道所有部分的蛋白表达,均显著降低。B3galt5的eWAT中,M1与M2巨噬细胞的比例显著增加。实验结果表明,肠道中B3galt5的特异性消融,会导致严重的HFD诱导的肥胖、胰岛素抵抗和炎症,这与B3galt5全身敲除一致。此外,肠道特异性B3galt5敲除,导致肠道屏障受损,因此可能导致肥胖、胰岛素抵抗和炎症的恶化。
B3galt5介导肠道PXR激活,对肥胖小鼠的有益作用
目前为止,研究结果支持B3galt5是肠道PXR的直接靶基因,可调节肥胖的进展。TBC的有益作用取决于B3galt5,证实了B3galt5是传导肠道PXR功能的信息传递者,PXR-B3galt5轴对肠道屏障的维持至关重要,从而防止肥胖和炎症的发生。
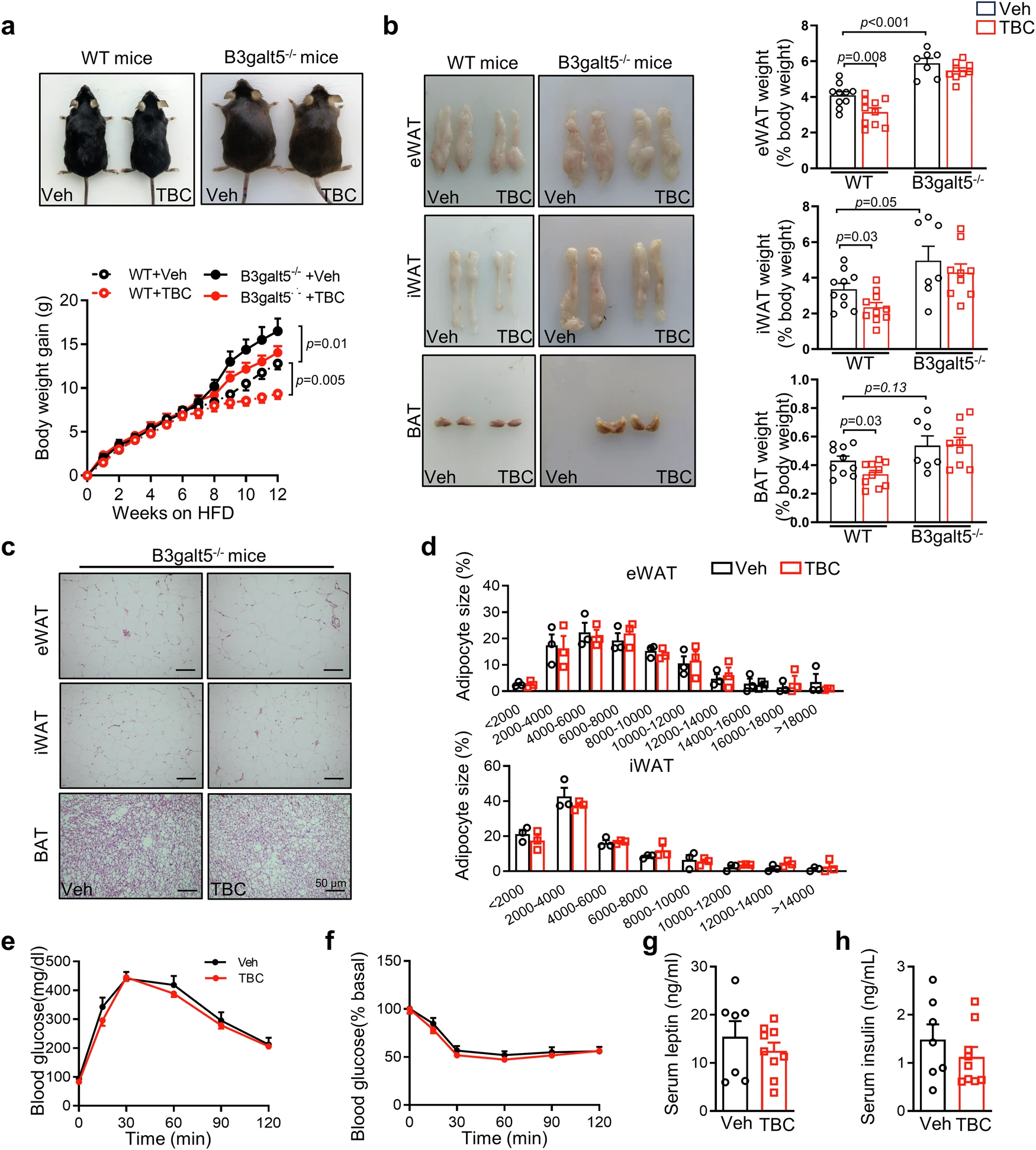
B3galt5介导肠道PXR激活对肥胖小鼠的影响。
研究结论
03
在本研究中,团队提供了第一个证据,证明肠道PXR的选择性激活,可以通过上调肠道B3galt5表达,来缓解饮食诱导的肥胖和胰岛素抵抗。团队发现,B3galt5是PXR的直接转录靶标。在全身B3galt5基因敲除小鼠中,团队发现,HFD攻击后肥胖、胰岛素抵抗和组织炎症加重。此外,B3galt5在结肠中高表达,肠道特异性B3galt5消融小鼠,也表现出更严重的代谢紊乱,以及HFD的肠道屏障完整性。B3galt5是肠道PXR激活,对HFD诱导的代谢紊乱的有益作用所必需的。基于这些观察结果,团队得出结论,肠道PXR可能通过提供功能性肠道屏障,在代谢疾病中发挥重要作用,而B3galt5是关键的执行者。
在过去的二十年中,人们一直在探索PXR在葡萄糖和脂质代谢中的作用。通过使用肠道选择性PXR激活剂TBC,团队首先提供了肠道中PXR的选择性激活,改善HFD诱导的肥胖和胰岛素抵抗的证据。表明肠道PXR在代谢紊乱中具有保护作用,这与肝脏PXR的有害作用不同。在肠道中选择性激活PXR及其下游靶点,以改善肥胖和相关代谢紊乱,可能具有更多的临床意义,副作用最小。
尽管有越来越多的证据表明,PXR激活可以调节肠粘膜屏障的炎症,或能够改善硫酸葡聚糖钠诱导的炎症性疾病;然而,在肠道中执行PXR有益作用的靶向基因,尚未完全确定。使用来自PCN治疗的小鼠肠道的RNA-seq数据,团队发现,B3galt5是进一步评估的主要候选者之一。在TBC刺激下,PXR敲除未能提高B3galt5的表达,并且,B3galt5启动子的突变,破坏了与PXR的相互作用。这证实了,B3galt5是肠道PXR的直接和特异性转录靶标。
B3galt5与癌症相关蛋白的糖基化有关,因为它能够催化鞘脂球苷-4(Gb4)的半乳糖基化形成球苷-5(Gb5),也称为SSEA3,一种在乳腺癌干细胞中高度表达的常见癌症特异性标志物。B3galt5还可以催化肿瘤标志物CA19-9的合成,CA19-9在小鼠胰腺炎和胰腺癌的发展中,起着重要作用。在本研究中,团队已经证实,B3galt5是PXR的靶基因,并且可以通过PXR激活诱导。当高脂肪饮食受到挑战时,肥胖、胰岛素抵抗和炎症加剧。
利福昔明是一种人肠道选择性PXR激动剂,具有广谱抗菌活性。在临床上,利福昔明主要用于治疗细菌性肠道感染、肝性脑病和炎症性肠病。在本研究中,团队已经证实,PXR-B3galt5轴通过调节粘蛋白的O-糖基化,作为肥胖和相关代谢紊乱的治疗靶点。作为临床用药,利福昔明是否能缓解肥胖及其潜在机制,有待进一步研究。
总之,研究数据表明,选择性激活肠道PXR,通过上调肠道B3galt5,来缓解饮食诱导的肥胖和胰岛素抵抗。B3galt5作为PXR的下游靶基因,通过影响结肠粘液的O-糖基化,来调节肥胖、胰岛素抵抗和全身炎症的作用。因此,团队证实了,通过靶向肠道PXR或B3galt5调节肠道粘液屏障,是预防和治疗肥胖和相关代谢紊乱的有吸引力的策略。
参考资料:
1.James, S. L. et al. Global, regional, and national incidence, prevalence, and years lived with disability for 354 diseases and injuries for 195 countries and territories, 1990–2017: a systematic analysis for the Global Burden of Disease Study 2017. Lancet 392, 1789–1858 (2018).
2.Seravalle, G. & Grassi, G. Obesity and hypertension. Pharm. Res 122, 1–7 (2017).
3.Upadhyay, J., Farr, O., Perakakis, N., Ghaly, W. & Mantzoros, C. Obesity as a Disease. Med Clin. North Am. 102, 13–33 (2018).
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发