【Nature子刊】复旦大学刘天舒团队:免疫抵抗新发现及胃癌治疗潜在靶点
| 导读 | 近年来,免疫治疗,尤其是PD-1抗体显著改善了胃癌患者的预后。尽管取得了这些进展,但一些患者对治疗的应答不佳,这凸显了了解耐药机制和开发治疗效果预测标志物的必要性。 |
7月13日,复旦大学刘天舒团队在期刊《Cell Death&Disease》上发表了研究论文,题为“IL-4/IL-4R axis signaling drives resistance to immunotherapy by inducing the upregulation of Fcγ receptor IIB in M2 macrophages”,本研究回顾性分析106例接受一线免疫治疗联合化疗的ⅳ期胃癌患者的资料。通过比较对PD-1抗体治疗耐药和敏感患者的血浆细胞因子水平,研究人员发现耐药患者的IL-4表达水平升高。研究表明,IL-4诱导巨噬细胞代谢改变,并激活PI3K/AKT/mTOR通路。这一改变促进了巨噬细胞的ATP生成,增强糖酵解,增加乳酸生成,并上调FcγRIIB表达。这些变化最终导致胃癌中CD8+ T细胞功能障碍和对PD-1抗体治疗的抵抗。这些发现强调了IL-4诱导的巨噬细胞极化和代谢重编程在免疫抵抗中的作用,并验证了IL-4作为改善胃癌患者治疗结果的潜在靶点。

https://www.nature.com/articles/s41419-024-06875-4
背景知识
01
根据2020年全球癌症统计数据,胃癌发病率居全球第5位,死亡率居全球第4位。由于早期胃癌的症状不典型以及胃癌筛查普及程度不够,据报道有1 / 3的患者在初诊时已发生远处转移,这意味着此类患者短期内无法获得根治性手术,只能采取全身抗肿瘤治疗。近年来,以免疫检查点抑制剂为代表的免疫治疗,尤其是PD-1抗体,有效改善了胃癌患者的预后。由于免疫系统的激活和杀伤作用在肿瘤微环境中受到抑制,通过免疫治疗恢复CD8+T细胞的功能是目前胃癌领域的研究热点。随着肿瘤免疫学研究的不断发展,PD-1、CTLA-4和PD-L1均已成为相对成熟的免疫治疗靶点,其中PD-1抗体是胃癌免疫治疗中最常用的靶点。
PD-1是已知的免疫检查点之一,主要表达于活化的T细胞表面。PD-1及其配体PD-L1 (CD274)或PD-L2 (CD273)在肿瘤细胞的免疫逃逸中发挥关键作用,可显著抑制T细胞的功能,而肿瘤可通过PD-L1/PD-L2的高表达抵抗免疫系统的攻击。通过阻断PD-1与其配体之间的相互作用,免疫系统可以正常识别和杀伤肿瘤,从而增强抗肿瘤活性,这是免疫治疗的核心。
目前,多项临床研究表明,免疫检查点阻断治疗可有效增强胃癌患者的抗肿瘤活性,改善预后。研究证实,与单纯化疗组相比,一线免疫治疗联合化疗可显著改善全人群晚期胃癌患者的预后,中位OS延长2.9个月,客观缓解率(ORR)由48.4%提高至58.2%,缓解持续时间(DOR)显著延长。研究还证实,一线化疗联合纳武利尤单抗也可使晚期胃癌或胃食管癌患者的OS或ORR显著获益。临床研究结果证明,帕博利珠单抗联合化疗和her2靶向治疗可显著抑制肿瘤,提高患者客观缓解率(ORR),达到74.4%。这些结果提示,免疫治疗将给胃癌患者的治疗带来巨大变化,晚期胃癌的治疗将从化疗和靶向治疗向免疫联合治疗转变。
IL-4抑制体内胃癌PD-1抗体作用
02
为了进一步确定IL-4对抗PD-1治疗抵抗的影响,研究人员在接受MFC细胞的异种移植615小鼠中检测了PD-1抗体的抗肿瘤作用。与PD-1抗体组相比,IL-4受体小鼠移植瘤生长表现出明显的抗PD-1治疗耐药表型。
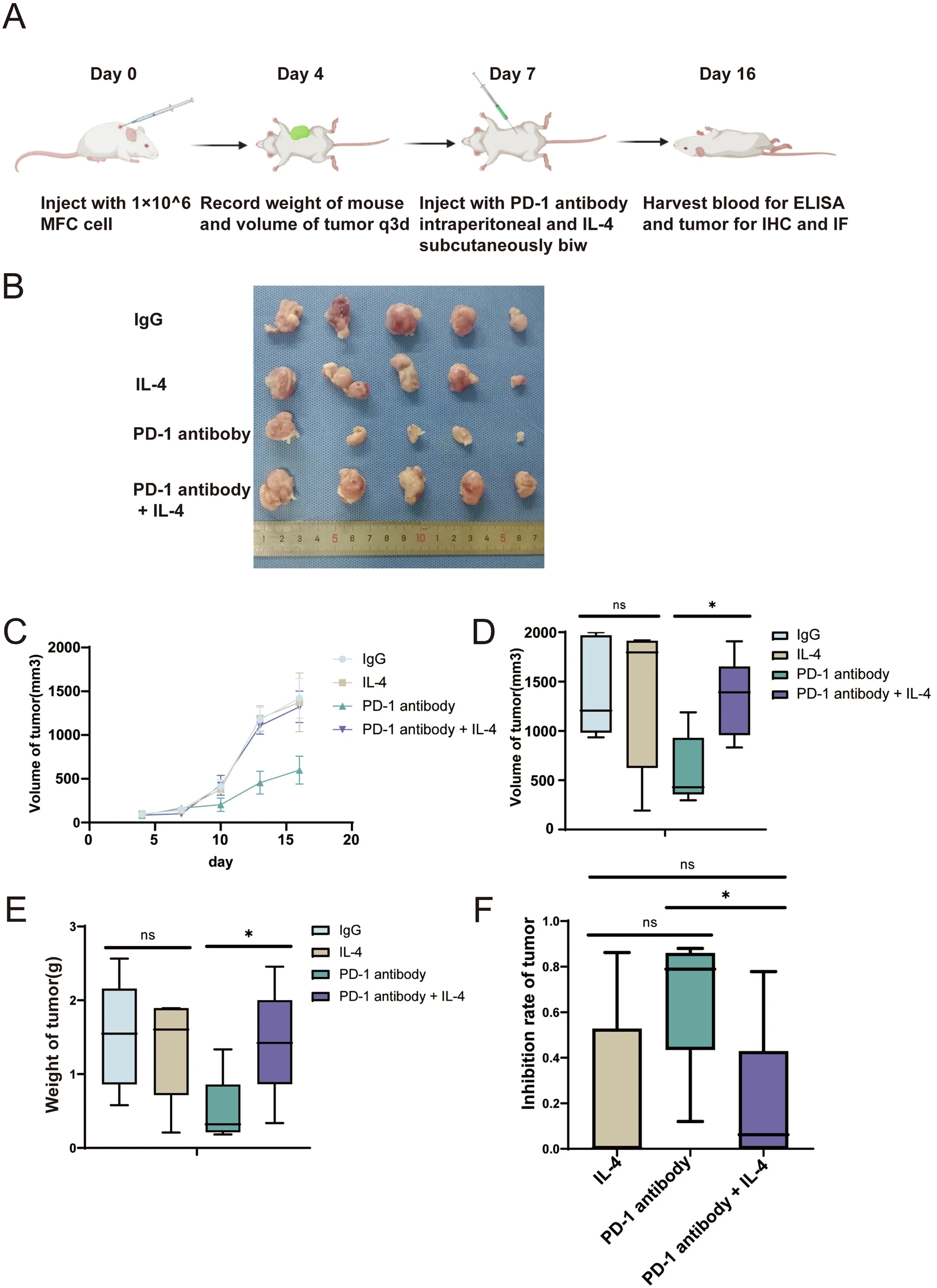
IL-4在体内抑制胃癌PD-1抗体的疗效
IL-4与胃癌组织中巨噬细胞M2型极化相关
03
研究人员在小鼠胃癌模型中发现了大量的巨噬细胞浸润,这些巨噬细胞被肿瘤微环境中的趋化因子和细胞因子募集,清除巨噬细胞可以抑制体内肿瘤的生长。因此,研究人员利用算法对TCGA中胃癌的RNA-seq数据进行分析,发现与正常组织相比,肿瘤中巨噬细胞浸润明显增加,伴有Treg细胞浸润增加和浆细胞浸润减少,证实了胃癌的免疫微环境处于免疫抑制状态。研究人员分析了TCGA胃癌数据中免疫细胞浸润与患者预后的关系,发现巨噬细胞与患者生存显著负相关。
此外,对TCGA的胃癌RNA-seq数据进行xCELL免疫浸润分析发现,随着IL-4/IL-4R轴的激活,M2型巨噬细胞浸润增加,Th1和Th2细胞浸润减少。对TCGA的胃癌测序数据分析显示,IL-4R的表达与巨噬细胞的浸润强相关。
研究人员分析了单细胞测序数据GSE163558,并使用IL-4R的表达水平来代表每个细胞上IL-4/IL-4R轴的激活水平。研究人员发现,在从胃癌组织中分离出的13个细胞亚群中,IL-4R主要表达于巨噬细胞、单核细胞、基质细胞和上皮细胞。对巨噬细胞进行亚群分析后发现,IL-4R主要在M2型巨噬细胞中高表达。研究人员对巨噬细胞亚群分析发现,M1型和M2型巨噬细胞处于巨噬细胞发育的晚期,随着IL-4R表达的增加,巨噬细胞逐渐向M2型巨噬细胞转化。
此外,研究人员在GSE163558中检测了IL-4/IL-4R轴下游分子PI3K、AKT1、AKT2和STATA6的表达。研究人员发现它们在巨噬细胞中表达。同时,对巨噬细胞亚群进行分析,发现PI3K、AKT1、AKT2和STATA6在M2型巨噬细胞中过表达,也证实了研究人员关于M2型巨噬细胞中IL-4/IL-4R轴激活的观点。
研究小结
04
综上所述,本研究首次发现IL-4与胃癌免疫治疗抵抗相关,并揭示了IL-4介导巨噬细胞代谢重编程的分子机制。本研究为胃癌免疫治疗提供了新的有效预测指标,为提高PD-1抗体治疗的临床疗效提供了潜在的治疗靶点和理论依据。(转化医学网360zhyx.com)
参考资料:
https://www.nature.com/articles/s41419-024-06875-4
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发