新视角!山东第一医科大学王允山/山东大学魏光伟合作揭示乳酰组在肠胃道癌症中的调控机制
| 导读 | 赖氨酸乳酸化(Kla)在许多生理过程中起着至关重要的作用。然而,Kla在胃肠道(GI)肿瘤中的癌症特异性调节需要系统的阐明。 |
2024年7月17日,山东第一医科大学王允山及山东大学魏光伟共同在《Advanced Science》 发表了题为“Integrated Lactylome Characterization Reveals the Molecular Dynamics of Protein Regulation in Gastrointestinal Cancers”的研究论文,该研究对40例胃肠道癌患者的癌变和邻近组织进行了全球乳酸酶谱分析,确定了11698个Kla位点。总的来说,这项研究为了解胃肠道癌症中的乳糖酶景观提供了宝贵的资源,这可能为这些毁灭性疾病的药物发现提供新的途径。

https://onlinelibrary.wiley.com/doi/full/10.1002/advs.202400227
背景知识
01
胃肠道(GI)癌症是一组异质性恶性肿瘤,占癌症发病率的26%以上,占所有癌症相关死亡率的35%以上。最近对个别人类消化道肿瘤的蛋白质基因组学研究揭示了肿瘤进展的广泛分子机制。然而,目前针对胃肠道肿瘤的靶向治疗手段有限,因此迫切需要开发有效的分子靶点用于诊断和治疗胃肠道肿瘤。
代谢重编程是癌症的标志之一,肿瘤细胞主要依赖糖酵解提供能量和代谢中间体来支持肿瘤生长。有氧糖酵解过程中产生的乳酸在肿瘤细胞中过度累积。随着高分辨液相色谱-串联质谱(LC-MS/MS)技术的发展,以中间代谢物为底物的各种酰基化修饰被鉴定出来。2019年,组蛋白中乳酸源性赖氨酸乳糖化(lactate-derived lysine lactylation, Kla)被鉴定为一种新型的翻译后修饰(post - translation modification, PTMs)。越来越多的证据表明,蛋白质乳糖化参与肿瘤增殖、神经系统调节、代谢调节等多种生物学过程。鉴于癌细胞中糖酵解的增强和乳酸的过度产生,乳酸的发现为乳酸在癌症进展中的重要机制提供了一个新的视角。
CBX3中的K10乳化促进CBX3与H3K9me3的相互作用和胃肠道肿瘤生长
02
通过检测CBX3和CBX3 K10la与其他数据的相关性,研究人员发现CBX3 K10la较高的肿瘤显示出蛋白质组学上氧化磷酸化代谢的下调,以及涉及剪接体、DNA复制和细胞周期的过程的上调。乳糖组分析显示CBX3 K10la水平较高的肿瘤在核糖体、剪接体和代谢通路中存在Kla上调。此外,与CBX3及其K10la显著相关的蛋白富集在多个负责基因调控的蛋白结构域。另外,CBX3与K10la的分子对接分析表明,K10的乳糖化影响CBX3的构象。这些结果表明,在胃肠道肿瘤进展过程中,K10的乳化在介导CBX3的功能和调节基因表达方面具有潜在的作用。
CBX3是一种高度保守的异染色质蛋白,通过与H3K9me3结合与染色质特异性相互作用,调节基因沉默。在本研究中,免疫共沉淀分析进一步支持了这一结果。研究表明,在胃肠道癌细胞中,内源性CBX3与H3K9me3结合。免疫共沉淀证实了野生型CBX3与H3K9me3的结合,而与CBX3K10R的结合程度较低,表明K10的乳化促进了CBX3与H3K9me3的结合。
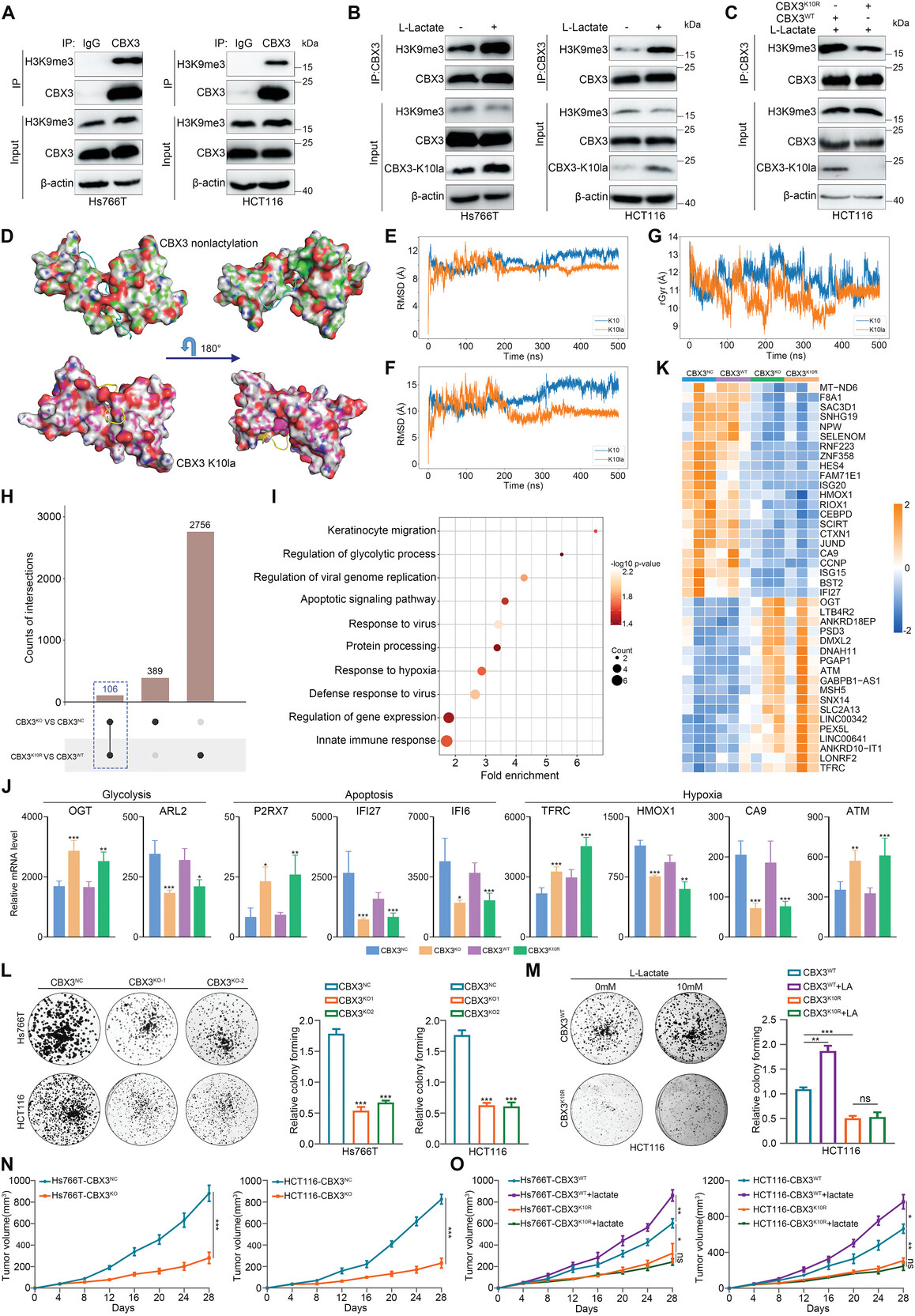
K10的乳糖化促进CBX3与H3K9me3的相互作用和胃肠道肿瘤的生长
为了更好地理解乳糖化如何促进CBX3与H3K9me3的相互作用,研究人员利用分子动力学模拟比较了未乳糖化和k10 -乳糖化CBX3的结构动力学,并分析了H3K9me3肽段的结合状态。对接分析表明,非乳化CBX3具有更动态的构象(从300 ns开始收敛),而乳化K10从200 ns开始保持稳定。此外,乳酸化CBX3的H3K9me3肽段的均方根偏差(root- meansquare deviation, RMSD)波动在7.5 Å-10 Å,远低于非乳酸化CBX3 (12.5 Å-15 Å)。此外,乳糖化CBX3中H3K9me3肽的旋转半径远小于非乳糖化CBX3,表明在模拟乳糖化CBX3结构的过程中,波动幅度减小。这些结果表明,CBX3在K10的乳糖化诱导了有利于与H3K9me3肽结合的构象变化。
为了探索CBX3 K10la与基因表达的相关性,研究人员在CBX3缺失或CBX3K10R转染的胃肠道癌细胞中进行了RNA-seq。生物信息学分析显示CBX3KO和CBX3K10R细胞株中分别有3251和615个差异表达基因(DEGs)。两组间差异表达基因的交集分析显示,CBX3KO和CBX3K10R细胞中均存在106个差异表达基因。KEGG通路分析显示,共同的DEGs分布在糖酵解、凋亡和缺氧反应等多种标志性肿瘤通路。这些结果表明,Kla可以调节CBX3介导的转录过程,而CBX3是胃肠道肿瘤进展的关键。与TCGA泛癌数据一致,研究人员的蛋白质组学数据表明CBX3在全球范围内的胃肠道肿瘤中丰度升高。Kaplan-Meier生存分析显示CBX3的表达与消化道肿瘤患者的预后呈负相关。在本研究中,研究人员研究了CBX3的功能及其乳化在胃肠道肿瘤进展中的作用。在胃肠道肿瘤中,CBX3的缺失导致了显著的增殖停滞,而CBX3K10R的恢复则显示出比CBX3WT更慢的生长。此外,将CBX3缺失或CBX3K10R转染的胃肠道癌细胞注射到裸鼠皮下。CBX3缺失或CBX3K10R表达可抑制肿瘤生长。这些结果表明CBX3的乳化在胃肠道肿瘤的进展中是至关重要的。
研究小结
04
总之,本研究表明CBX3赖氨酸10的乳酸化(CBX3 K10la)在胃肠道肿瘤中被证实显著上调,功能分析显示CBX3 K10la在调节基因表达和胃肠道肿瘤恶性过程中发挥重要作用。本研究强调了一些值得进一步研究的Kla修饰,以全面了解不同GI癌症的蛋白质调控。(转化医学网360zhyx.com)
参考资料:
https://onlinelibrary.wiley.com/doi/full/10.1002/advs.202400227
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发