“乔布斯病”神解药!复旦大学吉顺荣团队:发现胰腺肿瘤潜在联合治疗策略
| 导读 | O6-甲基鸟嘌呤DNA甲基转移酶(MGMT)从鸟嘌呤O6位置(O6- mg)去除烷基加合物并修复DNA损伤。高MGMT表达导致替莫唑胺(TMZ)治疗反应差。然而,MGMT在胰腺神经内分泌肿瘤(PanNETs)中的生物学重要性及其高表达的机制仍不清楚。 |
7月23日,复旦大学吉顺荣研究团队在期刊《Advanced Science》上发表了研究论文,题为“MEN1 Deficiency-Driven Activation of the β-Catenin-MGMT Axis Promotes Pancreatic Neuroendocrine Tumor Growth and Confers Temozolomide Resistance”,本研究发现,与配对的正常组织相比,PanNET组织中MGMT表达水平显著升高,并与PanNET患者的无进展生存(PFS)时间呈负相关。敲除MGMT抑制体内外癌细胞生长,MEN1的异位表达通过依赖β-Catenin核输出和降解的方式抑制MGMT转录。MEN1的267亮氨酸残基在调节β-Catenin-MGMT轴激活和TMZ化疗敏感性中发挥重要作用。干扰β-Catenin使肿瘤细胞对TMZ重新增敏,并显著降低高剂量TMZ处理的细胞毒性作用,而MGMT过表达抵消了β-Catenin缺陷的影响。本研究揭示了MGMT的生物学重要性以及MEN1缺陷调控其表达的新机制,从而为治疗TMZ耐药PanNETs患者提供了一种潜在的联合策略。

https://onlinelibrary.wiley.com/doi/full/10.1002/advs.202308417
背景知识
01
多发性内分泌腺瘤病1型(MEN1)综合征是一种由MEN1缺陷突变驱动的肿瘤易感性疾病,以人体器官中散发的神经内分泌肿瘤为特征。胰腺神经内分泌肿瘤(PanNETs)是一种罕见的肿瘤,发病率相对较低,在胰腺肿瘤中所占比例较小,是乔布斯当年的患病,被称为“乔布斯病”。PanNETs具有高度异质性,根据其分泌的生物活性激素分为非功能性PanNETs和功能性PanNETs。此外,2017年世界卫生组织(WHO)分类系统根据Ki67指数、有丝分裂指数和组织病理学分化程度将PanNETs分为高分化NETs和低分化胰腺神经内分泌癌。虽然MEN1、DAXX(死亡结构域相关蛋白)、ATRX (α -地中海贫血- x连锁智力障碍综合征)和肿瘤蛋白53 (TP53)的突变更有可能促进PanNET进化和进展,但肿瘤的异质性和恶性机制仍不清楚。
MEN1是PanNETs中最常见的突变基因,也是典型的抑癌基因。根据全基因组测序研究,30%以上的主要PanNETs携带体细胞突变。研究人员最近使用全外显子组测序(WES)的研究结果一致,MEN1具有最高的突变频率,并且这些突变与其功能的丧失相关,提示MEN1基因在驱动PanNET肿瘤的发生和发展中起主导作用。MEN1编码的蛋白menin在细胞质和细胞核之间穿梭。在细胞核中,menin可能作为一种必需的支架蛋白,与染色质修饰蛋白或转录因子相互作用,以响应细胞外环境的刺激(如DNA损伤剂和生长因子),并调节多种信号通路,如核因子κB (NF-κB), TGF-β(转化生长因子β), Hedgehog和DNA损伤修复信号通路。之前的研究表明,细胞质MEN1可以促进单不饱和脂肪酸代谢并减弱雷帕霉素激酶(mTOR)的活化。另外,过表达MEN1可诱导PanNET细胞铁死亡,并通过抑制SCD1来抑制癌细胞生长。更重要的是,MEN1可直接与β-Catenin结合,并通过核孔复合物依赖的核输出受体染色体区域维持蛋白1 (CRM1)将β-Catenin转运出细胞核,从而降低β-Catenin的核定位及其转录活性。因此,这些结果提示MEN1在细胞核和细胞质中均起关键作用。然而,MEN1在PanNETs中的重要功能尚未完全阐明。
高MGMT表达与PanNETs患者的不良预后相关,并促进体内肿瘤生长
02
为了评估MGMT在PanNETs中的作用,研究人员首先通过免疫组织化学染色(IHC)检测了121例PanNET样本的组织微阵列(TMAs)的表达水平。其中包括70例配对的原发肿瘤组织和癌旁正常组织样本。研究人员观察到MGMT在肿瘤组织中的表达水平高于配对的正常组织(p < 0.05)。根据欧洲神经内分泌肿瘤学会(ENETS)和第8版美国癌症联合委员会(AJCC) PanNETs分期系统,T1期患者占17.4%,T2期患者占52.1%,T3期患者占22.3%,T4期患者占8.2%。2 / 3的患者诊断时无区域淋巴结转移,其余患者至少有1处淋巴结转移。大多数患者的肿瘤处于M0期而无转移灶,14%的患者的肿瘤处于M1期而有转移灶。G1型占全部病例的30.6%,G2型占全部病例的61.2%,G3型占全部病例的8.2%。MGMT表达水平与患者分期、肿瘤部位、肿瘤分级、肿瘤大小和淋巴结转移等临床病理特征之间无显著差异。接下来,研究人员评估了MGMT表达与PanNETs患者预后之间的关系。Kaplan-Meier生存分析显示,高水平MGMT与患者的PFS时间呈负相关(log-rank P = 0.015)。由于包含罕见肿瘤数据的数据库数量较少,根据基因表达综合(GEO)数据集(GSE73338),人类PanNET组织和癌旁组织中MGMT的mRNA水平无明显差异,而对小鼠GEO数据(GSE248606)的分析表明,MGMT在PanNET组织中的表达高于癌旁组织。
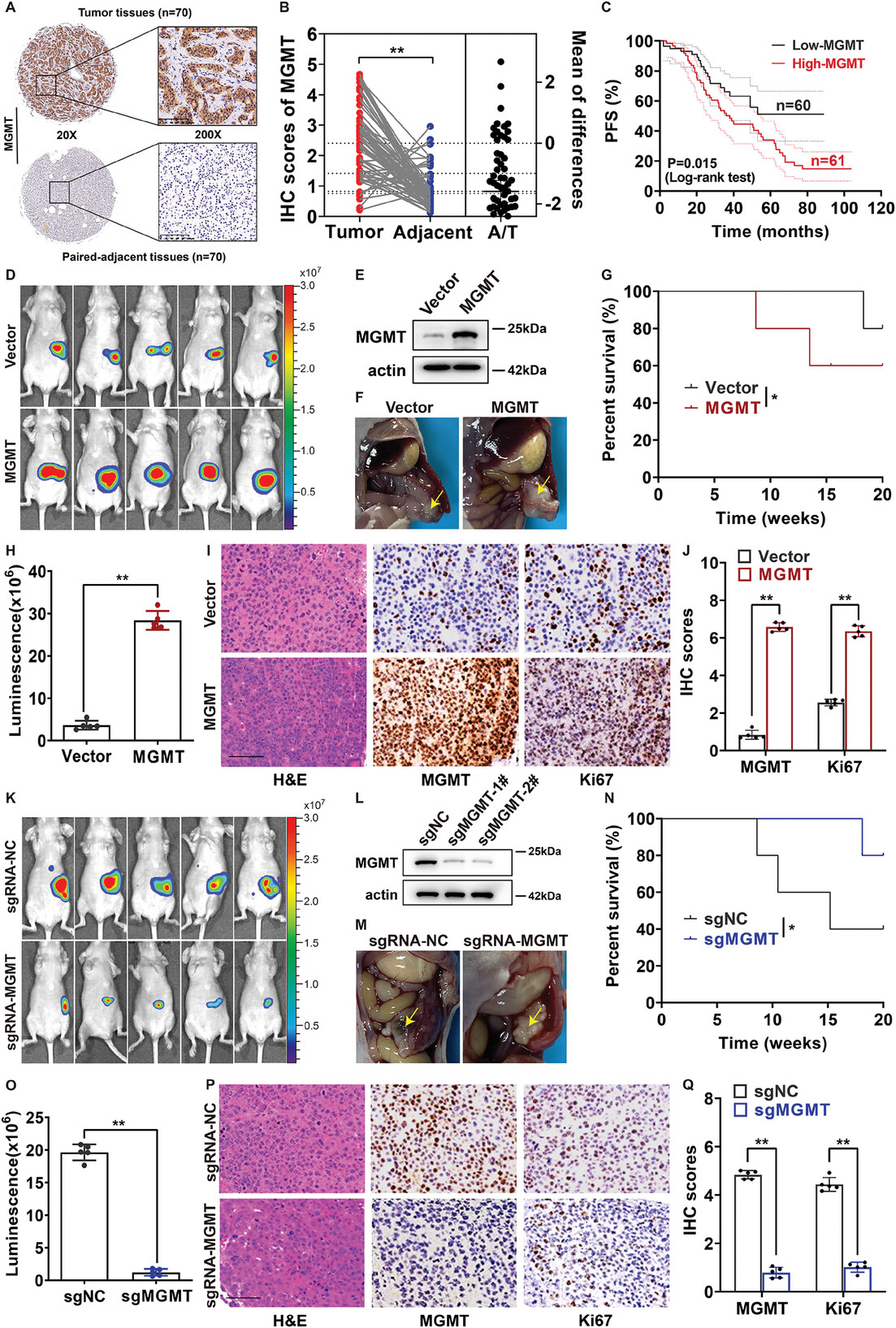
在PanNETs患者中,MGMT高水平表达与不良预后相关,并促进体内肿瘤生长
这些发现促使研究人员探究MGMT在PanNET进展中的作用。研究人员利用一种慢病毒系统构建了稳定的MGMT过表达和沉默细胞系,并评估了MGMT对肿瘤生长的影响,在异位胰腺神经内分泌瘤模型中进行。与阴性对照组相比,三周后,MGMT的过表达显著促进了异位胰腺种植肿瘤的生长(n=5,p<0.05),尤其是,对小鼠肿瘤的免疫组织化学(IHC)显示,MGMT的过表达显著增加了Ki67的表达,而与载体控制治疗相比,Ki67的表达在MGMT敲除组中较低。与阴性对照组相比,QGP-1/sgRNA-MGMT组的小鼠存活时间更长。与阴性对照细胞相比,QGP-1/sgRNA-MGMT细胞在小鼠模型中表现出Ki67表达降低。总之,这些数据表明MGMT在PanNET中发挥了致癌作用。
研究小结
03
综上所述,研究人员确定了MGMT在PanNETs中的致癌作用,并阐明了其高表达调控的机制。MEN1缺失诱导了β-Catenin的核积累和β-Catenin在MGMT启动子上的募集,从而促进MGMT转录,导致癌细胞生长和TMZ反应的破坏。MEN1的Leu267残基对于调节β-Catenin-MGMT轴的激活至关重要。干扰β-catenin-MGMT信号级联可使PanNET细胞对TMZ重新敏感。总体而言,本研究揭示了MEN1在PanNETs中调控MGMT表达的新机制,并为支持TMZ耐药PanNETs患者的治疗决策提供了潜在的联合治疗策略。(转化医学网360zhyx.com)
参考资料:
https://onlinelibrary.wiley.com/doi/full/10.1002/advs.202308417
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录

还没有人评论,赶快抢个沙发