【Lancet子刊】复旦大学附属肿瘤医院吴炅团队:特瑞普利单抗联合治疗早期三阴性乳腺癌效果显著
| 导读 | 团队进行了一项II期试验,研究一种新的辅助化学免疫治疗方案,包括早期TNBC免疫治疗的降级。 |
2024年7月26日,复旦大学附属肿瘤医院吴炅团队在期刊《Lancet eClinical Medicine》上发表了题为“Neoadjuvant anthracycline followed by toripalimab combined with nab-paclitaxel in patients with early triple-negative breast cancer (NeoTENNIS): a single-arm, phase II study”的研究论文。本研究的数据表明,短期将特瑞普利单抗添加到NAT中,可为TNBC患者提供令人鼓舞的抗肿瘤活性和良好的安全性。

https://www.thelancet.com/journals/eclinm/article/PIIS2589-5370(24)00279-7/fulltext#%20
研究背景
01
三阴性乳腺癌(TNBC)包括缺乏雌激素受体(ER)、孕激素受体(PgR)和人表皮生长因子受体2(HER2)表达的乳腺癌亚群。TNBC占新诊断乳腺癌病例的10-20%,与内脏转移发生率较高、早期复发风险较高和预后较差有关。新辅助化疗(NAC)后手术,是II-III期TNBC患者的首选治疗方法。除了可能增加肿瘤可切除性和乳房保留的可能性外,NAC后出现病理完全缓解(pCR)的患者,具有更长的无事件生存期(EFS)和总生存期。
许多当前和先前的临床试验,已经探索了如何增加TNBC患者在新辅助治疗(NAT)后,发生pCR的可能性。越来越多的证据表明,当与NAC联合使用时,免疫检查点抑制剂(ICI)比单独使用NAC的pCR率更高;然而,免疫治疗的最佳持续时间和可靠预测早期TNBC反应的生物标志物的鉴定,仍不清楚。此外,考虑到ICIs治疗的潜在长期副作用,必须紧急探索新的治疗方式,以优化程序性死亡-1(PD-1)/程序性死亡配体1(PD-L1)阻断的使用。
在具有免疫调节特性的化疗药物中,蒽环类药物作为一种启动策略特别有吸引力,可以将肿瘤免疫微环境重塑为免疫允许状态,具有更多的CD8 T细胞浸润和IFN-γ产生,可以增强ICIs的活性。此外,在TNBC转移性环境中,使用蒽环类药物诱导,可以使肿瘤对免疫相关基因上调支持的ICIs产生反应。
特瑞普利单抗是一种抗PD-1单克隆抗体,在用作一线治疗时,在转移性TNBC患者中,显示出令人鼓舞的抗肿瘤活性;然而,特瑞普利单抗在局部晚期乳腺癌的辅助治疗效果,仍有待阐明。
团队进行了一项II期试验,以评估一种新型辅助化学免疫治疗方案,该方案结合免疫治疗,降级治疗早期 TNBC。该方案包括基于蒽环类药物的化疗诱导,然后使用特瑞普利单抗联合白蛋白结合型紫杉醇,进行比标准疗程更短的免疫治疗。
研究进展
02
疗效
在第1阶段,12/25患者(48.0%)实现了tpCR,并且试验继续进行至完全累积。总体而言,39例(55.7%,95%CI 43.3-67.6)患者达到tpCR,41例(58.6%,95%CI 46.2-70.2)患者达到bpCR。基线CD8淋巴细胞浸润高和Ki-67指数高的患者,经历了更高的tpCR率。MP系统中RCB-0/I和5级的比例,分别为65.7%和58.6%。完成研究治疗后,18.6%和74.3%的患者,分别达到CR和PR,FAS人群的ORR为 92.9%。
9例(12.9%)患者行保乳联合腋窝清扫术,9例(12.9%)行保乳术联合前哨淋巴结活检,16例(22.9%)行乳房切除术并立即采用自体皮瓣、扩张器或植入物重建。在最初适合乳房切除术的58名患者中,有6名接受了乳房保守手术。截至2023年7月30日,EFS不成熟,记录了6个(8.5%)事件。
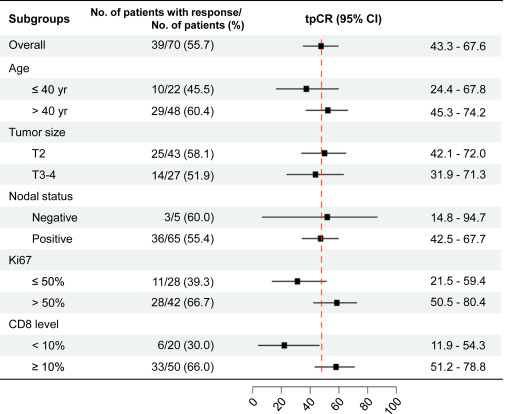
总病理完全缓解(ypT0/Tis ypN0)患者百分比差异的亚组分析。缩写:tpCR,总病理完全缓解;CI:置信区间。
安全性和毒性
3-4级治疗相关AE(TRAE)发生在16例(22.9%)患者中;最常见的是中性粒细胞减少(12,17.1%)、白细胞减少(11,15.7%)、丙氨酸氨基转移酶升高(4,5.7%)和疲劳(3,4.3%)。2级周围感觉神经病变 (4, 5.7%) 被认为与白蛋白结合型紫杉醇相关。8例(11.4%)患者存在与特瑞普利单抗相关的潜在免疫相关AE(irAE);最常见的是甲状腺功能减退症(5,7.1%,均为1-2级),转氨酶水平升高(3,4.3%,3级)和肌酐水平升高(1,1.4%,均为2级)。
1名患者(1.4%)因感染性静脉炎而停止研究治疗。没有发生与治疗相关的死亡。14例(20.0%)患者发生剂量减少,其中10例(14.3%)发生在使用蒽环类药物期间,7例(10.0%)发生在特瑞普利单抗联合白蛋白结合型紫杉醇治疗期间。由于转氨酶水平升高(2,2.9%)、皮疹(1,1.4%)和发热(1,1.4%),4例(5.7%)患者的NAC延迟。
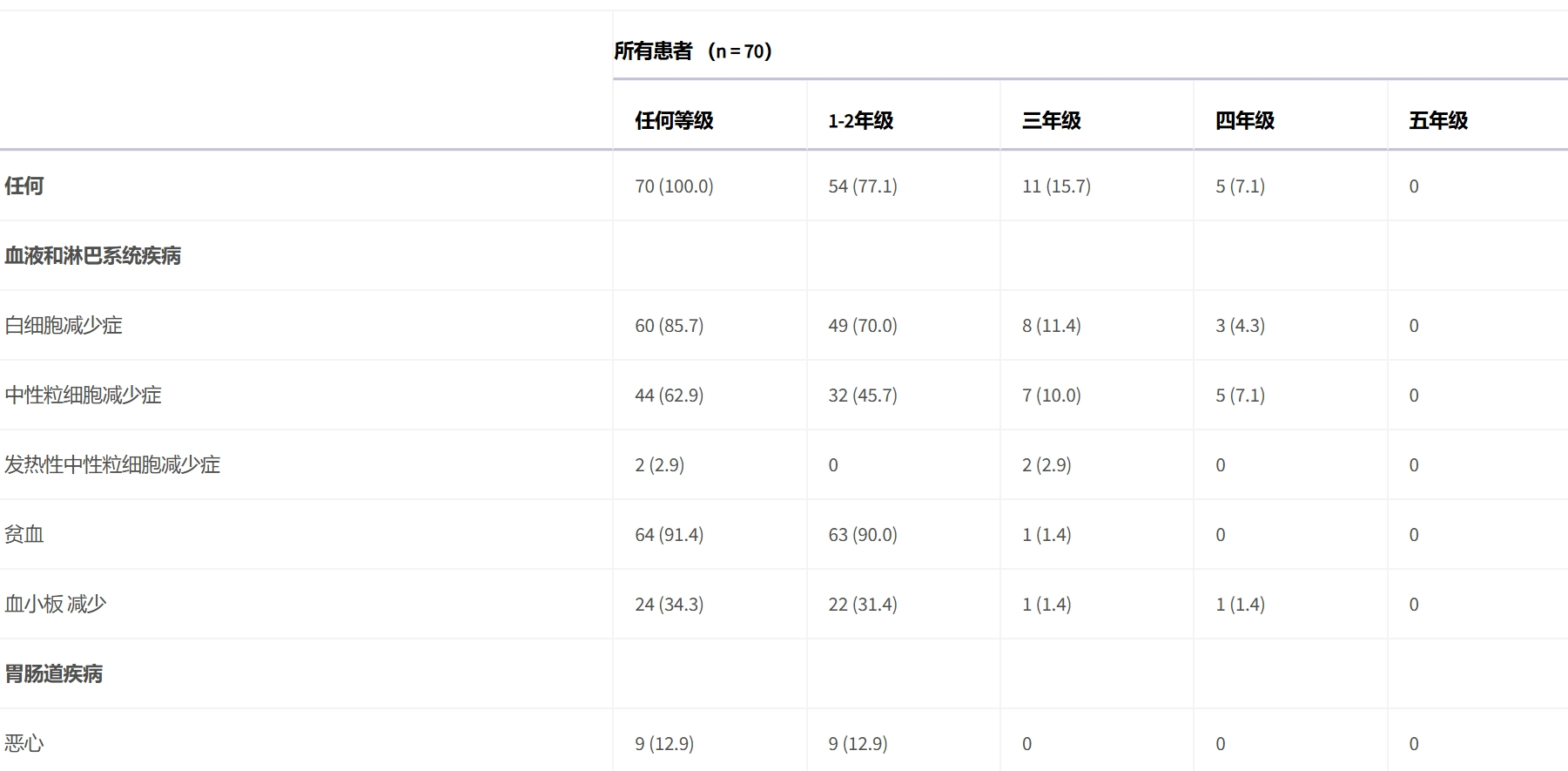
治疗相关不良事件
研究结论
03
本研究是第一个,也是最大规模的临床试验,证实了抗PD-1抗体降级加无铂化疗,是新辅助环境中早期TNBC的有效和安全选择。在NAC中加入特瑞普利单抗,可提供高tpCR率(55.7%)和可控的毒性。
目前,尚无针对早期TNBC的NAT全球标准。铂类药物已被添加到基于蒽环类药物和紫杉烷类药物的TNB 新辅助治疗中。本研究采用了不含铂的化疗骨架,包括蒽环类/环磷酰胺(EC)和白蛋白结合型紫杉醇,以最大限度地减少化疗毒性。尽管ICIs的化疗框架和持续时间存在差异,但两项试验之间的pCR率相当(KEYNOTE-552为64.8%,NeoTENNIS为55.7%)。考虑到本研究中,患有常规定义的高风险疾病的患者,比例要高得多(KEYNOTE-522中为25%的III期患者,而NeoTINNIS中为62.9%的III期患者),这些结果尤其令人印象深刻。
研究发现,患有T2和T3-4疾病的患者,从ICI中获益相似(T2为58.1%,T3-4为51.9%),突出了可能归因于NeoTENNIS试验样本量较小的差异,以及亚组分析中偶然发现的可能性。此外,紫杉烷和蒽环类药物给药顺序的差异,可以解释这些差异。
团队观察到,表柔比星-环磷酰胺化疗后,CD8淋巴细胞浸润增加。这一结果,与管腔B样乳腺癌新辅助治疗中报告的结果一致。化疗后,肿瘤MHC-II表达上调。这种上调可能会诱导IL7RCD4驻留记忆T细胞的浸润,从而可以预测ICI治疗的反应(未发表的数据)。数据表明,蒽环类药物通过促进淋巴细胞从基质迁移到肿瘤细胞巢,来调节免疫微环境,这可以优化免疫疗法的有效性。
确定生物标志物,以预测哪些患者可以从免疫疗法中获得最大益处,至关重要。试验结果表明,无论PD-L1状态如何,ICI增强pCR都是一致的。值得注意的是,与PD-L1阴性肿瘤相比,PD-L1阳性肿瘤患者在化疗方案中加入ICIs后,pCR率明显增加(KEYNOTE-522为68.9%对45.3%,IMpassion031为69%对48%)。CD8淋巴细胞的高基线浸润与较高的tpCR率之间,存在显著相关性(50人中有33人[66.0%]对20人中有6人[30.0%],P = 0.006)。重要的是,团队选择通过常规免疫组织化学和使用市售抗体,来评估CD8水平。与昂贵的基因组检测相比,这提供了一种更简单的方法,来量化实体瘤中的免疫细胞。
参考资料:
1.Bianchini G. Balko J.M. Mayer I.A. et al.
Triple-negative breast cancer: challenges and opportunities of a heterogeneous disease.
Nat Rev Clin Oncol. 2016; 13: 674-690
2.Mougalian S.S. Soulos P.R. Killelea B.K. et al.
Use of neoadjuvant chemotherapy for patients with stage I to III breast cancer in the United States.
Cancer. 2015; 121: 2544-2552
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发