【BMC Medicine】上海交通大学朱国培团队:揭示多西他赛与顺铂在口腔鳞状细胞癌术后放疗中的潜力
| 导读 | 鉴于需要有效但毒性较小的替代品,团队进行了一项试验,揭示同步多西他赛放疗(Doc-RT)具有良好的安全性和令人欣喜的疗效。 |
2024年7月29日, 上海交通大学医学院、上海口腔医学院朱国培团队在期刊《BMC Medicine》上发表了题为“Postoperative radiotherapy with docetaxel versus cisplatin for high-risk oral squamous cell carcinoma: a randomized phase II trial with exploratory analysis of ITGB1 as a potential predictive biomarker”的研究论文。ITGB1有望作为一种潜在的生物标志物,帮助指导患者选择化疗药物,科学界需要进一步的研究,以阐明所涉及的机制,并在更大的全球患者队列中进行验证。

https://bmcmedicine.biomedcentral.com/articles/10.1186/s12916-024-03541-6
研究背景
01
口腔鳞状细胞癌(OSCC)是全球最常诊断的癌症之一。手术切除联合辅助放疗(adjuvant radiotherapy, RT)仍然是局部晚期OSCC的标准治疗方法。在OSCC患者中,术后放化疗(chemoradiotherapy, CRT)比单独放疗具有生存获益。然而,顺铂相关不良事件(AEs)如骨髓抑制和肾毒性仍是主要问题,这限制了顺铂同步治疗的实际临床应用。
多西紫杉醇已显示出作为放射增敏剂的前景。据推测,通过在高度辐射敏感的G2/M期诱导细胞周期同步,以及通过调节参与细胞辐射反应的各种基因的表达,可以增强放疗的效果。 多项II期试验表明,HNSCC患者同时进行多西他赛放疗可耐受,且缓解率高。在本研究中,多西他赛联合放疗显示出良好的毒性特征,并实现了无病生存期(DFS)和总生存期(OS)的改善。
通过药物基因组学确定预测性生物标志物,对于理解癌症反应异质性和实现个性化治疗至关重要。团队启动了一项前瞻性、开放标签、随机试验,旨在评估多西他赛放疗(Doc-RT)与标准顺铂放疗(Cis-RT)相比,在符合顺铂条件的OSCC患者中的疗效。此外,团队在试验中提出了一项预先设定的生物标志物评估,评估肿瘤ITGB1表达与Doc-RT和Cis-RT的疗效之间的潜在关联。
研究进展
02
生存
中位随访28.8个月(四分位距(IQR):17-49 个月)后,发生了98例DFS事件,其中47例在Doc-RT组(25 例局部区域进展(LRP)、15例远处转移(DM)、4例LRP伴DM、1例原发肿瘤(SPT)和2例死亡作为首发事件),51例在顺式放疗组(包括27例LRP、 15例DM、5例LRP伴DM、1例SPT和4例死亡作为首发事件)。Doc-RT组的2年DFS为63.7%(95%CI,55.2%至73.2%),而Cis-R组为56.1%(95%CI,49.3%至67.7%)(p=0.55;多西他赛组与顺铂组DFS的风险比(HR)为0.92(95%CI,0.61至1.4)。两组均未达到中位DFS。
总共发生了72例死亡,其中34例在Doc-RT组,38例在Cis-RT组。两组均未达到中位OS。Doc-RT组的2年OS为71.2%(95%CI,61.5%至78.8%),而Cis-RT组为70.4%(95%CI,61%至78%)。多西他赛与顺铂相比OS的HR为0.87(95%CI,0.55至1.38)。多西他赛组的2年LRFS率为76.4%,而顺铂组为71.5%。对于DMFS,多西他赛组的2年率为81.9%,而顺铂组为77.9%。
在一项亚组分析中,在有两个或多个转移性淋巴结的患者中,多西他赛与顺铂相比,DFS的HR为0.41(95%CI,0.18至0.91,p = 0.028),表明Doc-RT组具有优势。其他亚组分析,未显示两个治疗组在DFS和OS方面有任何统计学上的显著差异。LRFS的进一步亚组分析显示,ENE和/或阳性切缘亚组的HR为1.16(95%CI,0.63至2.12,p=0.567),多发淋巴结转移亚组的HR为0.49(95%CI,0.20至1.18,p=0.121)。ENE和/或阳性切缘亚组DMFS的HR为1.19(95%CI 0.75-1.91,p=0.735),多发性淋巴结转移亚组的HR为0.20(95%CI 0.04-0.97,p=0.105)。
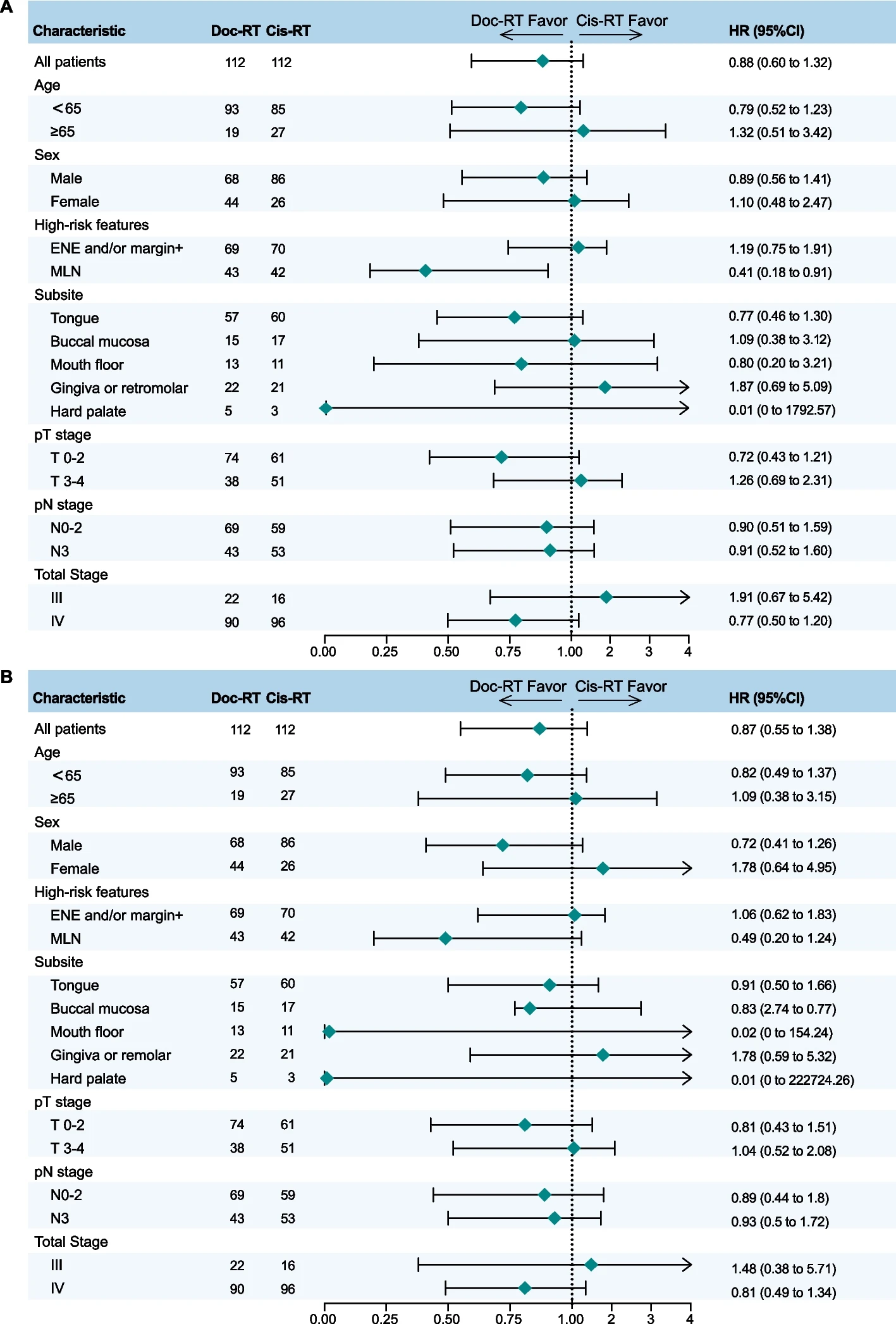
所有患者DFS(A)和OS(B)的亚组分析。森林图描绘了处理效果对多个亚组的DFS(A)和OS(B)的影响。Doc-RT,多西他赛放疗;顺式放疗,顺铂放疗;ENE, 结外延伸;MLN, 多发性淋巴结;T, 肿瘤;N, 节点;HR, 风险比;CI, 置信区间
ITGB1表达和疗效结果
在接受Doc-RT或Cis-RT治疗的224例患者中,206例患者(Doc-RT组:100例;顺式-RT臂:106)。在Doc-RT队列中,39名患者(39%)显示ITGB1的IRS较低,而20名 (20%)和41名(41%)分别具有中度和高IRS。在Cis-RT队列中,观察到ITGB1表达的相似分布,分别有44例(41.5%)、21例(19.8%)和41例(38.7%)患者表现出低、中、高IRS。
按ITGB1表达水平分层,Doc-RT治疗的低、中、高表达患者的2年DFS,分别为73.8%(95%CI 56.7-84.99%)、75.0%(95%CI 50.0-88.7%)和48.7%(95%CI 32.8-62.8%)。相比之下,CIS-RT治疗的ITGB1表达低、中、高患者的2年DFS分别为54.5%(95%CI [38.7-67.7%)]、52.4%(95%CI 29.7-70.9%)和58.5%(95%CI 42.0-71.8%)。在Doc-RT患者中,与高表达相比,低ITGB1表达与预后改善相关,包括2年DFS显著升高(73.8% vs 48.7%;p = 0.016),2年OS数值升高,但无显著升高(79.0% vs 60.9%;p = 0.083)、局部区域无复发生存期和无远处转移生存期。在Cis-RT队列中,与ITGB1表达的预后相关性不明显。
尽管样本量有限,但Doc-RT/低ITGB1亚组在各个终点的生存率,始终优于Doc-RT,这表明该人群可能比Cis-RT更受益于Doc-RT。值得注意的是,ITGB1的预后价值仅在Doc-RT组中明显,而在Cis-RT组中不明显。这表明ITGB1有望作为一种预测性生物标志物,用于识别特异性针对Doc-RT的敏感和耐药亚组。
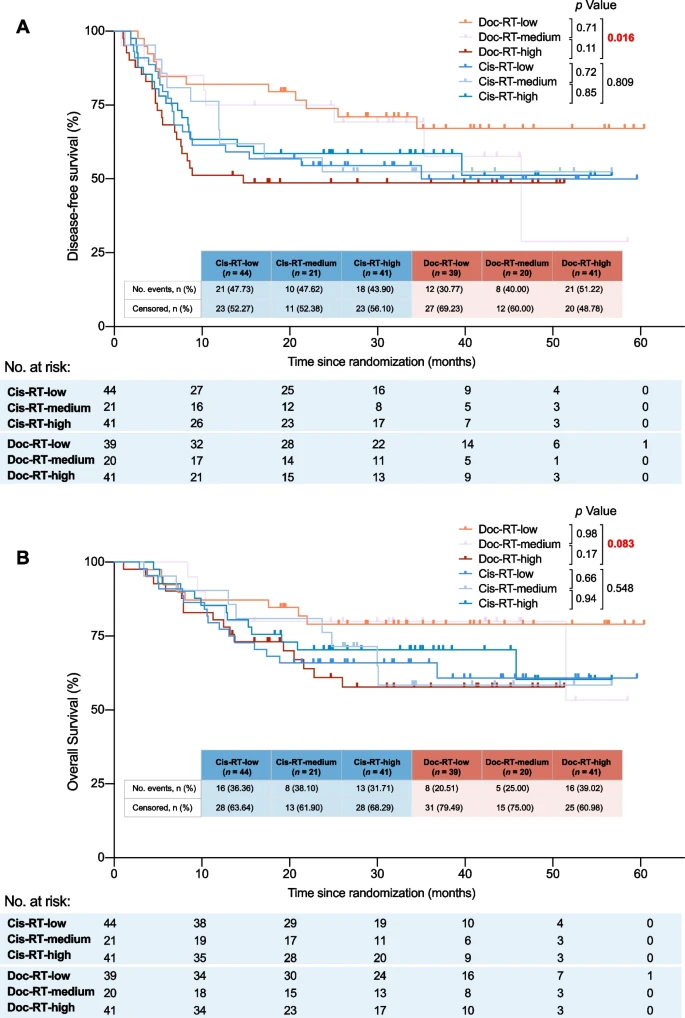
ITGB1表达和疗效结果。A 通过ITGB1表达的无病生存期。B ITGB1表达的总生存期;ITGB1, 整合素β1;Doc-RT,多西他赛放疗;顺式放疗,顺铂放疗。
研究结论
03
本研究的目的,是比较多西他赛作为同步化疗方案与高剂量顺铂,在OSCC患者中的疗效和安全性。尽管该试验不是作为非劣效性研究设计的,但Doc-RT组和Cis-RT组之间的肿瘤学结果相当,包括DFS、LRFS、DMFS和OS。此外,Doc-RT组的血液学不良事件较少。该研究还表明,ITGB1状态可能有助于识别对多西他赛敏感的患者亚组。
每周同时服用20mg/m2的多西他赛在高危OSCC患者中,辅助放疗耐受性良好,与历史对照组相比,其生存获益良好。多西他赛组的3-4级血液学和吞咽困难发生率显著降低,具有相似的肿瘤学结果。3-4级口腔粘膜炎在多西他赛组的发生率略高,但<10%的患者需要调整治疗或停药。因此,20mg/m2每周多西他赛与术后放疗同时服用,可作为高危OSCC患者的可耐受替代疗法。
Doc-RT组的2年DFS与RTOG-0234中报告的多西他赛-西妥昔单抗-RT方案相当,同时表现出较低的3-4级口腔粘膜炎发生率。20mg/m2的更高剂量多西他赛方案对于高危OSCC患者,与放疗同时进行,可能是术后同步放化疗耐受性良好且有效的选择。
精准肿瘤学有望通过考虑患者之间肿瘤的分子异质性,来改变癌症治疗。虽然标准化方案仍然是常态,但预测患者特异性药物反应的生物标志物,有助于提高个性化治疗方案的安全性和有效性。 此前,团队在OSCC模型中,发现ITGB1介导对多西他赛的耐药性。团队新的临床研究表明,ITGB1表达与OSCC患者的多西他赛放疗反应相关,而顺铂敏感性与ITGB1状态无关。展望未来,ITGB1和其他药物基因组学标记物的分子分析,可能会指导每位患者的最佳个性化治疗选择。
涉及多西他赛的新策略仍在探索中。正在进行的RTOG-1216 II/III期试验,将为术后每周同时进行多西他赛-西妥昔单抗和顺铂-PD-1抑制剂放化疗治疗高危HNSCC,提供高质量证据。鉴于本研究中指出的ITGB1-多西他赛的潜在关联,像ITGB1这样的生物标志物,未来有望帮助患者进行联合多西他赛和其他药物的治疗方案。
参考资料:
1.Sung H, Ferlay J, Siegel RL, Laversanne M, Soerjomataram I, Jemal A, et al. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2021;71:209–49.
2.Chinn SB, Myers JN. Oral cavity carcinoma: current management, controversies, and future directions. J Clin Oncol. 2015;33:3269–76.
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发