【Lancet子刊】瑞金医院赵维莅团队:联合靶向药物与CHOP方案治疗外周T细胞淋巴瘤初诊患者
| 导读 | 团队进行了一项开放标签、2期非随机、外部对照研究,以评估靶向药物联合CHOP(环磷酰胺、多柔比星、长春新碱和泼尼松龙)(CHOPX)在一线环境中,治疗PTCL的疗效和安全性。 |
2024年7月29日,上海交通大学医学院附属瑞金医院赵维莅团队在期刊《Lancet Western Pacific》上发表了题为“Targeted agents plus CHOP compared with CHOP as the first-line treatment for newly diagnosed patients with peripheral T-cell lymphoma (GUIDANCE-03): an open-label, multicentre phase 2 clinical trial”的研究论文。在本研究中,靶向药物加CHOP显示出更好的疗效,而没有额外的安全性问题。这些发现提供了初步数据,支持生物标志物驱动的治疗策略是可行的,并且可能针对PTCL中的分子特征,带来有希望的疗效。
 https://www.thelancet.com/journals/lanwpc/article/PIIS2666-6065(24)00154-8/fulltext#%20
https://www.thelancet.com/journals/lanwpc/article/PIIS2666-6065(24)00154-8/fulltext#%20
研究背景
01
外周T细胞淋巴瘤(PTCL)是一种异质性疾病,具有侵袭性行为和令人沮丧的后果。标准CHOP(环磷酰胺、多柔比星、长春新碱和泼尼松龙)化疗,仍然是使用最广泛的一线治疗,尽管反应不佳。除间变性大细胞淋巴瘤(ALCL)外,大多数亚型PTCL患者的5年总生存率(OS)约为30%-40%。布伦妥昔单抗vedotin已证明对于新诊断的CD30阳性PTCL的有效性和安全性,科学界鼓励在一线环境中应用靶向药物联合标准化疗。
PTCL中的基因组分析,可以提高生物学理解,并确定治疗靶点。TP53是一种关键的抑癌基因,TP53突变发生在15%-28%的PTCL中。TET2(Ten Eleven易位2) 是PTCL中最常见的突变基因。KMT2D是另一个与组蛋白甲基化相关的基因,可预测不良结果。CREBBP/EP300是涉及组蛋白乙酰化的主要表观遗传学基因,在12%左右的PTCL中发生突变,且与较差的无进展生存时间(PFS)相关。
团队进行了一项开放标签、多中心、非随机、外部对照的2期试验,比较了基因突变加CHOP(CHOPX)与CHOP的靶向药物选择策略,在初诊PTCL患者中的疗效和安全性,旨在探索生物标志物驱动的治疗方法,在这一难治人群中的可能性。
研究进展
02
生存分析
截至2023年8月30日,中位随访时间为24.3个月(IQR 12.0–26.7)。CHOPX组的中位PFS为25.5个月(95%CI 8.5-42.5),而CHOP组为9.0个月(95%CI 3.5-14.5)(HR0.57,95%CI 0.34-0.98;p=0.039),对应的2年PFS率分别为53.2%(95%CI 38.7–67.7)和28.0%(95% CI 13.6–42.3)。同时,CHOPX组未达到中位OS,而CHOPX组为30.9个月(95%CI 11.0-50.8)(HR0.55,95%CI 0.28-1.10;p=0.088),对应的2年OS率分别为68.0%(95%CI 53.0–82.9)和60.8%(95%CI 45.2–76.3)。
移植
11例患者(CHOPX组为6/48 [12.5%],CHOP组为5/48 [10.4%]),其中8例为长期生存,3例为进展性自身HSCT。4例患者在挽救性治疗后,行自体造血干细胞移植,其中2例因疾病进展而死亡。接受同种异体造血干细胞移植的3名患者,均为CR,并且仍然存活。HSCT患者未达到中位OS,非HSCT患者分别为30.9个月(95%CI 24.9-36.8)。
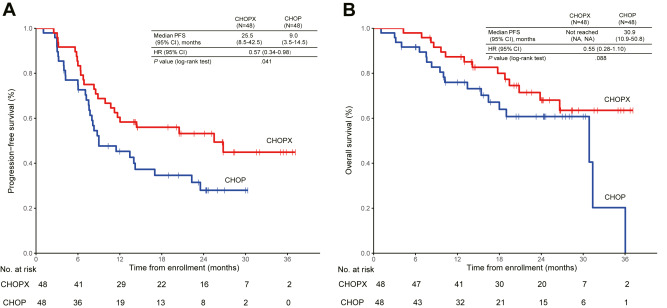
根据治疗组的生存曲线。根据治疗组,Kaplan-Meier估计(A)无进展生存期和(B)总生存期。
毒性
对96名接受至少1剂研究治疗的患者,进行了安全性评估。中性粒细胞减少,是两组中最常见的事件(CHOPX组为82%,CHOP组为73%)。1名接受CHOP联合氮杂胞苷治疗的患者,因肺部感染而无法完成第6个周期。CHOPX组最常见的3-4级血液学不良事件,是中性粒细胞减少(31,65%)、发热性中性粒细胞减少症(11,23%)和贫血(11,23%)。对于非血液学AEs,CHOPX与所有级别的皮疹(5,10%)相关,主要在接受来那度胺的患者中观察到。所有级别的胃肠道反应(25,52%),主要在接受氮杂胞苷和tucidinostat的患者中观察到,但主要是1-2级(23,48%)。CHOPX组中最常见的3-4级非血液学AE,是感染(5,10%)、胃肠道反应(2,4%) 和转氨酶升高(2,4%)。CHOP组最常见的3-4级血液学不良事件,是中性粒细胞减少症(25%,52%)、发热性中性粒细胞减少症(9,19%)和贫血(8,17%)。CHOP组中最常见的3-4级非血液学AE,是感染(2,4%)、胃肠道反应(1,2%)、转氨酶升高(1,2%)和疲劳(1,2%)。两组3-4级血液学和非血液学AE相似。CHOPX中没有患者出现超过14天的长期中性粒细胞减少症,或靶向药物剂量调整。
尽管AE发生率增加,但两组化疗的剂量强度相近。在CHOPX组中,由于1例为3级血小板减少症,2例为4级中性粒细胞减少症,3例患者报告了tucidinostat的剂量中断,并在恢复后完成了计划的治疗。在接受地西他滨、氮杂胞苷和来那度胺治疗的患者中,没有报告剂量中断。来那度胺、妥西司他和地西他滨的剂量减少,未见报道。两组接受90%以上总剂量强度的患者,比例相似。
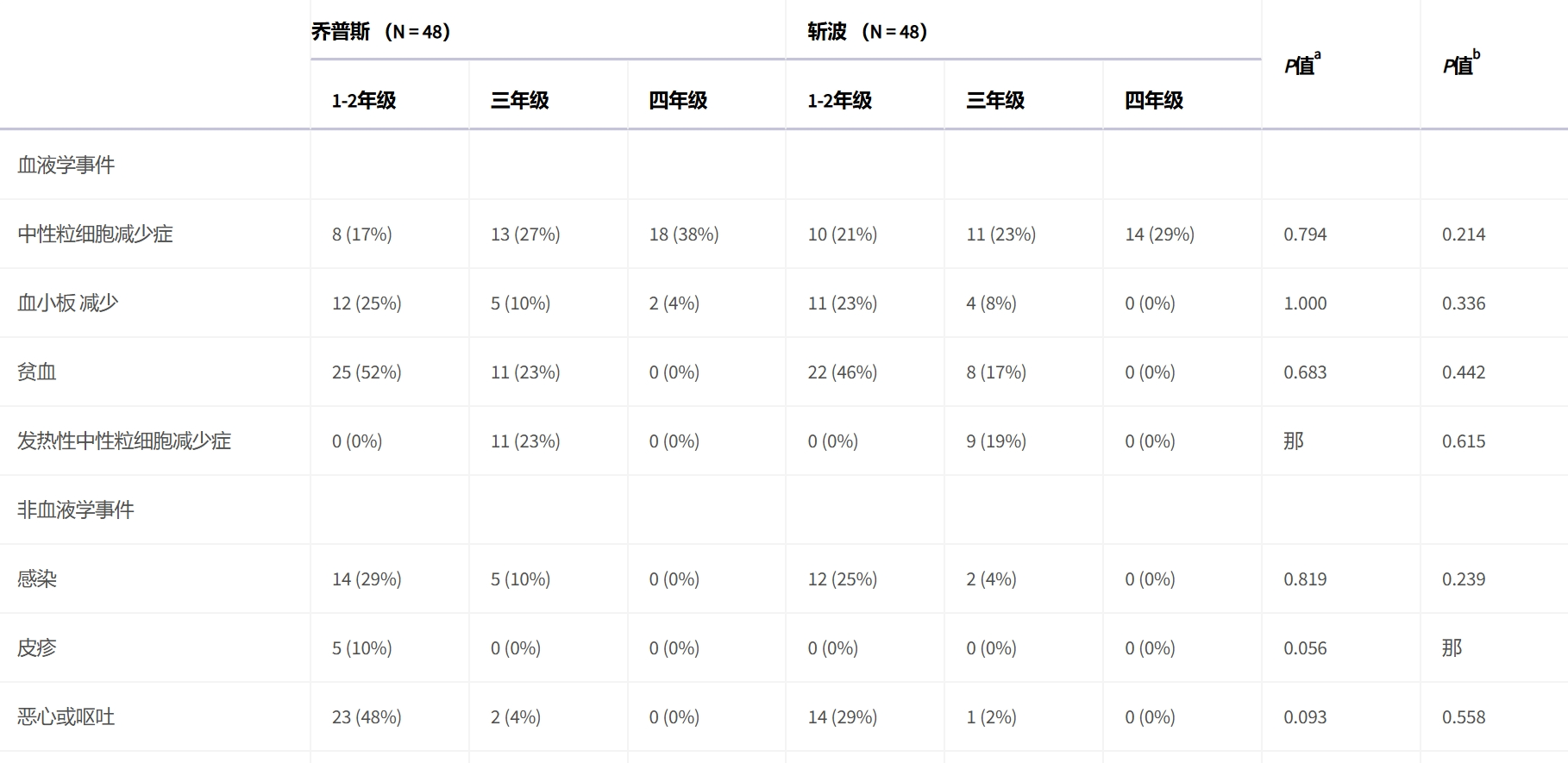
不良事件发生率。
研究结论
03
这是第一个基于新诊断的PTCL中特定基因突变,评估靶向药物加CHOP的疗效和安全性的临床试验。本研究达到了其主要终点。与CHOP相比,CHOPX具有优越的CRR和良好的耐受性。靶向药物的选择基于基因突变,与本研究中CHOPX组的病理亚型无关。研究结果显示,接受氮唑胞苷加CHOP治疗的TFHL患者,反应改善。
本研究中nTFHL-AI和TET2/KMT2D突变的发生率,分别为64%(61/96)和70%(67/96)。在来自亚洲国家的另一个大型PTCL前瞻性队列中,最常见的亚型是nTFHL-AI(54%,120/221),不包括NK/T细胞淋巴瘤、ALCL和其他罕见的亚型,与本研究的结果一致。其他研究还表明,nTFHL-AI在地理上,在亚洲国家比在西方国家更常见。
尽管靶向药物的个体化,并未在每个X亚组中得到支持,但团队已经注意到,其在TET2/KMT2D突变的患者中具有更高的疗效。根据团队最近对PTCL大型队列的分子分析,这种疾病可分为不同的分子亚型,具有不同但可靶向的致癌信号通路。一项根据遗传亚型和相关机制研究的多中心、随机2期试验 (NCT05675813) ,目前正在进行中。
参考资料:
1.Cai M.C. Cheng S. Wang X. et al.
CEOP/IVE/GDP alternating regimen compared with CEOP as the first-line therapy for newly diagnosed patients with peripheral T cell lymphoma: results from a phase 2, multicenter, randomized, controlled clinical trial.
Genome Med. 2020; 12: 41
2.Bachy E. Camus V. Thieblemont C. et al.
Romidepsin plus CHOP versus CHOP in patients with previously untreated peripheral T-cell lymphoma: results of the ro-CHOP phase III study (conducted by LYSA).
J Clin Oncol. 2021; 40JCO2101815
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发