协和医院刘子文团队:胰腺癌代谢的新机制和有前途的方法
| 导读 | 更全面、更深入地了解胰腺癌细胞的代谢调控,不仅丰富了对疾病进展机制的理解,而且为新的诊断和治疗方法提供了启示。 |
2024年8月1日, 中国医学科学院北京协和医学院附属北京协和医院刘子文团队在期刊《Cell Death & Disease 》上发表了题为“Emerging mechanisms and promising approaches in pancreatic cancer metabolism”的研究论文。本文总结了目前在肿瘤代谢背景下,正在研究的主要主题,并概述了针对PC代谢中关键酶和信号通路的基础研究和临床试验的现状。

https://www.nature.com/articles/s41419-024-06930-0
研究背景
01
肿瘤细胞具有许多独特的特征,其中许多特征直接受细胞代谢控制或受特定代谢物的调节。随着新技术的飞速发展,人们逐渐发现,肿瘤代谢涉及代谢网络多个层面的整体变化,在促进肿瘤发生和发展方面,发挥着重要作用。
代谢重编程,是指肿瘤细胞在恶性发育过程中,发生的合成代谢和分解代谢平衡的适应性变化,以满足对物质和能量的大量需求,已逐渐被认为是癌症的关键标志之一。这种重编程使肿瘤细胞能够在由快速增殖引起的营养饥饿的肿瘤微环境(TME)中,获得优势并存活。与蓬勃发展的研究领域相比,只有少数基于代谢的癌症药物研发成功,并且由于其低特异性和不良副作用,仍处于起步阶段。这些针对癌细胞内在代谢的策略,通常不考虑非癌性基质细胞和免疫细胞的复杂串扰,仍有待进一步研究。
胰腺癌(Pancreatic cancer,PC)是一种预后不良的侵袭性癌症。总体5年生存率低于13%。预计到2030年,PC将在美国恶性肿瘤相关死亡人数中排名第2位。探索代谢调控网络和潜在机制,制定综合治疗策略,推进基于个体患者的精准治疗,有望改善胰腺癌的整体预后。
研究进展
02
免疫疗法
免疫治疗已逐渐发展成为一种成熟的抗肿瘤策略,但其在PDAC中的疗效有限。一些研究试图根据代谢特征,预测免疫疗法的反应。TME中免疫系统的代谢紊乱,有望提高代谢靶向抗癌策略的疗效。
核苷酸代谢为免疫系统的激活和增殖,提供了遗传物质和能量资源。嘌呤类似物,如释放的细胞外ATP或腺苷,可激活免疫细胞的嘌呤能受体和腺苷受体,从而促进或抑制免疫应答。IFN在S期触发细胞周期停滞,导致核苷酸库和核苷外流不足,IFN与ATR抑制剂联合,可诱导致死的DNA损伤并减少核苷酸生物合成,从而限制PDAC的生长。
通过自体T细胞过继转移方案调节细胞代谢,可以促进具有记忆表型的T细胞的生成,提高其抗肿瘤作用。 改造溶瘤病毒表达瘦素,还可以通过增加FAO和OXPHOS,来增强抗肿瘤反应。PD-1阻断免疫疗法,是一种广泛使用的疗法,但PDAC患者反应不佳。靶向糖酵解,会影响PDAC临床前模型中PD-1+ TIL的积累。激活与线粒体代谢相关的AMPK和mTOR通路,也有望增强PD-1阻滞剂的治疗效果。
基于上述免疫-代谢串扰,科学界已经研究了新的治疗靶点。例如,吲哚胺2,3-双加氧酶(indoleamine 2,3-dioxygenase, IDO)可以降解色氨酸,并抑制免疫应答,该疗法已在几项临床研究中,进行了探索。
其他疗法
其他药物治疗,正在通过新兴技术逐步探索。使用一些纳米药物,可以增强氧化应激。调节脂质代谢和极化巨噬细胞的还原响应性纳米平台,可用于PDAC的联合治疗。一种新型树枝状聚合物纳米凝胶,通过内质网应激,增强化学免疫疗法。降解ECM后,可以增强纳米颗粒的运输,增加对PDAC的杀伤效果。 研究表明,硒有机化合物和双氢青蒿素,可以诱导PDAC细胞的铁死亡。 定制的钌复合物,也可以影响OXPHOS,并发挥抗癌作用。
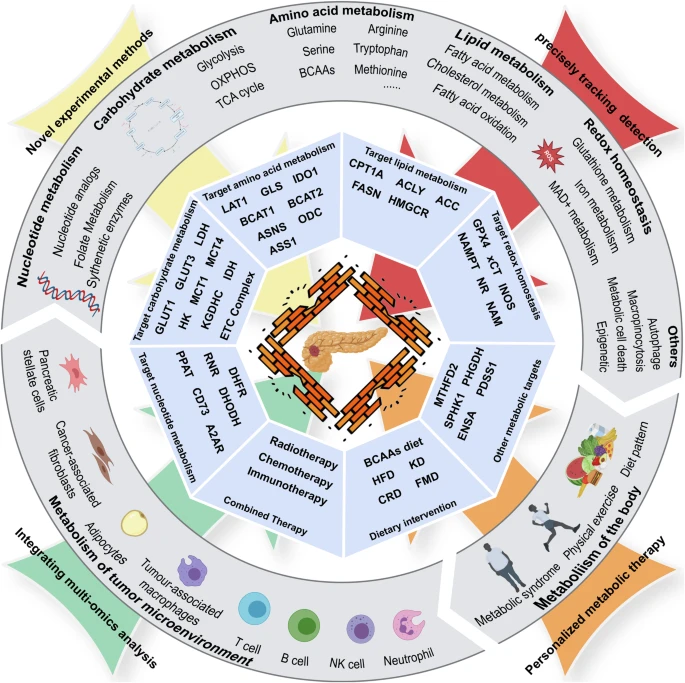
胰腺癌的代谢特征和治疗靶点概述。
靶向代谢的临床试验
代谢靶向治疗在作为常规治疗应用之前,还有很长的路要走。一些代谢调节剂,如二甲双胍和他汀类药物,已被用于发挥额外的癌症治疗效果。二甲双胍治疗PDAC,已经开展了多项临床试验,如NCT02048384、NCT03889795和NCT02201381。通过体内代谢追踪发现,他汀类药物可以抑制辅酶Q的合成,他汀类药物与MEK抑制剂合用,可以促进氧化应激和凋亡。基于这些有希望的数据,开展了NCT00944463期、NCT00584012期和NCT04862260期临床试验。厄贝沙坦可能通过抑制铁代谢,来逆转吉西他滨的耐药性。此外,地高辛(NCT04141995)、达格列净(NCT04542291)、奥美拉唑(NCT04930991)等药物,甚至多种代谢调节药物(NCT02201381)的组合,也被探索出来。
临床试验已经开始探索,基于糖酵解途径的治疗方法。在NCT00096707的情况下,2-脱氧-D-葡萄糖(2-deoxy-D-glucose,2-DG)联合多西他赛用于晚期实体瘤,具有可耐受的不良反应和一定的临床益处。硫辛酸类似物CPI-613被证明选择性地抑制PDH活性,并抑制PDAC的生长。
通过拮抗谷氨酰胺抑制剂(如6-重氮-5-氧代-L-正亮氨酸(DON)和DRP-104诱导代谢危机,在临床前模型中,是一种很有前途的策略。NCT03965845探讨了谷氨酰胺酶抑制剂特拉格纳司他 (CB-839) 在晚期或转移性实体瘤中的疗效。近年来,在NCT01523808、NCT02195180和NCT03665441中,红细胞包封天冬酰胺酶(如GRASPA和Eryaspase)联合化疗,已被证明可以改善患者的预后,表明其作为二线治疗的巨大潜力。在NCT00739609、NCT03432676和NCT03006302中,IDO1抑制剂和PD-1检查点抑制剂,引起PDAC对免疫治疗有反应,其与化疗联合使用的疗效,已在NCT02077881和NCT03085914等临床试验中,得到进一步探索。此外,对精氨酸(NCT02101580)和蛋氨酸(NCT03435250)的研究,提高了对靶向氨基酸代谢治疗PDAC的理解。
尽管脂质合成相关基因在多种癌症中过表达,但相关的临床试验仍处于探索阶段。科学界分别在NCT02223247和NCT03829436中,探索了FASN抑制剂TVB-2640和PPARα拮抗剂TPST-1120的应用潜力。
还有几种药物,可能通过影响氧化还原平衡,来发挥抗癌作用。例如,已经进行了青蒿琥酯和抗坏血酸的I期临床试验(分别为NCT02353026和NCT01049880)。在临床前模型中,将β-拉帕醌(ARQ761)与GLS1抑制剂联合使用,可诱导过多的ROS产生,并选择性地导致PDAC细胞死亡。NCT02514031探讨了ARQ761联合吉西他滨/白蛋白结合型紫杉醇治疗的潜力。
自噬在PDAC的进展中起重要作用,溶酶体抑制剂羟氯喹,可能与MEK抑制剂曲美替尼,具有协同作用。科学界已经进行了许多临床试验(NCT01777477、NCT03825289和NCT04132505)。
最后,有一些基于饮食干预的临床试验,如NCT01019382和NCT01419483,但它们都处于早期阶段,距离临床应用还很遥远。

针对胰腺癌癌症代谢的代表性临床试验
研究结论
03
近年来,PDAC治疗的代谢机制和转化应用,已成为新的、具有挑战性的研究方向。体内和体外实验,都揭示了PDAC的代谢依赖性。 稳定同位素的利用,已成为探索PDAC代谢途径的关键方法。类器官等先进技术平台,也在推动代谢相关研究转化的进步。许多基于代谢特征的分子亚型方法正在开发中,用于治疗和评估不同类型的PDAC患者。此外,单细胞测序和空间组学的发展,使得在细胞水平上表征不同组织的代谢串扰,成为可能。团队对细胞代谢在疾病进展中作用的理解,已经有了显著的进步。
鉴于目前对新陈代谢如何支持细胞增殖的大部分理解,都是基于对癌细胞的研究,因此,新陈代谢如何塑造不同细胞的相互作用,需要在更复杂的生态系统中进行探索。这些信息有望帮助科学界更深入地了解代谢调节网络,从而克服以往代谢疗法的局限性,为患者提供量身定制治疗方案的机会。
参考资料:
1.Finley LWS. What is cancer metabolism? Cell. 2023;186:1670–88.
2.Koppenol WH, Bounds PL, Dang CV. Otto Warburg’s contributions to current concepts of cancer metabolism. Nat Rev Cancer. 2011;11:325–37.
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发