中南大学张彬团队:XRCC2在肺腺癌治疗中的生物标志物潜力
| 导读 | 本研究为LUAD提供了宝贵的见解,提出了一种用于进一步临床验证的预后工具,并揭示了一种通过靶向c-Myc-XRCC2-VIM来对抗肺转移的潜在治疗策略。 |
2024年8月1日,中南大学湘雅医学院张彬团队在期刊《npj Precision Oncology》上发表了题为“XRCC2 driven homologous recombination subtypes and therapeutic targeting in lung adenocarcinoma metastasis”的研究论文。本研究加深了对LUAD中HRG的理解,为其预后和治疗意义,提供了新的见解。已确定的生物标志物XRCC2,以及拟议的c-Myc-XRCC2-VIM轴,在指导临床决策和改善LUAD患者的预后方面,具有重要前景。

https://www.nature.com/articles/s41698-024-00658-y#Sec12
研究背景
01
肺腺癌(LUAD)是最普遍和最致命的肺癌类型之一。虽然治疗策略改善了结果,但许多患者的预后仍然很差,尤其是那些患有转移性或化疗耐药性肿瘤的患者。
由DNA损伤修复缺陷引起的基因组不稳定性,是癌症的标志。同源重组(HR)通过促进DNA双链断裂的无错误修复,在维持基因组完整性方面,起着至关重要的作用。该过程由关键的同源重组基因(HRG)介导,例如 RAD51、BRCA1/2和XRCC家族的成员。HRGs的失调会损害修复机制,并通过增加基因组不稳定性,来促进肿瘤发生。此外,HRGs的改变,与抗肿瘤药物敏感性有关。
在本研究中,团队旨在解决理解HRG如何在临床上影响LUAD的差距,其目的是阐明新的分层工具和克服这种疾病的致死性。团队研究了HRG在LUAD患者中的表达和预后价值,并定义了与结局相关的不同HR亚型。此外,团队寻求开发一种预后HR评分系统,并确定介导LUAD发病机制的关键生物标志物和靶点。通过体外和体内实验,团队探索了XRCC2促进转移的假说及其作用机制。最后,团队研究了一种针对c-Myc-XRCC2-VIM轴的潜在治疗方法。
研究进展
02
HR评分系统开发及其在泛癌中的应用
为了个性化评估HR对患者预后的影响,团队开发了一个利用GSVA算法的HR评分系统。KM曲线显示,高HR评分与不良预后之间,存在显著相关性。此外,无论其他临床病理特征如何,HR评分都是独立的预后因素,从而展示了其临床适用性。实验结果显示,高HR亚组在验证集中,表现出较差的结果。
团队使用GSCA数据库,对肿瘤组织和正常组织之间的HR评分,进行了系统分析。团队观察到,所有癌症类型的HR评分,都一致上调。在11种不同类型的癌症中,高HR评分与不良预后之间,存在很强的关联;而THYM的预后,仅显示良好。这些发现表明,高HR评分是LUAD的一个危险因素,并在各种其他恶性肿瘤中,具有潜在影响。研究结果表明,HR评分系统作为一种具有广泛临床适用性的泛癌预后模型,具有广阔的临床适用性。
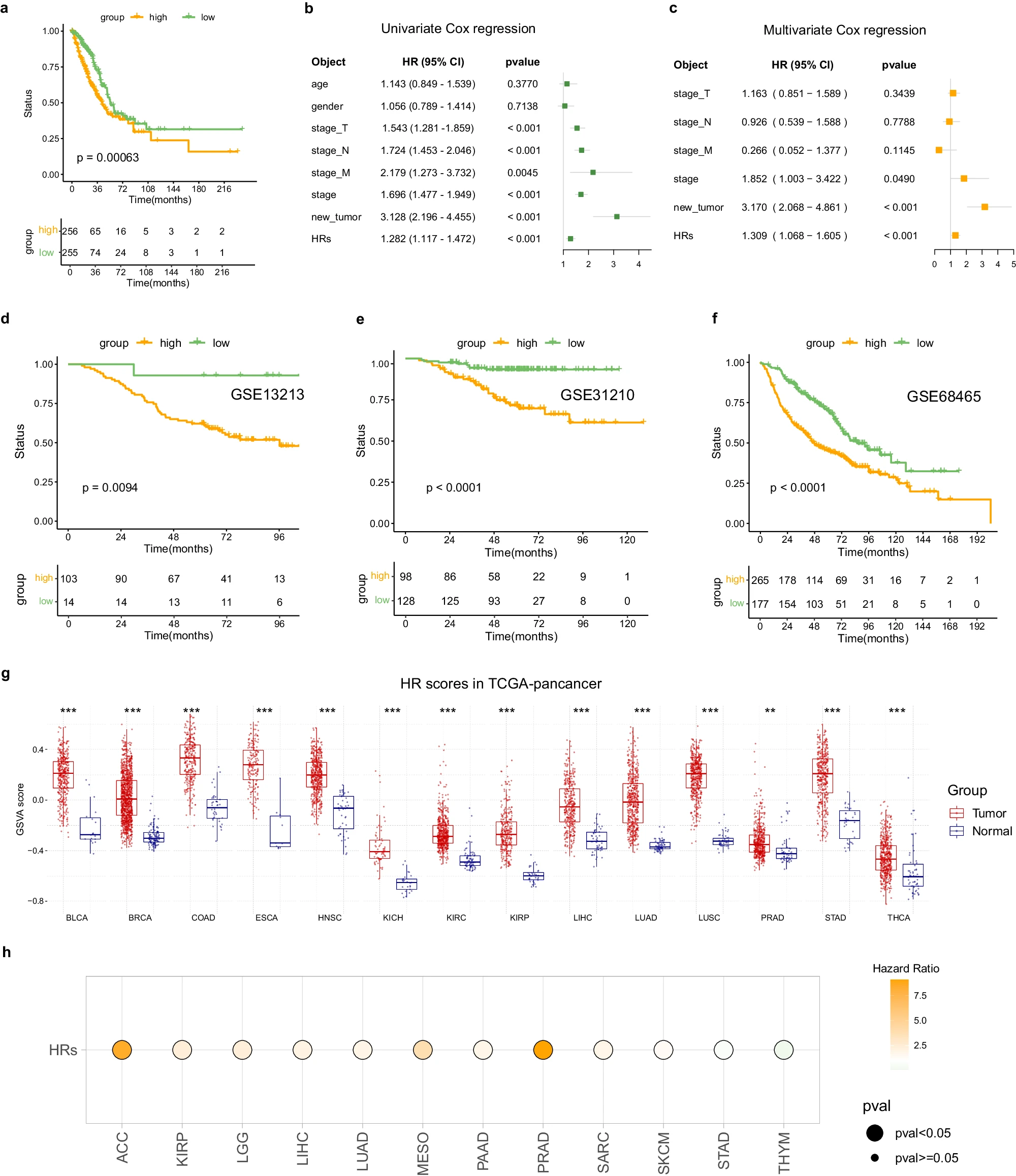
HR评分系统的构建与泛癌应用。
XRCC2在体外和体内促进肺癌细胞的迁移和侵袭
波形蛋白作为一种必需的细胞骨架蛋白,在上皮-间充质转化(EMT)中,起着至关重要的作用。EMT是肿瘤细胞获得迁移和侵袭特性的过程,导致转移和化疗的耐药性。团队在多种类型的肺癌细胞中,进行了细胞划痕和transwell检测。与对照组相比,敲低XRCC2导致细胞迁移显著减少,而XRCC2的过表达,导致细胞迁移显著增加 。同时,在细胞侵袭实验中,也证实了类似的趋势。在体内实验中,团队使用小鼠模型,研究了XRCC2对肺转移的影响。结果表明,与对照组相比,XRCC2敲除组的肺转移结节明显减少。两组裸鼠的肝脏和脾脏,均未观察到转移。这些发现提供了强有力的证据,表明XRCC2在促进肺转移方面,起着至关重要的作用。
靶向c-Myc-XRCC2-VIM轴进行治疗
阿霉素通过诱导DNA链断裂,引起细胞死亡。研究表明,缺乏同源重组的细胞,对阿霉素的敏感性更高。基于c-Myc-XRCC2-VIM轴的临床相关性,及其与HR活性的关联,团队提出靶向该轴,可能是克服LUAD中阿霉素耐药性的一种有前途的治疗策略。
团队观察到实验组(联合治疗)和对照组之间的小鼠体重没有显著差异,表明该治疗未对整体健康造成显著的毒性或不利影响。在比较肺转移结节的数量时,与对照组和仅使用阿霉素组相比,联合组的结节明显较少。两组裸鼠的肝脏和脾脏,均未观察到转移。免疫组织化学(IHC)分析表明,联合处理可有效下调XRCC2及其下游靶点VIM的表达。在用阿霉素处理的XRCC2敲低实验组中,VIM的表达进一步下调。然而,在用多柔比星处理过表达XRCC2的PC9细胞中,VIM的表达没有上升到过表达XRCC2组的水平。这些发现证实了靶向c-Myc-XRCC2-VIM轴,可能是一种有前途的肺腺癌治疗方法。
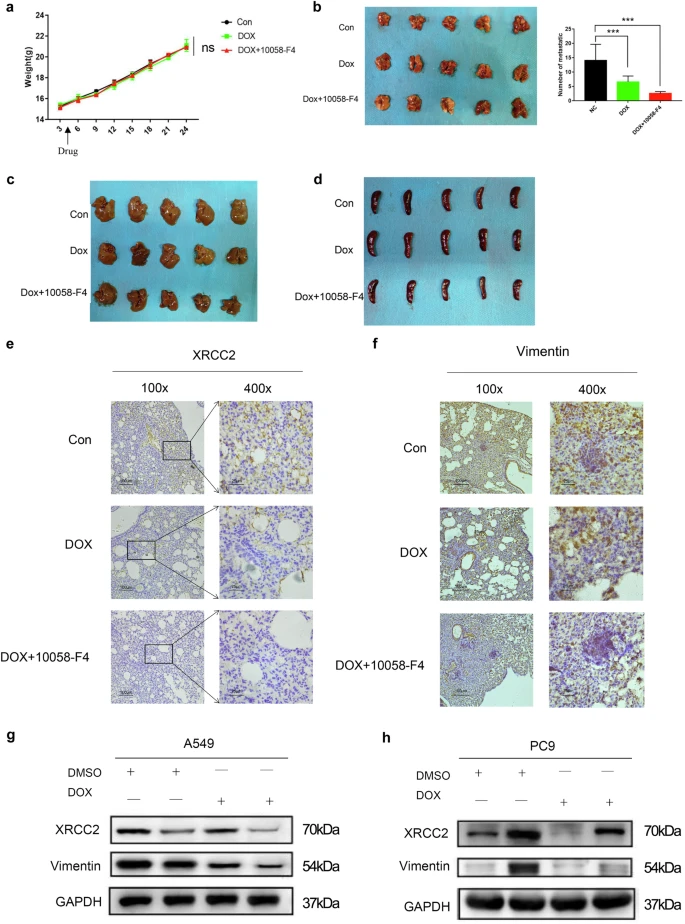
c-Myc抑制剂联合阿霉素(DOX)改善治疗效果。
研究结论
03
本研究全面探讨了HRGs在LUAD中的临床相关性和分子机制,支持其在肿瘤进展和结局中的作用。团队基于包括XRCC2在内的5个基因,开发了新的LUAD心率评分系统,这些基因与患者预后和免疫治疗反应显著相关。
虽然在大多数肿瘤中,高HR评分通常与不良预后有关,但也存在一些例外。在STAD和THYM中,高HR评分与更好的预后结局显著相关。癌症之间和癌症内部,存在相当大的异质性。某些基因可能在一种癌症中充当肿瘤抑制因子,但在另一种癌症中促进肿瘤,例如c-FOS27、STAT328和DDX529。HR基因可能在不同的肿瘤类型中,发挥不同的作用。
团队发现,XRCC2是一种新型的预后生物标志物,也是LUAD迁移和侵袭的驱动因素,为未来的临床试验提供了重要证据。团队从机制上证明了XRCC2通过去泛素化,稳定细胞骨架蛋白VIM。这种机制上的见解,不仅促进了科学界对LUAD转移的理解,而且为旨在破坏这一特定分子轴的有针对性的干预措施,开辟了途径。
有许多途径可以调节LUAD的进展和转移,例如TGF-β37或Wnt信号转导38。将c-Myc-XRCC2-VIM轴与参与LUAD进展和转移的其他已知途径进行比较,对于理解其意义至关重要。c-Myc和Dox的组合抑制,减少了体内转移,支持了其临床潜力。
参考资料:
1.Chen, P., Liu, Y., Wen, Y. & Zhou, C. Non-small cell lung cancer in China. Cancer Commun. 42, 937–970 (2022).
2.Hoppe, M. M., Sundar, R., Tan, D. S. P. & Jeyasekharan, A. D. Biomarkers for Homologous Recombination Deficiency in Cancer. J. Natl Cancer Inst. 110, 704–713 (2018).
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发