联合“铁死亡”多靶点!北京大学发文:发现胃癌治疗新策略
| 导读 | 虽然传统上认为ABCC2是一种多药耐药相关蛋白,与较差的预后相关,但之前和其它几项研究表明,胃癌(GC)的情况与此相反。研究人员的目标是探索这一发现的潜在机制。 |
8月2日,北京大学研究团队在期刊《Clinical And Translational Medicine》上发表了研究论文,题为“ABCC2 induces metabolic vulnerability and cellular ferroptosis via enhanced glutathione efflux in gastric cancer”,本研究中,研究人员发现ABCC2高表达与较好的预后相关,rs717620可通过干扰ETS1和SOX9的结合影响ABCC2的表达。GC细胞系的功能获得和功能丧失实验表明,氨基酸剥夺降低了ABCC2-high GC细胞的增殖,迁移和耐药性。ABCC2导致细胞内氨基酸库减少和细胞能量代谢中断。这种现象是由ABCC2介导的谷胱甘肽(GSH)外排引起的,从而导致氧化还原状态的变化,进而增加细胞对铁死亡的易感性。此外,研究人员还使用了患者来源的器官样组织和肿瘤样细胞群来观察ABCC2对治疗效果的影响。在ABCC2表达较高的异种移植模型中,研究人员观察到限制氨基酸摄入并抑制GPX4活性可导致明显的肿瘤消退。综上,研究结果表明,ABCC2通过介导GC中的GSH外排在氨基酸代谢和铁死亡中发挥重要作用。这一发现强调了联合多个铁死亡靶点作为ABCC2高表达胃癌有前景的治疗策略的潜力。

https://onlinelibrary.wiley.com/doi/full/10.1002/ctm2.1754
背景知识
01
胃癌是全球第五大恶性肿瘤,也是癌症相关死亡的第三大原因,2020年全球胃癌新发病例为1 089 103例,死亡人数约为768 793例。胃癌的常用治疗方法包括5-氟尿嘧啶(5-Fu)和铂类药物,这些药物引起的患者反应不同。由于其复杂的动态分子背景,胃癌是一种高度异质性的恶性肿瘤。因此,阐明驱动胃癌进展的分子机制对于开发新的有效治疗策略至关重要。
在之前的一项研究中,研究团队在一组接受新辅助化疗的胃癌患者中检测了几个基因的遗传变异,包括MTHFR、DPYD、UMPS、ABCB1、ABCC2、GSTP1、ERCC1和XRCC1。研究人员发现ABCC2-24C > T (rs717620)基因型与化疗效果和患者结局相关。其与胃癌的相关性及机制有待进一步明确。
ABCC2是ATP结合盒亚家族C的成员,发挥外排转运蛋白的作用,转运葡萄糖醛酸盐、硫酸盐和谷胱甘肽等阴离子型药物偶联物。它还促进了抗癌药物的运输,包括顺铂、长春花碱和喜树碱衍生物。多项研究证实,ABCC2的过表达使肿瘤细胞获得多药耐药。然而,最近的研究表明,ABCC2与接受FOLFOX-4治疗的结肠癌患者的无病生存率增加相关。ABCC2在结直肠癌细胞中的表达增加已被证明可增强对奥沙利铂治疗的反应。这一发现提示ABCC2可能在肿瘤进展中通过替代途径发挥抗癌药物的作用,而不仅仅是在胃癌的多药耐药中发挥作用。
谷胱甘肽(GSH)作为ABCC2的底物,是哺乳动物细胞中主要的抗氧化剂,也是GPX4的首选底物。GSH耗竭直接影响GPX4活性和稳定性,使细胞更容易发生铁死亡,铁死亡是一种独特的调节性细胞死亡形式,其特征是代谢功能障碍导致的广泛脂质过氧化。许多氨基酸代谢途径最近被发现与铁死亡相关。例如,促进三羧酸(TCA)循环的谷氨酰胺分解与氨基酸饥饿引发的坏死性细胞死亡有关,最终导致铁死亡。虽然ABCC2在GSH从肝细胞外排至胆管中起重要作用,但其在胃癌谷胱甘肽代谢和铁死亡中的作用尚不清楚。
饥饿导致的谷胱甘肽水平降低可诱发铁死亡
02
通过对TCGA数据进行相关性分析,研究人员发现铁死亡基因特征与ABCC2存在相关性。此外,来自ABCC2敲除细胞系和ABCC2低表达组织样本的RNA测序结果显著富集了铁死亡通路。研究人员使用liperfluo检测不同细胞系的过氧化脂质(LPO)。在ABCC2高表达细胞株中观察到LPO的积累,而在低表达细胞株中未观察到LPO的积累。透射电镜证实了铁死亡细胞的发生。研究还证实ABCC2促进营养剥夺诱导的铁死亡。蛋白质免疫印迹检测不同营养条件下胃癌细胞株中ABCC2表达与SLC7A11和GPX4的相关性。在正常营养条件下,ABCC2的表达对SLC7A11和GPX4的水平无显著影响。然而,在氨基酸剥夺条件下,ABCC2的高表达导致GPX4的水平显著降低,但不影响SLC7A11的表达。将不同水平ABCC2表达的细胞系暴露于铁死亡诱剂RSL3和抑制剂(ferrostatin-1),以评估其对铁死亡的易感性。与ABCC2高表达细胞株相比,RSL低表达细胞株的细胞内脂质过氧化物水平降低(p < 0.05)。Ferrostatin-1显著提高了ABCC2过表达细胞株的生存,表明铁死亡在其死亡中起作用。结果表明,ABCC2表达水平影响胃癌细胞对铁死亡的易感性。
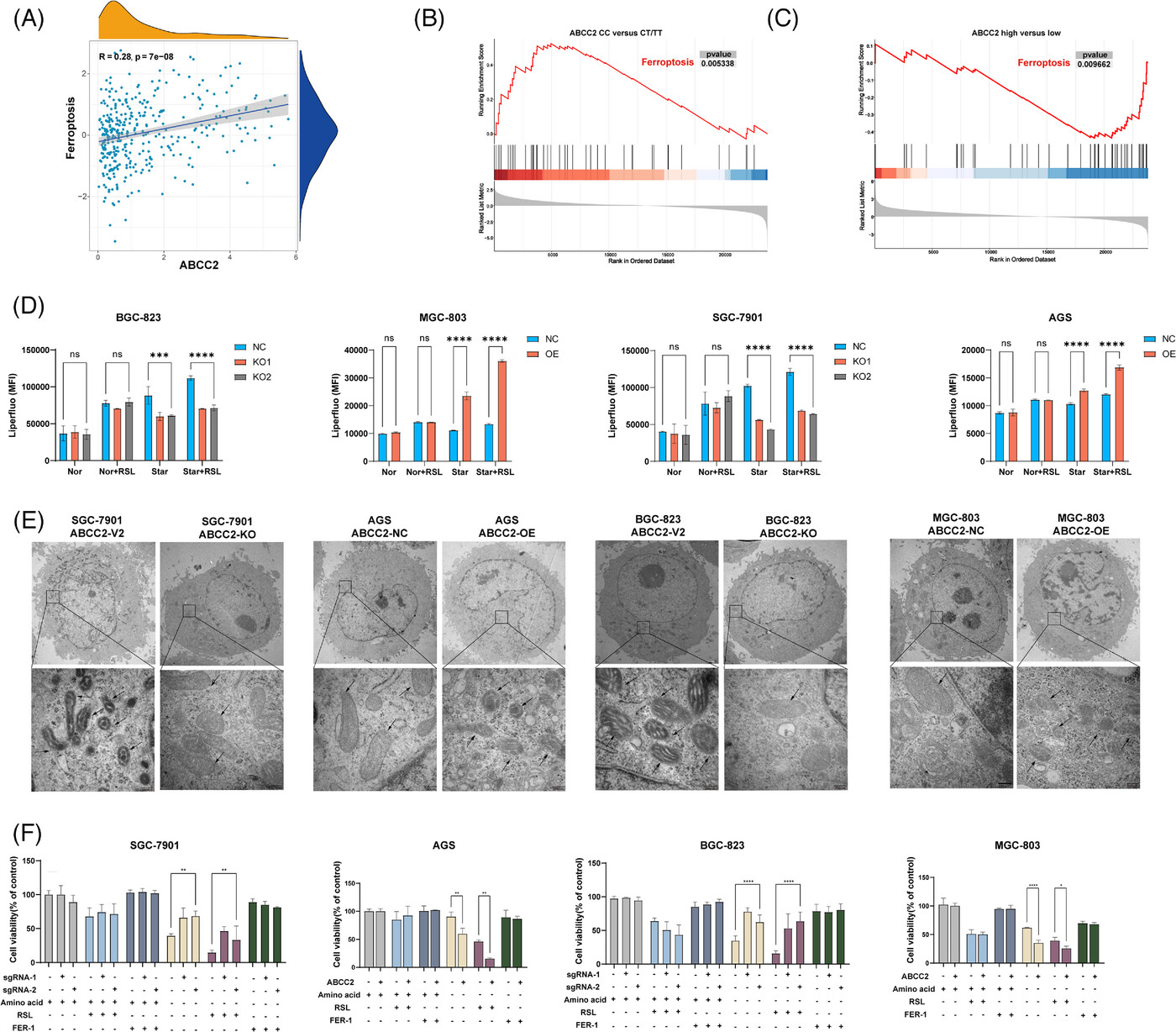
Liperfluo检测在营养剥夺条件下模拟肿瘤微环境条件下细胞内脂质过氧化变化
ABCC2与RSL3协同诱导体内铁死亡
03
为了进一步验证ABCC2在人胃癌中的作用,研究人员使用胃癌肿瘤组织建立了患者来源的类器官(PDO)模型,并用RSL3处理这些类器官并评估其生长情况。PDOs的生长速度表明,与ABCC2高表达的类器官相比,RSL3更有效地抑制了ABCC2低表达的类器官的活力。此外,Fer-1可有效提高ABCC2高表达类器官的活力。同时,研究人员使用患者来源的肿瘤样细胞簇(ptc)来模拟ABCC2 24C > t的临床相关性。手术切除后立即收集的PTC可以更好地模拟肿瘤微环境并保留原始肿瘤的基因型和表型,为化疗结果提供准确的预测。研究人员观察到具有ABCC2 24C > T的PTC对奥沙利铂和伊立替康的耐药性显著降低, 在其他化疗药物中观察到类似的趋势。
基于上述体外研究结果,研究人员通过皮下注射7901 vector细胞和7901 ABCC-KO细胞建立了NOD-SCID小鼠异种胃移植模型。在正常条件下,7901 ABCC-KO组的肿瘤重量和大小与对照组无显著差异。此外,研究结果表明,在饥饿条件下,SGC-7901 ABCC-KO组与对照组相比,肿瘤重量和大小显著增加。与ABCC2敲除组相比,经RSL3处理的ABCC2高表达组的肿瘤大小和质量显著降低。另外,ABCC2高表达的对照组中GSH水平显著降低,而MDA水平相应显著升高,支持ABCC2在胃癌细胞铁死亡中的关键作用。这些发现进一步证实了ABCC2在胃癌中的肿瘤抑制活性,并提示其作为胃癌预测生物标志物的潜力。
研究小结
04
在本研究中,研究人员进行了基于多队列的综合分析,以阐明ABCC2可以通过谷胱甘肽外排导致AA代谢紊乱,介导脂质过氧化的诱导,最终导致铁死亡的GC细胞。本研究强调了多个铁死亡靶点的联合治疗ABCC2水平升高的胃癌的潜力,这有可能揭示胃癌的发病机制,并有助于开发新的治疗策略。(转化医学网360zhyx.com)
参考资料:
https://onlinelibrary.wiley.com/doi/full/10.1002/ctm2.1754
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发