【Nature子刊】郑州大学第一附属医院唐俊楠团队推出前沿AI系统:精确评估晚期心力衰竭与肾功能不全的治疗
| 导读 | 在本研究中,团队开发了一个AI混合建模框架,并建立了一个可解释的生存评估系统:AIHFLevel。 |
2024年8月8日, 郑州大学第一附属医院唐俊楠团队在期刊《Nature Communications》上发表了题为“AI hybrid survival assessment for advanced heart failure patients with renal dysfunction”的研究论文。团队采用了AI混合建模框架来开发和验证AIHFLevel,这是一个基于Web的系统,旨在评估AHF和RD患者的长期生存状况。通过13个简单的查询,该系统使用户能够理解每个预测因子对个体生存结果的影响,从而能够在临床实践中优化管理策略和有针对性的干预措施。

https://www.nature.com/articles/s41467-024-50415-9
研究介绍
01
心力衰竭(HF)是一种危及生命的疾病,大多数心衰病例最终会进展到晚期,其特征是尽管进行了最大程度的治疗,但症状仍然存在。晚期心衰(AHF)的患病率正在增加,通常遵循逐渐恶化的模式,并伴有急性恶化发作,导致猝死。预后分层对于及时转诊至适当的中心、向患者和家属正确传达期望,以及规划治疗和随访策略非常重要。尽管有许多预后参数和工具,但准确评估AHF的结果,仍然很复杂。
慢性肾脏病(CKD)一直被认为是HF的一种普遍合并症。在所有合并症中,全因死亡率(ACM)和AHF住院的人群归因风险最高。在临床上,患有RD的AHF患者可能会遇到额外的伤害,因为这些患者经常接受较低剂量的药物,并且避免使用造影剂进行诊断测试。最近的研究强调,患有AHF和RD共病的患者通常不会得到循证医学疗法的最佳治疗,即使他们的eGFR水平由于肾功能不全而禁忌此类治疗。科学界迫切需要进一步的努力,以减轻这种风险。虽然利钠肽等新兴生物标志物提供了一些出院后的预后价值,但它们对AHF或RD病例的特异性不够,限制了它们的临床实用性。使用连续利钠肽检测,进行管理和预后指导的有效性,仍未确定。此外,HF和RD群体内的异质性,降低了单一生物标志物的疗效。因此,科学界应优先考虑这一高危人群的全面生存预测,以获得明确的预后和有针对性的干预措施。
临床数据的高维性和交互性,使得假设驱动的传统统计方法效果不佳。目前,传统预后模型对心衰的预测能力,普遍有限。人工智能(AI)越来越多地用于建立预测死亡、再入院或复合终点的预后工具;然而,没有一种算法可以完美地评估心衰结果。尽管有许多选择,但研究人员的偏好和知识限制,可能导致建模算法的使用不理想,从而导致预测能力降低。算法选择应基于各种目标和条件,并与已知规则保持一致。此外,目前的风险模型通常带有冗余或昂贵的预测因子,对于日常临床的实践来说是不切实际的,并且在初级保健中是不可获取的。预测模型的实际应用,需要在准确性、可解释性和复杂性之间取得平衡。尽管人工智能具有强大的功能,但人工智能的“黑匣子”性质,在为临床医生提供清晰的解释和透明度方面带来了挑战,这是限制许多HF预后模型临床实施的关键因素。此外,许多HF预后模型缺乏广泛的外部验证和校准,限制了它们在不同临床环境和人群中的普遍性。
在本研究中,团队旨在开发和验证一种可解释的预测系统,用于多中心回顾性纵向队列中AHF和RD患者的生存评估。该AI混合建模框架最大限度地利用了各种算法,减少了研究人员偏见的影响。团队还将该系统与临床可解释性和预后分层相结合,优化了患者管理策略。该系统(AIHFLevel)已被翻译成一个方便的网络应用程序,以方便临床医生使用,医生可在“www.hf-ai-survival.com”上获得。
研究进展
02
AIHFLevel的预后意义和预测性能
为了探索AIHFLevel评分与ACM风险比(HR)之间潜在的非线性关系,团队初步估计了与受限三次样条分析的关联。在复制和发现队列中,团队始终观察到非线性关联的模式以及AIHFLevel的增加:ACM 风险“从快到低增加”(P整体<0.0001,P非线性< 0.0001) 。单因素Cox回归分析,强调了AIHFLevel作为ACM临床预测因子的意义(复制队列:HR=1.615,P < 0.0001,95%CI=1.417–1.863;发现队列:HR = 2.245,P < 0.0001,95%CI = 2.039–2.472)。为了评估 AIHFLevel的预后效果,团队根据中位数分数将受试者分为高组和低AIHFLevel组。ACM的Kaplan-Meier曲线表明,在复制队列和发现队列中,高AIHFLevel组的生存期均显著缩短(Log-rank 检验,P < 0.0001)。通过ROC分析量化了AIHFLevel的鉴别力,在6个月、12个月、24个月和30个月时的AUCs,显示出很强的预测准确性:复制队列为0.902、0.932、0.932、0.903,发现队列分别为0.931、0.952、0.973、0.976。6个月、12个月和24个月生存预测的校准分析显示,与复制和发现队列中观察到的结果高度一致。此外,决策曲线分析(DCA)证实了AIHFLevel在6个月、12个月和24个月生存期的显著临床效用和净获益,验证了其在临床决策中的价值。在Meta队列中观察到相当的卓越性,其中AIHFLevel评分与ACM风险之间,存在明显的稳健正相关(P整体< 0.0001,P非线性< 0.0001) (HR = 1.878, P < 0.0001, 95%CI = 1.770–1.992))。高AIHFLevel组长期ACM发生率显著更高(P < 0.0001)。6个月、12个月、24个月和30个月的AUC,证实了预测的卓越性:分别为0.925、0.947、0.965和0.960。校准和DCA图,进一步证实了AIHFLevel的预测准确性和临床益处,增强了其在不同预后阈值下的适用性。
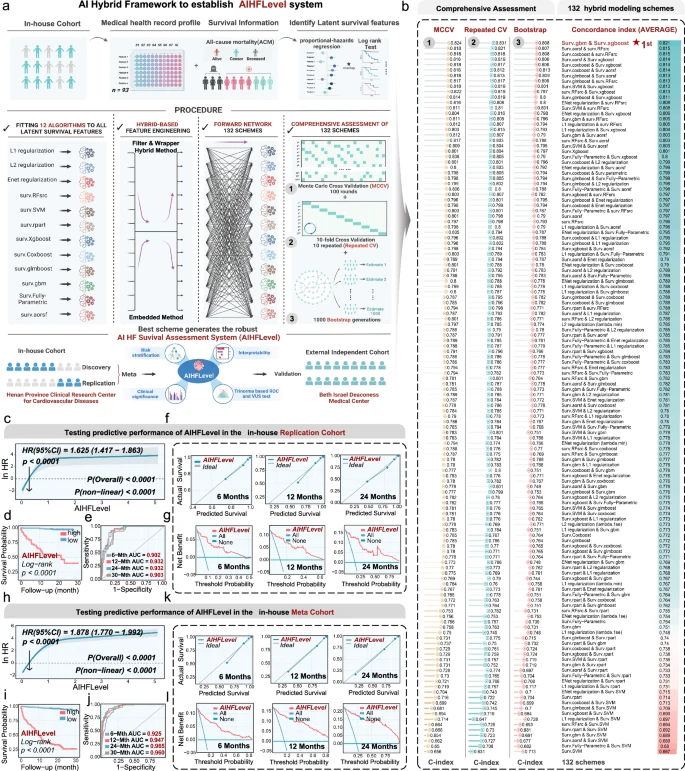
AIHFLevel的预测性能和预后价值。
便捷的Web应用程序,用于临床实用性
基于Django Web框架,AIHFLevel系统已部署在用户友好的应用程序(https://www.hf-ai-survival.com)中,旨在增强其在临床场景中的实用性。该系统包含一系列用于个体患者分析的功能,包括预后分层、长期生存概率的计算、指定时间点的全因死亡率预测、局部解释和预测因子贡献。
为了直观地演示实际应用,团队提出了一个示例案例。用户只需通过13个查询输入数据:年龄(72 岁)、心律失常合并症(No)、CAD 合并症(Yes)、CKD分期(IV)、Cr(101.3 μmol/L)、LVEF(51%)、eGFR(23.490 ml/(min/1.73 m3)、淋巴细胞(23.8%)、MCHC(328.00 g/L)、SV(42%)、CTnI(0.35 ng/ml)、TBIL(2.79 ng/ml)和兴趣时间点(600 天) 。进入后,系统自动执行条件推理生存树,将该个体归类为高风险状态。随后,它生成了一条长期生存曲线,计算出600天时,全因死亡率为45.5%的概率。条形图提供了随时间变化的生存曲线的直观视图,预测在180天、365天、730天、900天、600天的生存概率,分别为78.6%、61.5%、48.3%、45.5%和54.5%。此外,雷达图显示了预测因子对生存评估的贡献。据观察,eGFR、SV、CTnI、年龄和Cr的值,将决策推向了更差的预后;而Cr、LVEF和MCHC,则将决策推向了良好的预后。这表明,通过有针对性的干预措施或管理策略,使大多数预测值更接近其正常范围。例如,eGFR和SV,可以减轻该个体患ACM的风险,尽管总体预测将该病例推入高风险预后。总之,该系统可以帮助医生选择最佳治疗方法,并根据输出风险分层和个人信息的可解释性,提供个性化建议以改善结果。
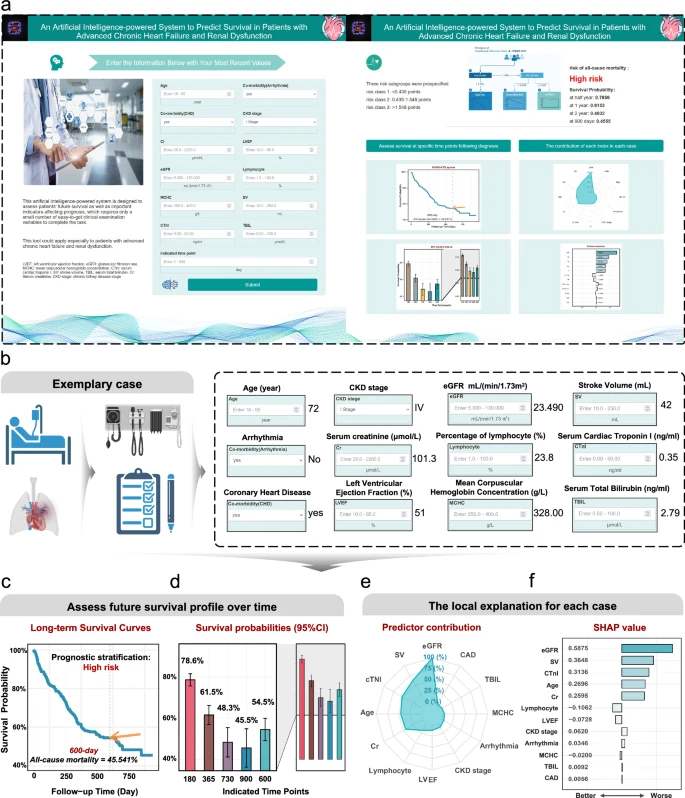
用于临床的便捷Web应用程序。
研究结论
03
本研究通过开发集成混合模型框架——AI混合建模框架,超越了现有的风险预测框架。通过这个过程,团队最大限度地减少了冗余信息,并建立了一个基于12个预测因子的系统,称为AIHFLevel。建模框架通过利用一系列多样化和独立的模型来发挥作用,这使得AIHFLevel能够减少泛化误差,并提高预测的可靠性。
本研究不仅应用了现有的风险预测学习算法,而且创新性地开发了集成混合模型框架,可能标志着RD合并症AHF风险预测领域的重大进展。团队借鉴了AI建模中的既定概念,特别是结合了基于集成的方法的混合范式。团队的方法不是选择最佳的个体学习算法,而是侧重于构建集成建模方案,以提高生存评估的准确性,特别是对于AHF与RD的合并症。团队采用了12种不同的AI学习算法,并通过集成3种独特的特征工程方法(Embedded、Filter 和 Wrapper)拓宽了潜在的模型方案。这种集成减少了泛化错误,并确保了在各种临床场景中的稳健的泛化性。该框架的新颖之处包括:(1)多种学习算法的集成;(2)先进的特征工程技术;(3)基于集成的建模;(4)综合评估策略。
在本研究中,CRCCD中心和Beth Israel Deaconess Medical BIDMC中心在随访、流失、检测和选择时间表方面的差异,为评估AIHFLevel的普遍性,提供了一个强大的测试平台。尽管面临挑战,但AIHFLevel已被证实是风险分层和评估的可靠工具。
团队将AIHFLevel与从AHF患者收集的近100个临床变量和分子特征进行了比较。根据一致性指数和IBS,AIHFLevel在所有队列中均优于其他特征,表明这是评估预后和推动临床患者个性化管理的潜在替代方案。AIHFLevel表现出比经典生物标志物更高的准确性,尤其是炎症指示剂。AIHFLevel通过全面的算法网络进行了优化,具有优越的外推可能性,与其他模型相比具有显著优势。AIHFLevel及其改装版本在各个队列中的表现都优于比较模型,再次肯定了AIHFLevel的优越性,并展示了其弹性和固有的预测能力。AIHFLevel不仅准确预测了AHF&RD患者的预后,而且具有简化的特征集,大大提高了其临床实用性和更广泛应用的潜力。
本研究在利用SHAP方法揭开AI模型的“黑匣子”性质方面,具有显著优势。预测模型可以通过使用Django框架开发的基于Web的工具方便地访问,从而在临床医生中更广泛地传播。AIHFLevel对可解释性的直接整合,凸显了年龄、GFR、cTNI和血清肌酐等因素,在影响AHF和RD患者长期生存结果方面的关键作用。该系统提供了预测因子的个性化和可视化。此功能允许用户查看每个因素如何在个体水平上影响生存结果,通过有针对性的干预措施或管理策略,将大多数风险预测值更接近其正常范围,可以降低患ACM的风险,即使总体预测将病例归类为高风险。
应注意几个限制。尽管使用大量异质性患者群体是一项观察性研究,但未来的验证应在前瞻性多中心队列中进行。此外,还需要进一步的随机和对照研究,以确定根据AIHFLevel系统的个体化和及时治疗措施,是否可以改善患者的预后。尽管该系统可以告知每个病例的12个临床指标对生存率的贡献,但超声心动图可能不适用于所有患有RD的AHF患者,尤其是在初级保健诊所。此外,在治疗使用方面,预后因素无法替代对预测因素的需求。如果系统显示患者的总体预后评分较差,医生应为她或他进行额外的加强治疗。例如,如果年龄是解释最差生存概率的第一个特征,那么强化治疗的决定,可能与合并症状态或病理学作为主要因素的情况,有很大不同。该系统将最终决定权交还给医生。
参考资料:
1.Crespo-Leiro, M. G. et al. Advanced heart failure: a position statement of the Heart Failure Association of the European Society of Cardiology. Eur. J. Heart Fail 20, 1505–1535 (2018).
2.Fang, J. C. et al. Advanced (stage D) heart failure: a statement from the Heart Failure Society of America Guidelines Committee. J. Card. Fail 21, 519–534 (2015).
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发