靶向“巨噬细胞”!武汉市第三医院(武汉大学附属同仁医院):胰腺癌免疫治疗新策略
| 导读 | 本研究主要探讨胰腺癌(PAAD)组织中IRF7调控M1型巨噬细胞RPS18转录的分子机制,以及IRF7通过外泌体转移RPS18至PAAD细胞以及对ILF3表达的调控。 |
8月8日,武汉市第三医院(武汉大学附属同仁医院)研究团队在期刊《Clinical And Translational Medicine》上发表了研究论文,题为“Single-cell sequencing combined with spatial transcriptomics reveals that the IRF7 gene in M1 macrophages inhibits the occurrence of pancreatic cancer by regulating lipid metabolism-related mechanisms”,本研究中,研究人员通过scRNA-seq和ST技术的联合分析,发现PAAD样本中的M1型巨噬细胞与脂代谢信号密切相关,而M1型巨噬细胞与癌细胞呈负相关。预后风险评分模型的构建发现RPS18和IRF7是M1型巨噬细胞的两个预后相关基因,分别呈负相关和正相关。机制上,研究人员发现M1型巨噬细胞中的IRF7可以抑制RPS18的转录,减少RPS18通过外泌体转移到PAAD细胞,从而影响PAAD细胞中ILF3的表达。M1型巨噬细胞中的IRF7/RPS18还可抑制PAAD细胞的脂质代谢、细胞活力、增殖、迁移、侵袭和瘤内形成能力,同时促进细胞凋亡。靶向IRF7/RPS18的M1型巨噬细胞可能是未来治疗PAAD的一种有前景的免疫治疗方法。

https://onlinelibrary.wiley.com/doi/full/10.1002/ctm2.1799
背景知识
01
胰腺癌(PC)是全球癌症相关死亡的主要原因,其5年生存率较低。胰腺癌(PAAD)是最常见的PC类型,约占所有PC的85% ~ 90%。这可能是由于大多数患者确诊时已处于晚期,因此可供选择的治疗方案有限。近年来,人们越来越重视了解胰腺癌的分子机制,以开发新的治疗模式。巨噬细胞作为一种免疫细胞,在包括PC在内的多种癌症中发挥着关键作用。巨噬细胞的几个亚型(包括M1和M2)在癌症进展中发挥着截然不同的作用。M1型具有抗肿瘤功能,而M2型具有促进肿瘤的特征。
最近的研究表明,脂质代谢在癌症的发生发展中起着重要作用,尤其是在肿瘤微环境中的巨噬细胞等免疫细胞中。单细胞RNA测序(scRNA-seq)和空间转录组学(ST)技术的进步使科学家能够在单个细胞水平上研究PC中巨噬细胞的精确功能。这些技术提供了宝贵的见解,使研究人员能够全面理解巨噬细胞和癌细胞之间的复杂动力学,以及这些相互作用如何影响癌症进展。
肿瘤微环境中的细胞通讯,特别是通过外泌体(Exos),已被证明在胰腺癌进展中具有重要功能。外泌体是能够从一个细胞转运到另一个细胞的微小囊泡,促进多种生物活性分子的转运,包括蛋白质、RNA和代谢物。这种能力使得细胞在促进细胞间通讯方面至关重要,特别是在癌症进展中。
IRF7在M1巨噬细胞中的调节改变脂质代谢,抑制PAAD细胞的增殖、活力和迁移
02
多项研究表明,调节脂质代谢可以影响癌细胞的生物学功能,促进癌症的发展。巨噬细胞可以影响细胞脂质代谢过程。为了研究IRF7+ M1巨噬细胞对PAAD细胞脂质代谢途径和生物学功能的影响,研究人员利用CRISPR/Cas9基因编辑技术构建了IRF7敲除(IRF7- ko) M1巨噬细胞(IRF7- wt作为IRF7- ko的野生型对照)。研究人员采用RT-qPCR和蛋白质免疫印迹实验分析评估IRF7和RPS18在单细胞克隆中的表达水平,选择IRF7零表达的单细胞克隆进行后续扩增。研究发现,IRF7-KO细胞表现出显著增加的RPS18表达水平和增强的RPS18 mRNA稳定性。此外,研究人员通过慢病毒转导建立过表达IRF7的M1巨噬细胞(e-IRF7,以e- nc为对照),并通过RT-qPCR和Western blot验证IRF7的转染效率和RPS18的表达水平。尤其是,结果表明,RPS18在e- irf7细胞中的表达水平变化与IRF7-KO细胞相反,RPS18 mRNA的稳定性明显降低。
接下来,研究人员将不同组M1巨噬细胞的胞外囊泡与PAAD细胞系(PANC-1/BxPC-3)共培养。然后,使用代谢组学分析量化共培养后PAAD细胞中脂质代谢物的总含量。结果显示,与IRF7-WT组相比,IRF7-KO组PANC-1和BxPC-3细胞中脂质代谢物的总含量显著增加。相反,与e- nc组相比,e- irf7组PANC-1和BxPC-3细胞中脂质代谢物的总含量显著降低。
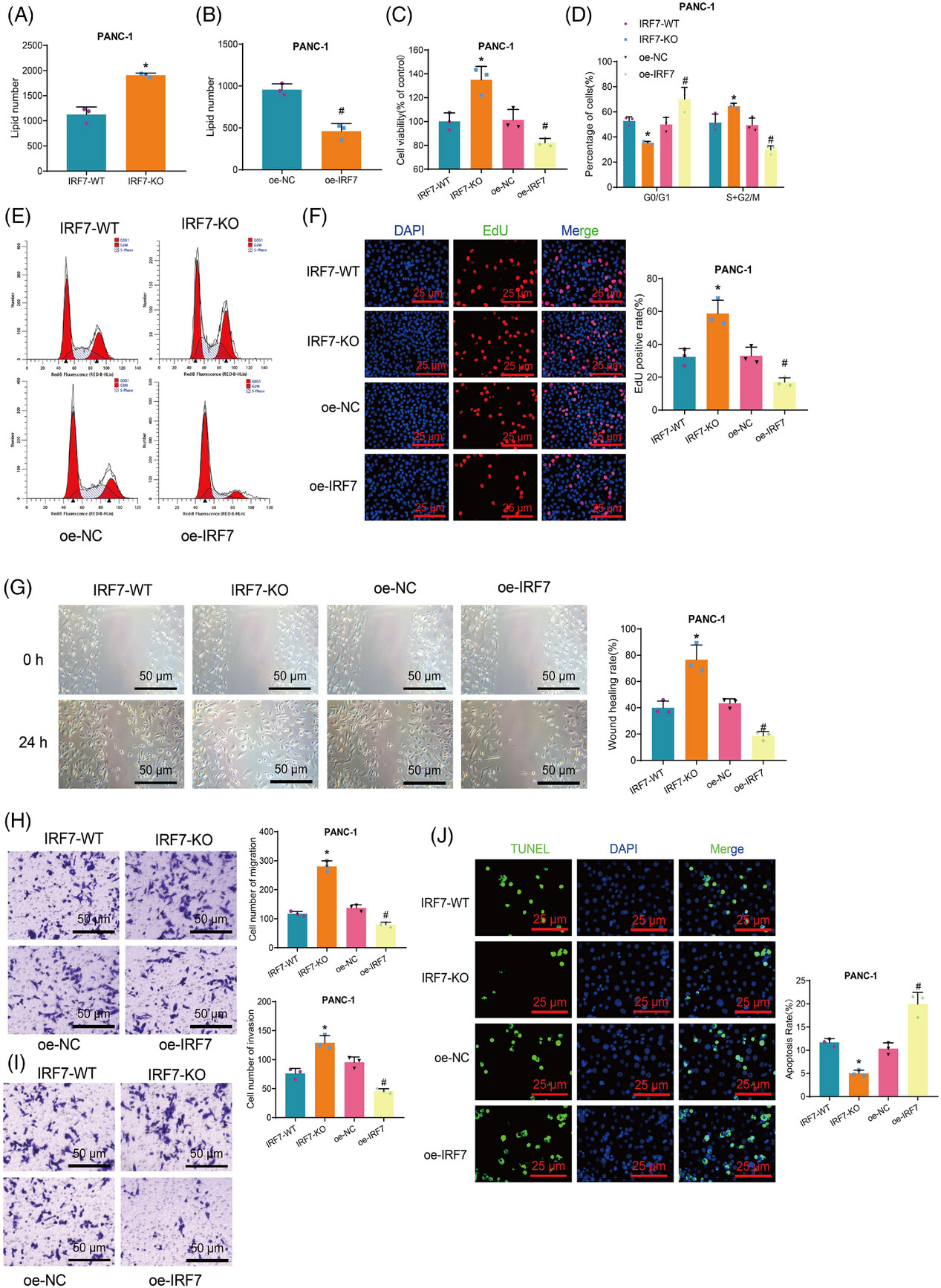
IRF7对胰腺腺癌细胞生物学功能的影响
此外,研究人员使用3-(4,5-二甲基噻唑-2-酰基)-2,5-二苯基溴化四唑(MTT)实验评估细胞活力,通过流式细胞术和5-乙基-2 ' -脱氧尿苷(EdU)实验评估细胞分裂和增殖能力,使用划痕和迁移实验评估细胞迁移和侵袭能力,并用末端脱氧核苷酸转移酶dUTP尼克末端标记(TUNEL)染色方法评估细胞凋亡。结果表明,与IRF7-WT组相比,IRF7-KO组表现出更高的细胞活力、增殖和迁移能力。此外,S+G2/M期细胞比例升高,细胞凋亡减少。与e- nc组相比,e- irf7组细胞活力、增殖和迁移能力下降,S+G2/M期细胞比例下降,细胞凋亡水平增加。
上述结果表明,IRF7可抑制M1巨噬细胞脂质代谢,抑制PAAD细胞的活力、增殖、迁移、侵袭,促进细胞凋亡。
另外,研究人员通过免疫组化染色检测Ki67在小鼠肿瘤组织中的表达。结果表明,与NC-Exos + oe-NC组相比,oe-IRF7-Exos + oe-NC组小鼠肿瘤组织中ki67阳性细胞的百分比降低。相反,与e- irf7 - exos + e- rps18组相比,e- irf7 - exos + e- nc组小鼠肿瘤组织中ki67阳性细胞的百分比有所上升。这些结果表明,IRF7在M1型巨噬细胞中过表达导致RPS18转录受到抑制。因此,M1-Exos减少了RPS18向PAAD细胞的转移,从而抑制了PAAD细胞中ILF3的表达。此外,抑制ILF3表达进一步阻碍脂质代谢,最终抑制体内PAAD细胞的肿瘤形成。
研究小结
03
本研究阐明了M1巨噬细胞IRF7/RPS18与PAAD细胞脂质代谢的关系及其在增殖、迁移和凋亡中的作用。这为PAAD的发病、进展和免疫治疗提供了新的视角。通过使用scRNA-seq和ST对PAAD组织进行深入分析,可以更准确地识别与癌症相关的特定细胞群和信号通路。如果进一步的验证证实了IRF7的功能和机制,它可能成为PAAD治疗的有效靶点,为患者提供更多的治疗选择和改善预后。(转化医学网360zhyx.com)
【参考资料】
https://onlinelibrary.wiley.com/doi/full/10.1002/ctm2.1799
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发